2月21日,中国国家药监局药品审评中心(CDE)官网最新公示,阿斯利康(AstraZeneca)的抗PD-L1单抗度伐利尤单抗注射液又一项新适应症上市申请获得受理,具体适应症尚未披露。公开资料显示,度伐利尤单抗此前已经在中国获批治疗非小细胞肺癌、广泛期小细胞肺癌、胆道癌适应症,此外该产品还有至少3项新适应症上市申请已经获CDE受理,正处于审评阶段。
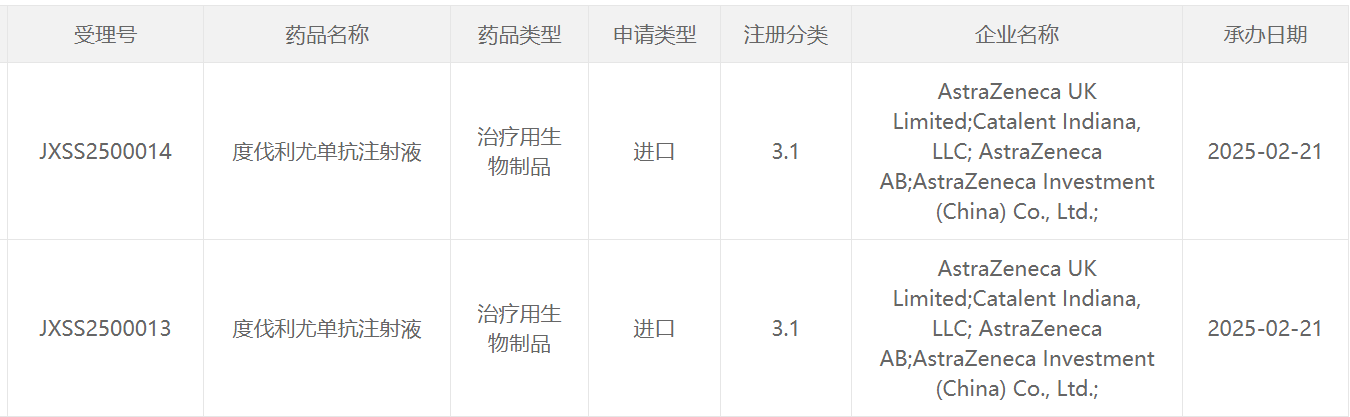
截图来源:CDE官网
度伐利尤单抗(durvalumab,商品名:英飞凡,Imfinzi)是一个人源化的PD-L1单克隆抗体,能够阻断PD-L1与PD-1和CD80的结合,从而阻断肿瘤免疫逃逸并解除对免疫反应的抑制。
在中国,度伐利尤单抗于2019年12月首次获NMPA批准,用于在接受铂类药物为基础的化疗同步放疗后未出现疾病进展的不可切除、III期非小细胞肺癌患者的治疗;2021年7月,该药获批与依托泊苷联合铂类(卡铂或顺铂)化疗方案联合,用于广泛期小细胞肺癌的一线治疗;2023年11月,度伐利尤单抗获NMPA批准,联合吉西他滨和顺铂用于局部晚期或转移性胆道癌(BTC)成人患者的一线治疗。
在全球范围内,度伐利尤单抗目前已在多个国家获批用于治疗多种类型的肺癌。度伐利尤单抗是在放化疗后疾病无进展的III期不可切除的NSCLC患者的全球标准疗法。此外,其还被批准联合新辅助化疗用于可切除NSCLC的围手术期治疗,以及与Imjudo (tremelimumab)短期疗程和化疗联合用于转移性NSCLC的治疗。
针对小细胞肺癌(SCLC),度伐利尤单抗已经被批准用于在接受铂类同步放化疗(cCRT)后病情未进展的局限期小细胞肺癌(LS-SCLC)成人患者;联合化疗(依托泊苷和卡铂或顺铂)治疗大分期SCLC。
除了肺癌适应症外,度伐利尤单抗还在多个国家被批准联合化疗(吉西他滨加顺铂)治疗局部晚期或转移性胆道癌、联合tremelimumab治疗不可切除的肝细胞癌(HCC)。在日本和欧盟,度伐利尤单抗还被批准作为单药疗法治疗不可切除的肝细胞癌。在美国,度伐利尤单抗也被批准与化疗(卡铂和紫杉醇)联合使用,然后再使用度伐利尤单抗单药治疗原发性晚期或复发性子宫内膜癌错配修复缺陷(dMMR)。在欧盟,度伐利尤单抗联合化疗后再加olaparib(奥拉帕利)和度伐利尤单抗被批准用于配修复功能正常(pMMR)晚期或复发子宫内膜癌患者。
作为广泛开发计划的一部分,度伐利尤单抗正在作为单一治疗和与其他抗癌治疗联合用于SCLC、NSCLC、膀胱癌、乳腺癌、几种胃肠道和妇科癌症以及其他实体肿瘤患者。
比如,今年2月15日,阿斯利康宣布度伐利尤单抗围手术期治疗方案,与新辅助化疗联用,在肌层浸润性膀胱癌(MIBC)患者中改善了无事件生存期(EFS)和总生存期(OS)。基于该研究结果,度伐利尤单抗正在欧盟、日本及其他多个国家和地区接受审评。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..