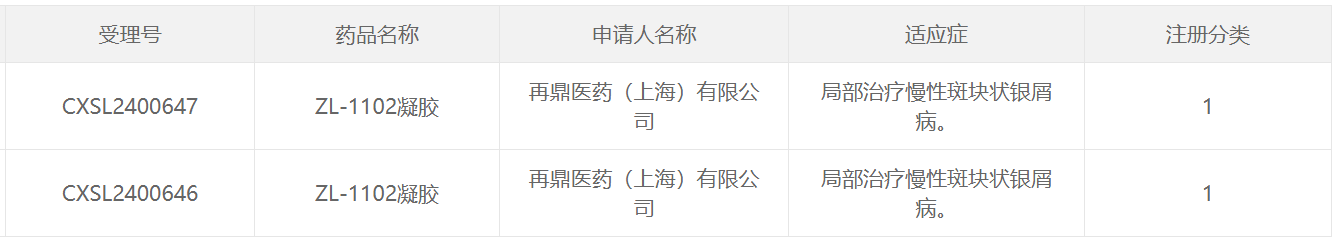
 截图来源:CDE官网
截图来源:CDE官网
斑块性银屑病是银屑病中最常见的类型,其中约70~80%的斑块状银屑病病例为轻中度。局部治疗是轻中度斑块状银屑病的标准疗法。然而目前的治疗选择疗效有限或长期使用存在安全问题。
ZL-1102是一款在研新型全人源VH抗体片段,靶向作用于IL-17A细胞因子。它被配制成水凝胶。由于这一类分子体积小,与全长单克隆抗体相比,ZL-1102具有更高的靶标亲和力和组织渗透性。再鼎医药此前新闻稿介绍,由于具有更好的安全性和耐受性的潜力,ZL-1102这款局部治疗产品有望将现有IL-17靶向疗法的使用扩展到群体庞大的症状不太严重的慢性斑块状银屑病患者。
再鼎医药此前报告了ZL-1102在轻中度慢性斑块状银屑病患者的概念验证性研究数据。该研究显示,在治疗4周时,ZL-1102组靶皮损的局部银屑病面积和严重程度指数(PASI)评分显示出高出安慰剂组约45%的相对改善。随着时间的推移,ZL-1102在4周内持续表现出比安慰剂更高的应答率,且在治疗结束后可维持应答到研究的第6周。
该研究的主要研究者此前在新闻稿中表示,该研究中观察到ZL-1102局部疗法对于轻中度慢性斑块状银屑病患者可快速起效,并有望持久响应,证实ZL-1102是一款可对银屑病皮肤渗透并产生临床应答的局部生物制剂。
2024年5月,再鼎医药宣布启动ZL-1102的全球2期临床研究,用于局部治疗慢性斑块状银屑病。这是一项5臂试验,约250名患者将接受为期16周的局部治疗。研究的主要终点是达到mPASI75的患者的比例,即治疗第16周时,mPASI评分较基线至少下降了75%。研究还将确定确定不同剂量的ZL-1102与安慰剂相比在治疗结束时的疗效。根据ClinicalTrials官网,该研究拟在澳大利亚10个研究中心开展,患者接受ZL-1102凝胶或安慰剂每日两次给药(BID)。
IL-17A作为促炎细胞因子,通过多种途径建立维持银屑病患者表皮炎症反应的反馈回路、促进角质形成细胞的增殖并抑制其分化、破坏皮肤屏障,在银屑病发病机制中起到关键作用。公开资料显示,针对IL-17A靶点的新药近期不断迎来新进展。尤其是今年以来,优时比(UCB)公司的抗IL-17A/F单抗比奇珠单抗、恒瑞医药IL-17A单抗夫那奇珠单抗、智翔金泰IL-17A单抗赛立奇单抗陆续在中国获批上市。此外,通过公开渠道查询,全球范围内还有数十款靶向IL-17的新药正在研发中,绝大多数为单抗产品。
本次ZL-1102在中国获批临床,意味着这款作用于IL-17A细胞因子的新型全人源VH抗体片段在研新药也将在中国启动临床研究。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..