精彩内容
近年来,国家陆续出台多项利好政策,合力驱动儿科药创新研发。2023年至今,已有120余个儿科药获NMPA批准上市,其中39个为首次获批,集中在神经系统药物、抗肿瘤和免疫调节剂等治疗大类;32个通过优先审评审批程序得以加快上市,涉及恒瑞医药、济川药业等知名药企。踏入七月,新一轮国谈正式启动,56款儿科药有望冲线2024国谈,溶液剂及注射剂在数量上领跑;独家品种(含剂型独家,下同)为主力军,占比超过60%。
中国是全球第二大儿科用药市场,根据国家统计局的数据,2020年0-14岁少儿人口数为2.53亿人,约占全国总人口数的18%。随着国家“三胎”政策的全面放开,儿科用药需求也随之增加。
米内网数据显示,近年来我国儿科药市场销售额均保持良好的增长态势,除2020年受疫情影响首次出现下滑,其余年份销售额增速均在6%以上,市场潜力十足。其中,儿科中成药2023年在中国三大终端六大市场(统计范围详见本文末)合计销售规模已突破180亿元。
近年来中国三大终端六大市场儿科中成药销售趋势(单位:万元)
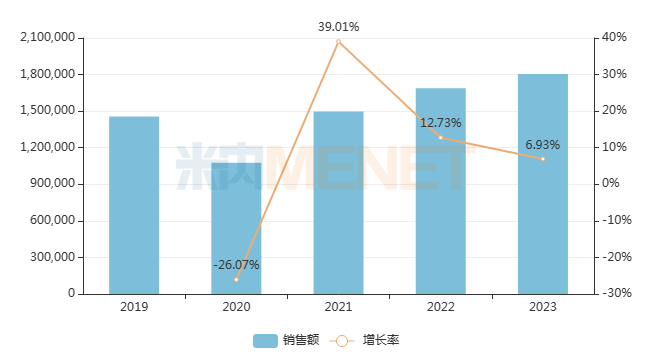
来源:米内网格局数据库
270余款儿科药强势来袭!恒瑞、济川......成绩亮眼
伴随临床用药需求的激增,近年来儿科药申报量、获批量均呈现明显上升趋势,2019年至今,中国已获批的儿科药数量超过270个,且获批数量逐年递增,2019-2023年四年间获批上市的儿科药数量分别为19个、26个、47个、66个和92个,而今年以来已有近30个儿科药获批,进一步缓解儿童适宜剂型少、规格少等问题。
据不完全统计,2023年至今获批的儿科药中,约有39个品种为首次获批上市,其中口服液体剂占比接近四成,满足儿科用药便利性的需求;治疗大类上以神经系统药物、抗肿瘤和免疫调节剂居多,分别有11个和8个品种进账,消化系统及代谢药(6个)、全身用抗感染药物(4个)则位居其后。
具体产品方面,如:兴齐眼药的2.4类新药硫酸阿托品滴眼液,于今年3月获批上市,是国内首款获批用于延缓儿童近视进展的低浓度硫酸阿托品滴眼液。据国家卫健委颁布的《儿童青少年近视防控适宜技术指南》指出,低浓度阿托品是被推荐的抗胆碱类药物,具有阻断中枢神经系统以及周围神经系统中神经递质的作用,可控制近视加深。
从审评审批路径上看,共有32个药品(不含预防用生物制品,下同)通过优先审评审批程序得以加快上市,其中独家品种有22个,占比接近七成,包括恒瑞医药的广谱抗肿瘤药环磷酰胺胶囊、石家庄四药的罕见病Dravet综合征治疗药司替戊醇干混悬剂、济川药业用于小儿风热感冒挟滞证的中成药小儿豉翘清热糖浆、以及阿斯利康的Ⅰ型神经纤维瘤病治疗药硫酸氢司美替尼胶囊等。
56款儿科药剑指新国谈,独家品种“霸屏”
近年来,系列指导政策的频频出台,一方面推动着临床价值明确、疗效显著、安全性高的儿科药加速面世,另一方面也加快了其准入医保的速度,提高更多患儿的用药可及性。
比如:2017版医保目录新增91个儿科药品种,目录中明确适用于儿童的药品或剂型增加至540个。随后,2019-2023版医保目录调整方案中也分别指出,重点调整及优先纳入儿科药,其中2021版医保目录经谈判准入的34个独家儿科药平均降价55.6%;2023版医保目录共纳入9个儿科药,独家品种有4个,分别为齐鲁制药的孟鲁司特钠口溶膜、力品药业的盐酸可乐定缓释片、茂康药业的盐酸氟西汀口服溶液和Neurelis的地西泮鼻喷雾剂。
上周五(6月28日),国家医保局公布的“2024版国家医保目录调整工作方案”(下文简称:《调整方案》)中指出,新一轮国谈重点继续向儿科药倾斜:纳入鼓励仿制药品目录或鼓励研发申报儿科药清单的药品,且于2024年6月30日前获NMPA批准上市的均可申报。
据不完全统计,目前至少有56款儿科药有望参与2024年国谈,其中独家品种“霸屏”,占比超过60%;剂型上溶液剂为主力军,占比接近四成,注射剂和片剂各占23%;从治疗大类看,神经系统药物、消化系统及代谢药、抗肿瘤和免疫调节剂分别占据9个及以上的席位。
恒瑞医药的尼莫地平口服溶液用于颅内囊性动脉瘤破裂的蛛网膜下腔出血,而口服液体剂具有剂量灵活和易于吞咽等特点,尤其适用于老年人以及儿童群体,2016年该药被纳入第一批鼓励研发申报儿科药名单。苑东生物的马来酸依那普利口服溶液为第三批鼓励研发申报儿科药品种,也是国内首个儿童专用的血管紧张素转化酶抑制剂(ACEI)口服溶液,若该药能顺利进保,有望提高各年龄段高血压、心力衰竭以及肾脏疾病患儿的用药可及性。
小儿紫贝宣肺糖浆是健民药业的1.1类中药新药,其组方源于国家级名老中医经验方,具有良好的临床应用基础,在治疗小儿急性支气管炎风热犯肺证咳嗽方面疗效显著,且安全性好。吸入用一氧化氮是兆科药业旗下的一款血管扩张剂,可用于改善脆弱新生儿群体的氧合;2020年1月,该药被CDE以“治疗儿科罕见病”为由纳入优先审评,随后于2022年3月获批上市,是全球首款获批的医用NO气体......
骄阳似火,七月已至。根据《调整方案》的工作安排(5-6月:准备阶段;7-8月:申报阶段;8-9月:专家审评阶段;9-11月:谈判/竞价阶段;11月:医保目录公布),2024年国谈已进入申报阶段。届时,哪些品种能成功入选,年底有望见分晓。
利好政策纷至沓来,推动儿科药创新研发
作为特殊的用药群体,儿童有自己独特的生理特点,而目前儿科药市场供应仍呈现品种少、剂型少、规格少、特药少的“四少”现状。为解决儿科临床“急难愁盼”的用药需求,今年以来,国家各职能部门多措并举强化儿童用药保障,合力为企业创新研发提供新思路。
在儿科药研发环节,针对儿童专科用药缺乏以及适应症不均衡等问题,国家卫健委公示了《第五批鼓励研发申报儿童药品建议清单》,涉及阿尼芬净注射剂、柯拉特龙乳膏剂等23个品种、35个品规,覆盖神经系统药物、心脑血管系统用药、抗肿瘤和免疫调节剂及全身用抗感染药物等治疗领域。
在注册申报环节,为更好服务企业,促进儿科药研发,提升申报资料质量,国家药监局一方面与研发机构密切沟通,指导其更好、更快地推进研发工作;另一方面给予研发企业优先审评审批等政策支持,日前,优先审评审批的儿童用药清单在国家药监局药品审评中心网站正式“上线”。
在临床使用环节,为解决儿科临床超说明书使用的问题,国家药监局于2023年5月发布了《已上市药品说明书增加儿童用药信息工作程序(试行)》,并于2024年4月发布《药审中心关于已上市药品说明书增加儿童用药信息工作细则(试行)》,对品种遴选范围、说明书修订与审核流程,以及品种申报程序等作进一步的明确,提高临床安全用药水平。
相关部门表示,国家下一步将继续加大政策倾斜力度,推进儿科药优先审评审批,增强对儿科药的知识产权保护;针对儿科药临床需求制定技术指导原则,充分考虑儿科药的安全性和适宜性等特殊要求,提升企业研发水平,加快研发速度。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..