2023年是礼来大放光彩的一年,截止9月1日收盘,股价从2月底低点311美元涨到约557美元,涨幅高达79%。8月初,礼来公布了半年报,报告显示第二季度的总收入同比增长28%,受此强劲财报影响,礼来盘中股价一度跳涨18%,市值更是超过5000亿美元,成为全球第一家市值超过5000亿美元的药企。
不止步于此,礼来还在继续酝酿下一个目标:冲击万亿市值。礼来能做到吗?
众所周知,支撑一个公司股价和市值上升的主要因素是营业收入和未来预期,今年上半年,礼来就有多款药物突破十亿美元大关,包括度拉糖肽(Trulicity)、阿贝西利(Verzenio)、替尔泊肽(Mounjaro)、恩格列净(Jardiance)和依奇珠单抗(Taltz)等。
司美格鲁肽的成功给了GLP-1类降糖减重药物无限想象的可能,替尔泊肽是首款获批的GLP-1/GIP双重激动剂,有望获得比司美格鲁肽更强的效果,自去年获批上市以来销售额急剧上升,替尔泊肽今年上半年销售额就达到15.48亿美元,目前正在迅速放量,今年有望突破40亿美元,未来更是不可限量。
礼来在肿瘤领域也有多款重磅产品,其中阿贝西利销售额最高,今年上半年卖了16.78亿美元。它是目前唯一一个被FDA批准的用于辅助治疗以及被NMPA批准用于早期乳腺癌高危患者的CDK4/6抑制剂,销售额正在放量增长。
自免领域不满足已有的皮下注射IL-17单抗药物,8月9日礼来完成了对DICE的收购,希望开发口服小分子IL-17抑制剂,进一步扩充自免领域产品管线。
不仅如此,礼来的阿尔兹海默症药物Donanemab的3期临床取得积极结果,给人无限的想象和预期,如果获批,肯定会进一步推动的市值的上升。
01
度拉糖肽增速放缓
替尔泊肽潜力无限
有望冲刺40亿美元大关
度拉糖肽是由礼来研发的一款长效GLP-1类降糖药,GLP-1类药物因其出色的降糖作用,在糖尿病药物领域占比逐年增加。而度拉糖肽自2014年上市以后,市场份额迅速扩张,2019年,度拉糖肽以41.3亿美元销售额超过利拉鲁肽成为全球GLP-1类降糖药销售冠军,不过它遇到了强大的竞争对手司美格鲁肽,司美格鲁肽曾在头对头试验中打败了度拉糖肽(SUSTAIN 7试验)[1],并于去年销售额超过了度拉糖肽,未来度拉糖肽增速不容乐观。
不过好在礼来又于去年5月获批了首款GIP/GLP-1受体双重激动剂替尔泊肽,替尔泊肽上市不到半年,销售额已超2亿美元,今年上半年替尔泊肽销售额已达到15.48亿美元,放量速度惊人。
GLP-1类药物不仅有优异的降糖效果,也有显著的减重作用,目前在肥胖症适应症中,只有诺和诺德的利拉鲁肽减肥针Saxenda和司美格鲁肽减肥针Wegovy获批上市,减肥针Wegovy自获批以来销售额急剧上升,今年上半年销售额已达18亿美元,超过前两年销售额的总额,放量迅速,供不应求,更是曾被世界首富马斯克在推特上推荐,体现GLP-1类减肥药巨大的市场前景(图1)。
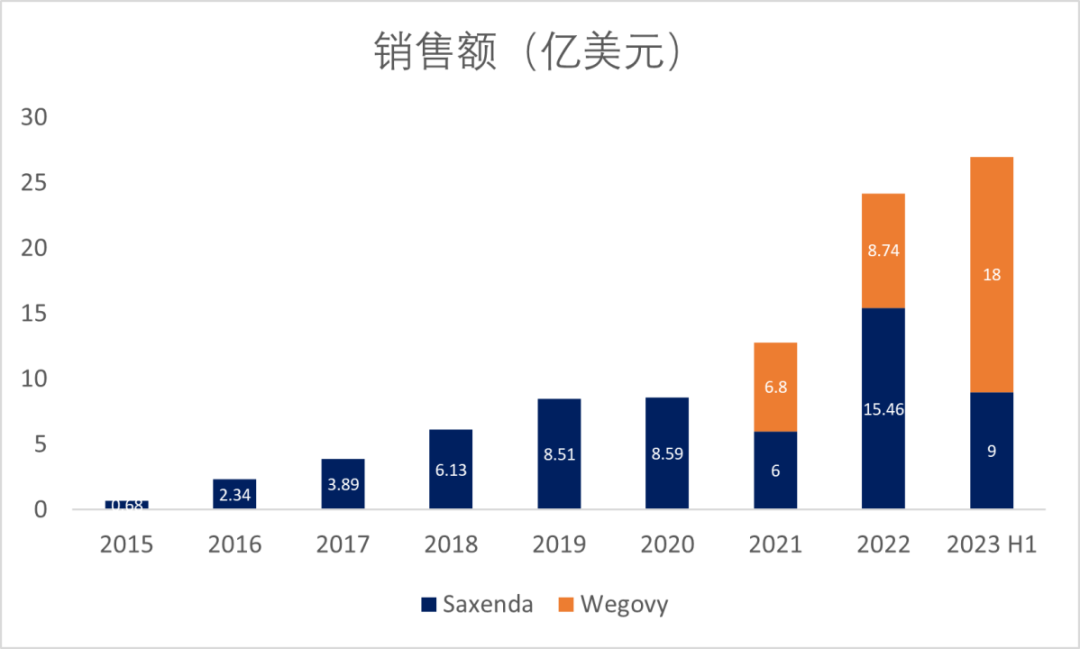
图1. 减肥针Saxenda和Wegovy的销售额(数据来源于诺和诺德财报)
替尔泊肽目前只获批了2型糖尿病适应症,正在积极开展肥胖症临床,希望早日获批肥胖症适应症。SURMOUNT系列 III 期临床是礼来开展的针对替尔泊肽长期体重管理的开发项目,已于 2019 年底开始,临床注册研究中招募了超过5000名肥胖或超重患者,包括SURMOUNT1-5,SURMOUNT-CN,SURMOUNT-J和SURMOUNT-MMO(图2)。
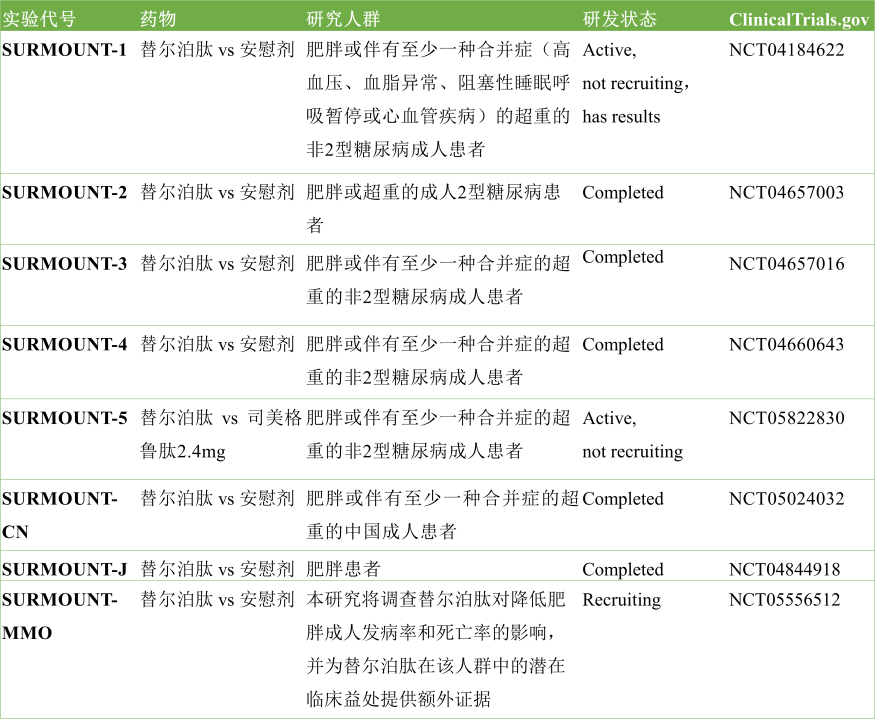
图2. SURMOUNT系列 III 期临床
SURMOUNT-1 主要研究结果及SURMOUNT-2研究结果已分别发表于《新英格兰医学杂志》[2]及《柳叶刀》[3], SURMOUNT-3 和 SURMOUNT -4 的研究结果预计于今年内公布。SURMOUNT-5是礼来开展的替尔泊肽对比司美格鲁肽2.4mg在成人肥胖或超重且伴有相关并发症患者中的有效性和安全性3b期临床试验,是首个3期替尔泊肽与司美格鲁肽头对头试验,预计于2024年12月完成。
SURMOUNT-1 已有的结果显示替尔泊肽优异的减重效果,最初的72 周试验已经完成,目前继续进行SURMOUNT-1额外104周的治疗,以评估使用替尔泊肽治疗3年后,对体重的影响及进展为2型糖尿病的潜在差异。
SURMOUNT-2的研究结果显示治疗72周后,安慰剂组、10mg剂量组和15mg剂量组受试者分别减重约3.18kg、13.5kg、15.6kg。基于此,礼来已在向FDA滚动提交替尔泊肽用于治疗肥胖或超重并伴有体重相关合并症的成人患者。
8月21日,国家药监局药品审评中心(CDE)官网显示,替尔泊肽注射液的减重适应症在国内申报上市并获受理,一旦获批替尔泊肽销售额会急剧上升。
除了度拉糖肽和替尔泊肽,在GLP-1类降糖减重药物领域,礼来还布局了GLP-1R/GCGR/GIPR三重激动剂Retatrutide和口服小分子GLP-1R激动剂Orforglipron,并且7月份以高达19.25亿美元收购Versanis Bio加码减重药物投资。
7月14日,礼来宣布与Versanis Bio达成一项协议,根据协议条款,礼来将支付高达19.25亿美元的现金,包括预付款和在实现某些开发和销售里程碑后的后续付款来收购Versanis Bio,加码其在肥胖症领域投入。随后8月14日,礼来宣布成功完成对Versanis Bio的收购。此次收购扩大了礼来的产品组合,包括Versanis的主要资产bimagrumab,目前正在一项2b期研究中进行评估,并与司美格鲁肽联合用于超重或肥胖的成年人[4]。
02
肿瘤领域阿贝西利遥遥领先
塞尔帕替尼和吡托布鲁替尼等后续发力
礼来在肿瘤领域主要有阿贝西利(Verzenio)、雷莫芦单抗(Cyramza)、塞尔帕替尼(Retevmo)和信迪利单抗(Sintilimab)等产品,其中阿贝西利上半年销售收入达到16.78亿美元,同比增长59%。
阿贝西利是一款CDK4/6抑制剂,目前全球有5款CDK4/6抑制剂获批上市,包括辉瑞的哌柏西利、礼来的阿贝西利、诺华的瑞博西尼、G1 Therapeutics/先声药业的曲拉西利以及恒瑞的达尔西利。
在这几款药物中,由于哌柏西利上市时间早,其销售额一直遥遥领先,然而近期因为专利以及其它CDK4/6抑制剂的竞争销售额有所下滑,阿贝西利近些年来由于出色的疗效和适应症的扩增销售额逐年上升,去年更是突破20亿美元大关,今年上半年销售额就已经达到16.78亿美元,放量迅速,有望冲刺40亿美元(图3)。
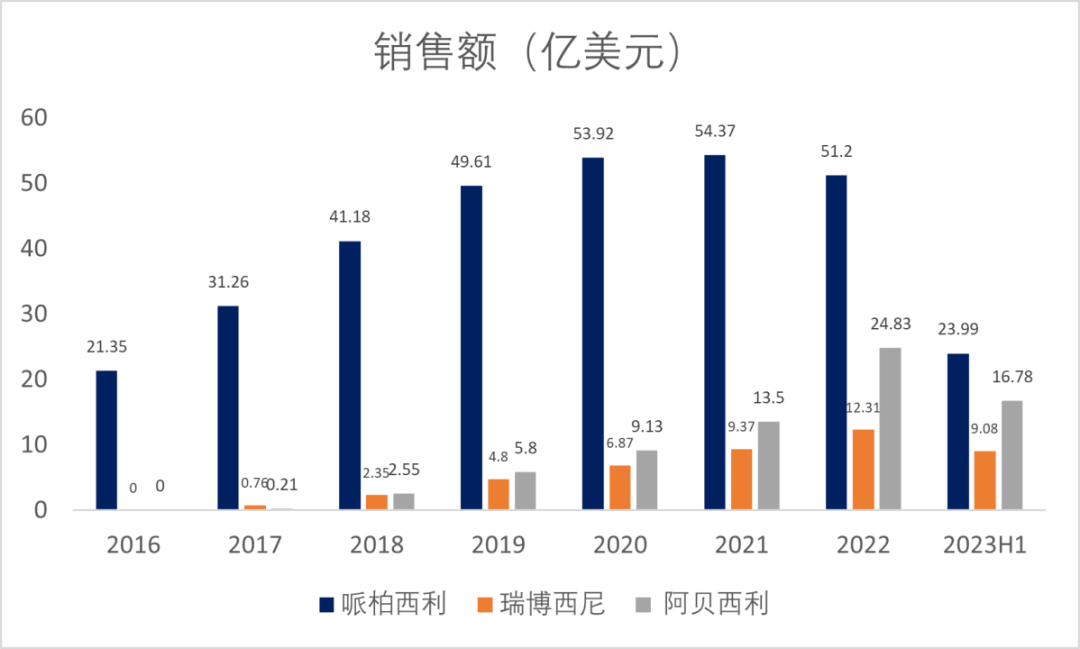
图3. CDK4/6抑制剂销售额
截止目前,阿贝西利是首个也是唯一一个获FDA批准用于乳腺癌辅助治疗的CDK4/6抑制剂,今年3月,FDA取消了对患者的Ki-67评分要求,进一步扩大了阿贝西利辅助治疗的范围,而且在临床上,阿贝西利对哌柏西利耐药后的患者仍能发挥疗效,克服哌柏西利耐药问题。
阿贝西利于2020年12月30日在国内获批上市,商品名唯择,成为国内首个且唯一获批用于早期乳腺癌高危患者的CDK4/6抑制剂,又于近期被NMPA批准扩展适应症,联合内分泌治疗用于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性、淋巴结阳性、高复发风险的早期乳腺癌成人患者的辅助治疗。
种种迹象都显示出阿贝西利巨大的市场前景,相信其销售额会继续高歌猛进。
除此之外,小分子肿瘤药物吡托布鲁替尼(pirtobrutinib)和塞尔帕替尼(Retevmo)也显示潜力,吡托布鲁替尼是首款获批上市的第三代非共价BTK抑制剂,BTK抑制剂在血液瘤治疗中取得巨大成功,其首款共价药物伊布替尼曾在2021年达到销售峰值97.8亿美元,然而伊布替尼治疗患者可能会对其耐药,吡托布鲁替尼在治疗经共价BTK抑制剂(cBTKi)预治疗的CLL/小淋巴细胞淋巴瘤(SLL),套细胞淋巴瘤(MCL),华氏巨球蛋白血症(WM)和边缘区淋巴瘤等患者时显示有效,有望解决cBTKi的耐药问题 [5]。
塞尔帕替尼(Retevmo)是礼来于2019年以80亿美元收购Loxo Oncology获得的一款强效、口服、高度选择性转染期间重排(RET)激酶抑制剂, 2022年9月,塞尔帕替尼获FDA加速批准新适应症,成为全球首个且唯一一个不限癌种用于治疗RET基因融合实体瘤的RET抑制剂。
今年8月22日,礼来宣布了LIBRETTO-531研究的主要结果,该研究评估了塞尔帕替尼与多激酶抑制剂(MKI)cabozantinib或vandetanib作为晚期或转移性RET突变甲状腺髓样癌(MTC)患者的初始治疗。该研究达到了其主要终点,表明无进展生存期(PFS)有统计学意义和临床意义的改善,这些临床试验的成功可能会进一步扩增塞尔帕替尼的市场空间[6]。
除了小分子肿瘤药物之外,礼来还有雷莫芦单抗(Cyramza)和信迪利单抗(Sintilimab)等多种单抗肿瘤药物,给其营收做出贡献,尤其是雷莫芦单抗,今年上半年贡献了4.97亿美元。
03
依奇珠单抗一马当先
礼来收购DICE扩展自免领域管线
自身免疫疾病是以局部或全身性异常炎症免疫反应为特征的炎症免疫性疾病,是仅次于肿瘤的研发热门领域。
礼来在自免领域也有诸多布局,靶点涉及IL-17、JAK和IL-23等。在自免领域中IL-17单抗依奇珠单抗(Ixekizumab,Taltz)销售额最高,今年上半年达到12.31亿美元,随后是口服JAK1/2抑制剂巴瑞替尼(Olumiant /Baricitinib),今年上半年销售额为4.48亿美元。除此之外,还有在日本上市的米吉珠单抗(Mirikizumab)以及正在被FDA审评的药物lebrikizumab等,涉及类风湿性关节炎、严重斑秃、中重度特应性皮炎、银屑病等自身免疫疾病。
依奇珠单抗是由礼来开发的一种靶向IL-17A的人源化`lgG4单克隆抗体,于2016年3月首次获得FDA批准,用于治疗强直性脊柱炎、中度至重度斑块状银屑病和活动性银屑病关节炎(PsA)等。目前全球范围内共上市5款靶向IL-17A/IL-17RA药物,分别是司库奇尤单抗(Cosentyx)、依奇珠单抗、尼塔奇单抗(Efleira)、比吉利珠单抗(Bimekizumab)和布罗利尤单抗(brodalumab)。在这几款药物中司库奇尤单抗和依奇珠单抗卖的最好。
今年6 月 20日,礼来以总计约 24 亿美元收购DICE Therapeutics,随后8月9日,礼来宣布成功完成对DICE Therapeutics的收购。此次收购扩大了礼来的免疫学产品组合,包括目前正在临床开发的口服IL-17抑制剂DC-806和DC-853,用于治疗免疫学中的慢性疾病[7]。
04
下一款重磅药物:Donanemab
支撑股价上升的一重要因素就是预期,俗话说买就买有未来的,礼来在研的阿尔茨海默症药物Donanemab给人无限想象。
随着全球老龄化加剧,阿尔茨海默症药物这一片蓝海令无数药企前仆后继,礼来在阿尔茨海默症十年如一日,经过无数的失败和努力,阿尔茨海默病(AD)是一种起病隐匿的进行性发展的神经退行性疾病,对大脑造成损害,占所有痴呆症病例的60 - 70%。先后终止了γ-分泌酶semagacestat、口服β分泌酶裂解酶(BACE)抑制剂lanabecestat和Aβ单抗solanezumab的开发。
功夫不负有心人,今年礼来终于看到了希望,在今年阿尔茨海默氏症协会国际会议(AAIC)上和JAMA杂志上,礼来发布了其研发的donanemab的3期TRAILBLAZER-ALZ 2研究取得积极结果,显示donanemab显着减缓了早期症状性阿尔茨海默病(AD)患者的认知和功能下降,为迫切需要新治疗方案的阿尔茨海默病患者带来了希望[8]。
研究结果显示Donanemab显着减缓淀粉样蛋白阳性早期症状性阿尔茨海默病患者的认知和功能下降,降低疾病进展的风险;在Donanemab治疗的疾病早期阶段,近一半的受试者在1年时没有临床进展;其他亚群分析表明,那些处于疾病早期阶段的研究参与者具有更大的益处,与安慰剂相比,下降速度减缓了60%,已向FDA提交上市申请,预计年底前将采取监管行动,如果获得批准,相信donanemab可以为患有这种疾病的人提供具有临床意义的益处,并且一旦淀粉样蛋白斑块被清除,最早可以在6个月内完成他们的治疗过程。
在1736名随机参与者中,1320(76%)人完成了试验。在低/中tau人群中donanemab组在76周时iADRS评分的最小二乘均值(LSM)变化为-6.02,安慰剂组为-9.27和在合并人群中donanemab和安慰剂组分别为-10.2和的-13.1。在低/中tau人群中,76周时donanemab组CDR-SB评分的LSM变化为1.20,安慰剂组为1.88,在合并人群中donanemab组为1.72,安慰剂组为2.42(图4)[9]。
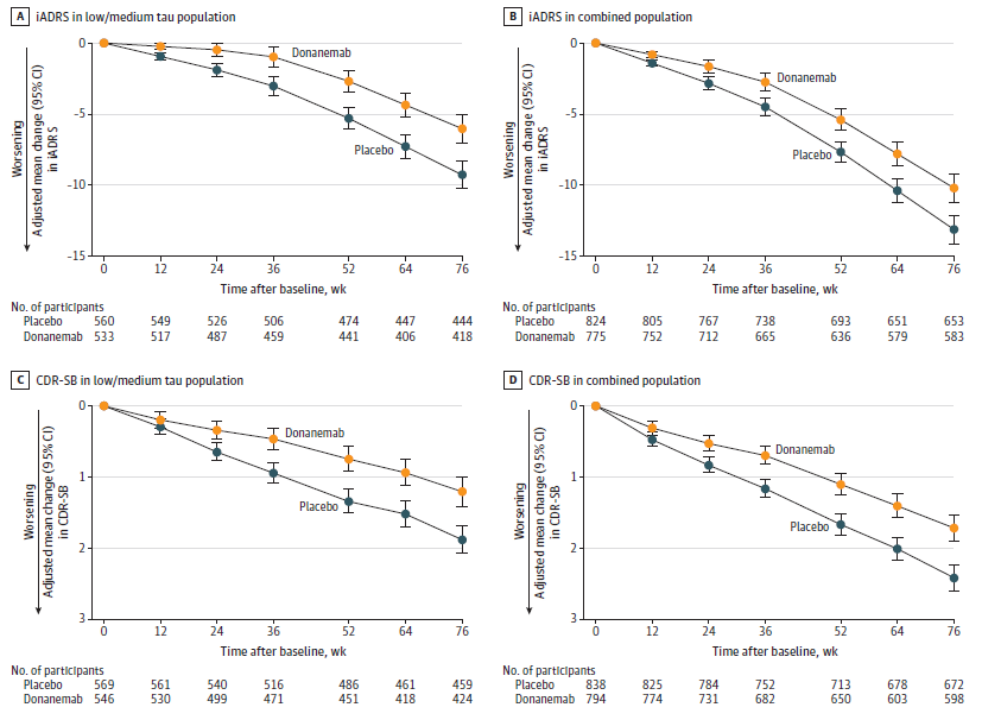
图4. 综合阿尔茨海默病评定量表 (iADRS) 和临床痴呆评定量表 (CDR-SB)的总和
小结
礼来以糖尿病药物发家,然而2022年,它的两款胰岛素产品赖脯胰岛素Humalog(优泌乐)和人胰岛素Humulin(优泌林)销售额分别下降16%和17%,降至20.61亿美元和10.19亿美元。不过其GLP-1王牌产品度拉糖肽销售额依然坚挺,2022年销售额同比增长15%至73.4亿美元,但是还是被诺和诺德的司美格鲁肽反超了。
好在礼来还有GLP-1/GIP双重激动剂替尔泊肽可以补上,替尔泊肽现有的临床试验显示其优异的降糖减重效果,自去年上市以来,销售额也呈现放量增长,分析师给予其超过的预期,未来有可能成为突破200亿美元销售额的重磅药物。
除了糖尿病和肥胖领域,礼来在肿瘤、自免领域以及神经领域持续发力,多款药物显示优异的临床意义,未来更是有无限可能,进一步推动礼来市值的上升,使其冲向万亿市值。
References
1.Richard E Pratley et.al, Semaglutide versus dulaglutide once weekly in patients with type 2 diabetes (SUSTAIN 7): a randomised, open-label, phase 3b trial, Lancet Diabetes Endocrinol. 2018 Apr;6(4):275-286.
2.Jastreboff AM, Aronne LJ, Ahmad NN, et al. Tirzepatide Once Weekly for the Treatment of Obesity. N Engl J Med 2022; 387(3): 205-16.
3.Garvey WT, Frias JP, Jastreboff AM, et al. Tirzepatide once weekly for the treatment of obesity in people with type 2 diabetes (SURMOUNT-2): a double-blind, randomised, multicentre, placebo-controlled, phase 3 trial. Lancet 2023
4.https://investor.lilly.com/news-releases/news-release-details/lilly-completes-acquisition-versanis-bio
5.Philip A. Thompson and Constantine S. Tam, Pirtobrutinib: a new hope for patients with BTK inhibitor–refractory lymphoproliferative disorders, Blood (2023) 141 (26): 3137–3142.
6.https://investor.lilly.com/news-releases/news-release-details/lillys-retevmor-selpercatinib-demonstrates-superior-progression
7.https://investor.lilly.com/news-releases/news-release-details/lilly-completes-acquisition-dice-therapeutics
8.http://lilly.mediaroom.com/2023-07-17-Results-from-Lillys-Landmark-Phase-3-Trial-of-Donanemab-Presented-at-Alzheimers-Association-Conference-and-Published-in-JAMA
9.John R. Sims, MD; Jennifer A. Zimmer, MD et.al, Donanemab in Early Symptomatic Alzheimer Disease, The TRAILBLAZER-ALZ 2 Randomized Clinical Trial, JAMA. 2023;330(6):512-527.
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..