西格列汀是默沙东公司开发的全球第一款获得批准上市二肽基肽酶-4(DPP-4)抑制剂降糖药物。磷酸西格列汀片于2006年10月首次在美国获批上市后,默沙东还开发有磷酸西格列汀多种复方产品上市,如不同组成比例的复方西格列汀二甲双胍片。
其中原研西格列汀二甲双胍片(Ⅱ)[规格为:磷酸西格列汀50mg/盐酸二甲双胍850mg]和西格列汀二甲双胍片(I)[规格为:磷酸西格列汀50mg/盐酸二甲双胍500mg]已进口中国。
默沙东在中国上市药品专利信息登记平台除登记有西格列汀化合物专利200480017544.3(专利保护期届满日到2024年6月18日)外,还登记有一件关键的制剂专利200680047103.7,专利保护期届满日到2026年12月12日。
该件制剂专利也成为了国内复方西格列汀二甲双胍片仿制药开发规避的主要目标,意味着仿制药如果能够绕开原研制剂专利将会提前2.5年上市销售。
针对默沙东公司和齐鲁制药就西格列汀二甲双胍片仿制药相关技术方案是否落入专利号200680047103.7保护范围一案,国家知识产权局于2022年9月7日做出(2022)国知药裁0001号行政裁决,北京知识产权法院于2022年11月21日做出(2022)京73民初409号判决,均确认齐鲁制药申请注册的药品相关技术方案未落入专利权保护范围。
之后,默沙东在过去的几个月内撤回了针对200680047103.7做出4.2类专利声明宁波美诺华天康药业、浙江九洲生物医药、宁波美诺华天康药业、吉林惠升生物制药、济南辰欣医药、浙江恒研医药6家企业仿制西格列汀二甲双胍片的药品专利纠纷行政裁决请求,并已结案。
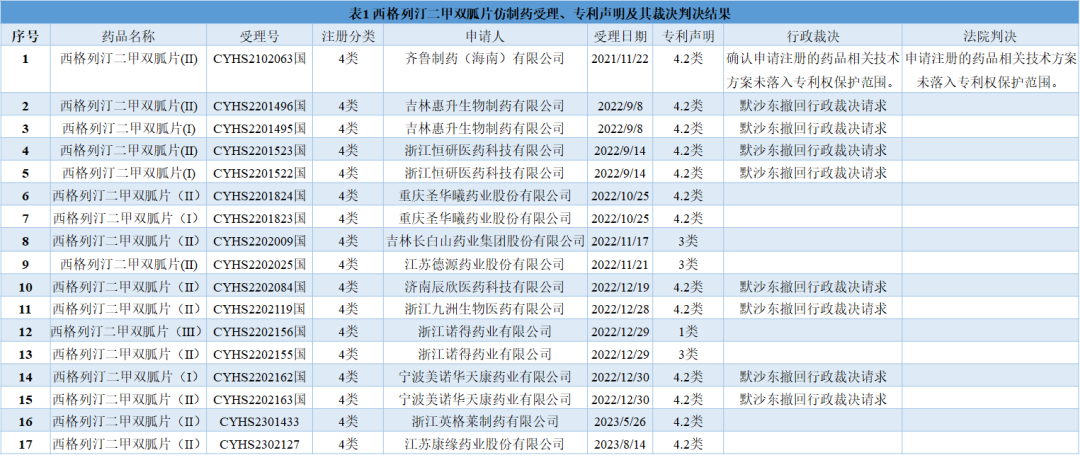
此外,还有3家企业虽然仿制药受理时做出了4.2类声明,但目前尚未公布药品专利纠纷行政裁决结果。
值得一提的是,也有3家企业在仿制药受理时针对200680047103.7做出了3类声明,也就意味着在相应专利权有效期届满之前(即2026年12月12日)所申请的仿制药暂不上市,将会比做出4.2类声明且行政裁决“确认申请注册的药品相关技术方案未落入专利权保护范围”的产品晚上市2.5年。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..