6月27日,再生元宣布收到FDA就阿柏西普8mg制剂的上市申请发出的完整回复函(CRL)。FDA在CRL中表示,此次拒绝批准是因为第三方填料商的问题,与疗效、安全性、试验设计、说明书和原料药生产等方面无关。

再生元表示,接下来会与FDA和第三方填料商密切联系,以确保阿柏西普8mg制剂尽快上市。再生元未透露该第三方填料商的具体信息。
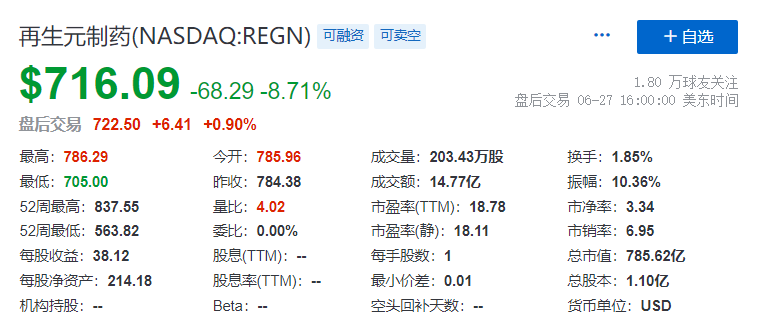
受此消息影响,再生元股价下跌8.7%。
阿柏西普是拜耳和再生元联合开发的一款VEGFR-Fc融合蛋白,于2011年11月首次在美国获批上市,商品名为Eylea(阿柏西普2mg)。再生元拥有阿柏西普在美国的专有权,拜耳则拥有美国以外的独家营销权。Eylea的注射频率为每两个月1次,阿柏西普8mg制剂是再生元和拜耳为延长给药间隔推出的长效制剂,其注射频率可降低至每四个月1次。
根据再生元财报,Eylea在2022年的销售额达到96.47亿美元,同比增长4%,其中美国地区收入62.65亿美元,美国以外市场收入33.83亿美元(拜耳负责,再生元分得13亿美元)。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..