近日,据Fierce Biotech等多家行业媒体报道,欧洲药品管理局(EMA)已接受CRISPR Therapeutics和Vertex两家公司递交的CRISPR基因编辑疗法exagamglogene autotemcel(exa-cel)的上市申请,该疗法拟用于治疗镰刀状细胞贫血病(SCD)和输血依赖性β地中海贫血(TDT)患者。这也意味着,exa-cel有望于今年获得批准,成为全球首个上市的CRISPR-Cas9基因编辑治疗药物。
SCD是一种遗传性血红蛋白病,因β链第6位氨基酸谷氨酸被缬氨酸代替,形成镰状血红蛋白,取代了正常血红蛋白。SCD临床表现为慢性溶血性贫血、易感染和再发性疼痛危象引起慢性局部缺血从而导致器官组织损害,主要通过输血、药物治疗等方法进行治疗。β-地中海贫血是一种由于β珠蛋白肽链合成减少或缺乏而引起遗传性溶血性疾病,相当一部分患者需要定期输血才能存活,从而导致输血依赖性地中海贫血(TDT)。目前,造血干细胞移植是唯一可根治的治疗手段,但存在配型概率低、年龄限制等问题。
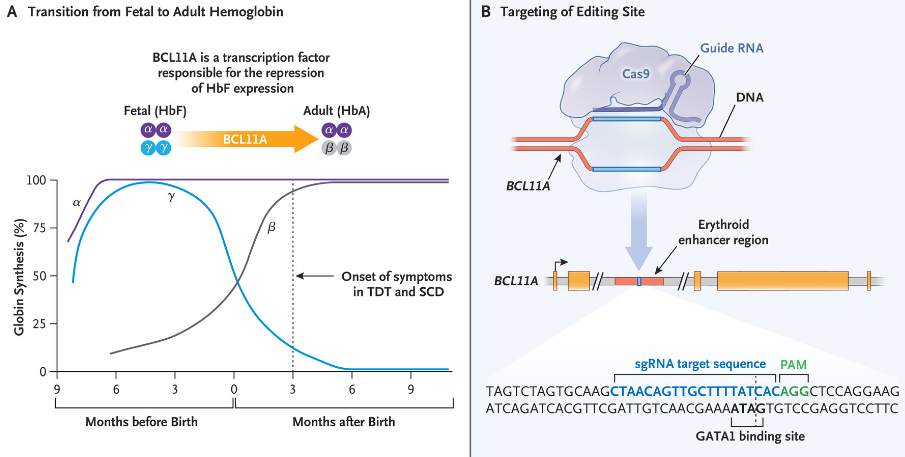
exa-cel是一款自体、体外CRISPR/Cas9基因编辑疗法,通过在体外对患者的造血干细胞进行改造,使其红细胞中产生高水平的胎儿血红蛋白(HbF,是一种可以携带氧气的血红蛋白,在出生时自然存在,随着婴儿的长大逐渐转换为成人形式的血红蛋白)。exa-cel可以提高HbF水平,帮助缓解TDT患者的输血需求,并减少SCD患者的疼痛和血管闭塞性危象(VOC)。
此前公布的临床试验结果显示 exa-cel具有一次治疗、功能性治愈的潜力。CLIMB-111、CLIMB-121和CLIMB-131研究的数据显示,在接受exa-cel治疗的44名TDT患者中,42名患者在随访时间为1.2-37.2个月时不再需要接受输血,剩余2名患者接受的输血水平分别降低75%和89%。同时,TDT患者的胎儿血红蛋白显著提高,总血红蛋白水平提高。平均总血红蛋白水平在接受治疗第三个月超过11g/dL并且得到维持。在31名接受exa-cel治疗的严重SCD患者中,所有患者在随访时间为2.0-32.3个月时,均未出现血管闭塞性危象,且患者的平均胎儿血红蛋白水平在接受治疗后第四个月时占总血红蛋白水平的40%,并且得到维持。
目前exa-cel已经获得美国FDA授予的再生医学高级疗法(RMAT)、快速通道、孤儿药和儿科罕见病的称号认证,以及欧盟委员会的孤儿药认证、EMA的优先药物(PRIME)指定。此外,除了在欧盟进入监管审评流程之外,Vertex和CRISPR Therapeutics也已经在美国启动监管申请的滚动递交,预计在今年第一季度完成滚动递交。
文 | 医谷
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..