9月16日,蓝鸟生物bluebird bio公司宣布,美国FDA加速批准其基因疗法Skysona(elivaldogene autotemcel,eli-cel)上市,用于减缓4-17岁早期活动性脑肾上腺脑白质营养不良(CALD)男孩神经功能障碍的进展。Skysona是首款FDA批准用于治疗早期脑性肾上腺脑白质营养不良的基因疗法。该疗法的定价让人震撼,在美国的定价为300万美元。

在8月17日,宣布美国FDA批准蓝鸟生物(Bluebird Bio)的首款基因疗法产品Zynteglo用于治疗β-地中海贫血患者,定价为280万美元,夺得当时最贵天价药的称号,谁料短短1个月,最贵药物的纪录就被自家另一个药物打破了。
Skysona用于治疗罕见病
肾上腺脑白质营养不良(ALD)是一种罕见的X染色体连锁代谢疾病,95%病患是男性,全球估计每21000名男性新生儿中就有1名被诊断为ALD。这种疾病是由于ABCD1基因突变引起的,这种突变影响了ALD蛋白的产生,随后导致极长链脂肪酸(VLCFAs)的毒性积累,主要发生在肾上腺,和大脑与脊髓的白质中。大约40%的ALD男童患者会发展为CALD,这是ALD中最严重的一种。CALD是一种罕见的神经退行性疾病,症状通常发生于儿童时期(中位年龄为7岁),可迅速导致进行性、不可逆的神经功能丧失和死亡,主要症状包括沟通丧失、尿失禁、无法行动等症状。
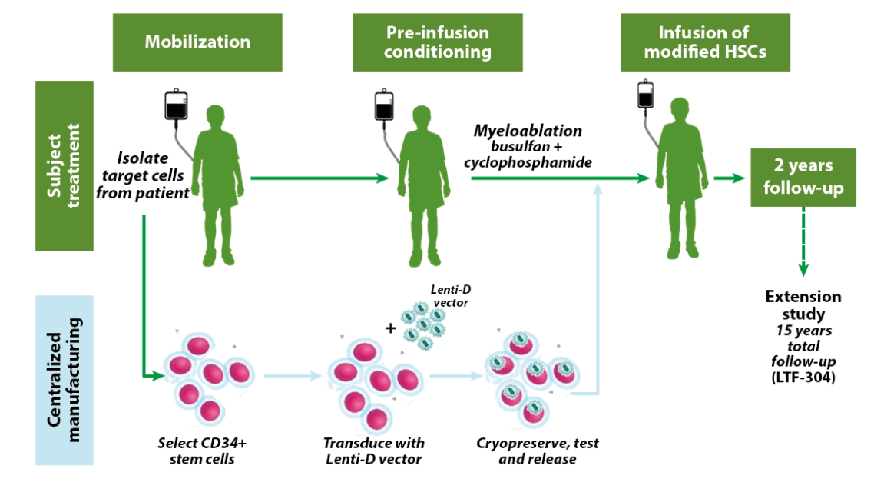
此前,CALD患者唯一可用的治疗选择是接受同种异体造血干细胞移植,然而据估计,超过80%的CALD患者的兄弟姐妹中没有匹配的供体。Skysona是一款一次性造血干细胞慢病毒体外疗法基因疗法,通过Lenti-D慢病毒载体 (LVV) 进行离体转导,将ABCD1基因的功能性拷贝添加到患者自身的造血干细胞 (HSC) 中。患者就能够产生ALD蛋白 (ALDP),该蛋白有助于分解超长链脂肪酸 (VLCFA)。
该疗法的治疗目标是阻止CALD的进展,并尽可能保留神经功能,包括保留患者的运动功能和沟通能力。此前获得FDA授予的突破性疗法认定、孤儿药资格、和优先审评资格。Skysona可以一次性从根本上缓解病情,但FDA给予了该疗法黑框警告。使用该疗法有导致罹患血液肿瘤的风险。
此次批准基于II/III期Starbeam临床研究(ALD-102)(N = 32)的功效和安全性数据支持,此外,BLA还包含III期临床试验ALD-104中35名受试者的数据。在ALD-102中,90%(29/32)的患者在24个月时达到主要评估终点,即无严重功能障碍(Major Functional Disabilities-free)的状态下生存。
根据相关数据,美国每年约有40~50名患者被诊断出患有CALD,蓝鸟生物预计每年约10名患者会使用Skysona进行治疗。
基因疗法加速上市
基因疗法无疑是近年生物技术治疗领域的新话题,蓝鸟生物前几年凭借领先的基因疗法而红极一时,2018年,蓝鸟生物股价一度超200美元/股,但2019年、2020年和2021年,该公司净亏损分别达到7.9亿美元、6.2亿美元和8.2亿美元,2022年6月的蓝鸟生物股价已经跌到了3美元,到了破产的边缘。如今Skysona和Zynteglo已经上市,股价几乎翻了一倍,之后能否凭此重振其业务?
从7月到9月,已有四款基因疗法获欧盟和FDA批准上市,除了Bluebird Bio的体外基因疗法Skysona和Zynteglo(用于治疗β地中海贫血),还有BioMarin Pharmaceuticalde的AAV基因疗法ROCTAVIAN(用于治疗血友病A)和PTC Therapeutics的AAV基因疗法Upstaza(用于治疗上芳香族L-氨基酸脱羧酶缺乏症)。越来越多的新疗法为罕见病病人带来新的治疗希望。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..