今天我们来看看美国 FDA 2021 仿制药论坛上有关生物药剂学风险评价、综合生产评价(integrated manufacturing assessment)、无菌保证以及仿制药上市后药物警戒方面的讨论。
药品质量办公室(OPQ)生物药剂学处代理生物药剂学主管 Min Li 讨论了生物药剂学风险评价用于指导固体口服制剂的溶出方法开发。报告介绍了对生物药剂学风险评价目的的理解,并讨论了如何进行评价,其重点是理解体外溶出度测试对 BA/BE 风险降低的作用。
OPQ 药品生产评价办公室的 Vidya Pai 介绍了对综合生产评价的监管期望。报告还讨论了需要关注对于来自生产审评团队的缺陷和问题的回应。报告的主要目的是让企业知道他们需要了解审评团队问的问题并提供相关、完整、简洁和准确的答复来解决 FDA 提出的问题。她在报告中举了一些缺陷例子和在回复时的考虑要点,通过这些例子可以更好地了解 FDA 在提出缺陷时背后的监管期望是什么。她重点指出:
普遍的缺陷是可解决的,需要适当注意细节并包含由科学和基于风险的分析支持的信息和论证。
存在澄清和与 FDA 讨论的途径(例如,针对复杂 ANDA 审评问题的中期电话会)。
提交的文件应表明对产品、工艺和实施风险有透彻的了解,从而可以进行可靠的产品质量管理。
OPQ 药品生产评价办公室微生物评价处处长 Marla Stevens-Riley 在构建更好的无菌保证申请中着重介绍了 OGD 在无菌保证申报资料中发现的一些常见问题。明确和简洁是关键,同时要确保无菌保证申报或 DMF 的不同部分之间没有差异。常见问题包括:
冲突信息 — 例如,在不同模块提到不同的设备或者叙述不一致
缺乏理论依据或合理性 — 例如,验证应支持商业生产
不包含有关接收到的无菌或去热原的物品信息
在高压釜中未发现灭菌过滤器
未描述生物负荷监测
生物负荷监测位置不充分 — 例如,应在任何过滤之前进行监测
没有压力和真空条件被用于容器密封系统完整性测试
对于生物指示剂来说不可接受的培养条件
培养基灌装不能代表最大生产状态
不正确地使用合并内毒素检测
用于产品放行的不正确内毒素限度
仿制药的上市后安全性和药物警戒通常来说并不重要,因为仿制药的概况与品牌药非常相似,但是如临床安全监督主管 Howard Chazin 所介绍,首仿药在质量属性方面可能会有差异,尤其是对于药械组合产品来说。过去有关质量问题的一些经验包括:
药片破裂
刻痕药品切分不均匀或碎裂
药片粘喉
异常气味、味道或质地
口服液和注射剂中有沉淀
贴剂不粘肤
容器/密封问题
滴眼液安全密封条脱落
大尺寸药片/胶囊
缓释产品无法维持一整天
注射器故障/断针
在新仿制药进入市场后,主动药物警戒可以检测是否存在问题。Chazin 提供了一些例子来说明主动药物警戒可以在哪些方面提前通知是没有潜在质量安全问题还是有重大问题。在干粉吸入器方面存在细微差别的 Advair 和仿制 Wixela Inhub 在初步监测后未显示质量或安全性问题。而用于多发性硬化症的 Copaxone 自动注射器与仿制产品之间允许的差异则导致,相对于品牌产品,仿制产品的自动注射器针头弯曲或折断的问题更常见。此问题正在调查中。
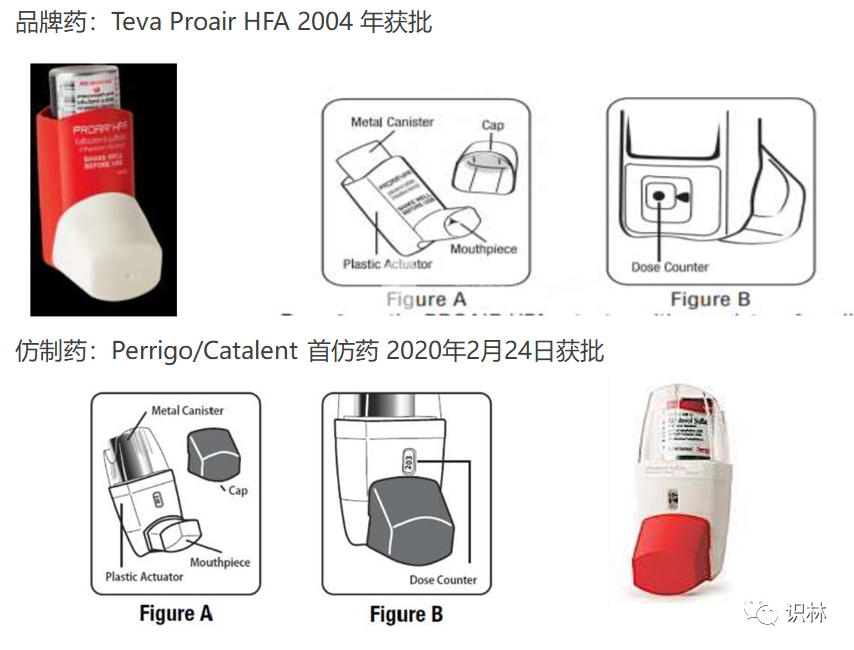
Proair HFA 沙丁胺醇吸入器是 Teva 的品牌产品,Perrigo/Catalent 的仿制产品在 2020 年 2 月 24 日获批,仿制产品与品牌产品之间存在允许的差异。【FDA 批准首个仿制硫酸沙丁胺醇吸入剂,国会关注复杂仿制药批准 2020/02/26】批准后仿制产品出现非预期安全性信号,开始有吸入器堵塞的报告。2020 年 8 月 , 仿制药商和分销商停止生产和分销,并发起自愿召回 , 现在正在调查堵塞问题。
Chazin 强调:
仿制药与品牌药一样安全有效
在极少数情况下允许的差异可能会导致非预期或意向外的质量或安全性问题
复杂仿制药械组合产品由于药物递送、器械组成部分的差异以及可能需要立即采取行动的意向外质量问题而引发独特的潜在安全问题
与增加仿制药市场份额有关的提前考虑有助于帮助重点关注仿制药的药物警戒工作
跨 CDER 的内部对话可帮助员工参与、支持研究并促进公众沟通
与仿制药利益相关者的联络是完善 OGD 正在进行的安全性监督流程和程序的关键
随着审评流程的不断变化,从 FDA 这些研讨会中获得信息将提供宝贵的学习经验。识林已收录“2021 仿制药论坛 — 仿制药的生命周期”全部视频和幻灯片。2021 仿制药论坛相关往期资讯:
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..