无菌药品因其给药途径的特殊性,相对于其他药品对其无菌性有着特殊而严格的要求。无菌药品的生产必须严格按照精心设计并经验证的方法和规程进行,产品的无菌或其他质量特性绝不能只依赖于任何形式的最终处理或产品检验(包括无菌检查)。如何保证无菌工艺科学实现需要从产品无菌工艺、灌装设备、人员操作、环境监测等进 行设计与管理,特别是无菌灌装室如何通过HAVC系统与洁净室设计,来确保无菌工艺产品生产环境有效实现,是无菌设施设计、验证与运行重要工作。
看似简单的要求,但在无菌灌装室设计、验证与运行工作,常常出现以下问题:在无菌工艺灌装室设计、验证与使用时,都往往仅关注A级的粒子指标和微生物指标,忽视了无菌工艺暴露保护与A级区的本质;在无菌工艺设计时,过多的依赖设备的物理隔离装置,忽视了生产人员操作大量带来直接或间接污染的风险。
这些问题都反映出当前部分从事生产工艺与洁净室工程技术人员,没有准确、科学与系统地理解无菌工艺药品污染风险的途径,同时对不同生产区域(或房间),所设置的不同HVAC系统的作用机理了解不足。
污染风险途径与污染预防手段
在药品制造过程中,常见的污染主要有非活性污染、活性、内毒素污染。其中活性污染为微生物污染,通常通过人员、外部空气、设备、工具、器具、模具、物料等外部环境带入洁净生产区域。药品制造过程中,无论无菌制剂还是非无菌制剂,都需要对产品、与产品接触对容器、设备工艺表面、最终处理完毕的内包装材料和包装容器等需要进行保护,避免受到外部污染,导致产品发生污染质量风险。药品制造对微生物污染一般可采用去除污染物来源、封闭技术、设计和执行有效的清洁和灭菌程序、人员培训与更衣、生产环境消毒和洁净区HVAC送风等手段或方法。
这些污染源对药品产生污染途径分为直接污染与间接污染两种方式,两种不同的污染途径的污染源,其污染负荷水平、污染范围、污染危害不尽相同,其污染来源与污染预防手段分析见表1所示。
特别是直接污染危害最为严重,通常需要采用灭菌工艺对物料、物品带来的污染源进行去除,对于操作人员采用穿戴无菌工艺手套、隔离装置等手段,彻底消除直接污染风险。对于间接污染,通常是生产人员身体所带的微生物污染通过空气传播,导致暴露区域的无菌工艺表面、产品遭到污染。
在实际无菌灌装过程中,常常需要生产操作人员进行无菌工艺部件装配、灌装计量调整、无菌胶塞添加、理瓶台倒瓶处理等生产操作时,由于人是最大污染源,时刻散发着大量微粒同时也携带有微生物,同时但是设备物体的表面都会积攒有微粒,当有紊流产生或人员动作时,设备物体的表面的微粒是可能带入到洁净气流中,从而影响到产品。如何消除与避免间接污染,也是无菌工艺生产需要解决的重要问题。
表1 药品制造过程污染途径与污染预防手段

气流保护原理
洁净室与洁净HVAC系统,通过高效过滤器,有效的去除外部空气污染物的同时,也HVAC系统送回风口的设置方式不同,实现“稀释”或“置换”二种不同工作原理。“稀释”机理是通过乱流方式,产生紊流,用新鲜对洁净室内对空气进行稀释,保持对外部正压空气屏障形成,保持温度与湿度的控制,同时实现压差梯度的实现,也通过回风或除尘系统,进行排风,实现整体工艺环境的保持与控制。“置换”机理是通过“单向气流”方式,采用置换方法,将洁净室或局部的空气进行挤压排出,实现局部工艺保护。二种不同HVAC机理与洁净空气控制目标分析见表2。
表2 净化HVAC机理与环境空气条件


单向流洁净室的原理,就是单向流洁净HVAC系统依靠送风气流“活塞”般的挤压作用,迅速把室内污染排出。单向流洁净HVAC系统不仅要求高度洁净的空气,而且要求能控制气流的方向,使气流从洁净度高的区域流向洁净度低的区域,并带走和排出气流中尘埃颗粒和微生物。
无菌生产工艺需要保护暴露的物料或产品、与产品接触的工艺表面表面、经灭菌工艺处理的内包装材料进行直接污染控制的同时,也需要对人员通过空气间接污染途径产生的污染需要消除。消除人员间接污染,可以利用HVAC系统产生的洁净空气单向流原理,可以通过洁净的单向送风,将工艺过程产生的颗粒污染进行去除,如设备、包装材料摩擦、操作人员洁净服等产生的粒子。同时也通过单向气流,形成“气流屏障”,将操作人员身体可能存在的微生物污染通过空气飘逸到无菌工艺暴露保护操作区内,确保无菌工艺生产过程污染的风险控制,气流屏障原理与工艺操作保护如图1所示。
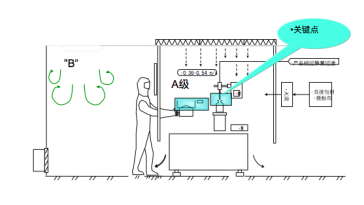
图1 气流屏障原理与工艺操作保护
无菌工艺操作区域单向气流技术要求与影响因素
《药品生产质量管理规范(2010年修订)》附录1《无菌药品》第九条也将无菌药品生产所需的洁净区可分为4个洁净级别:A级为高风险操作区,如灌装区、放置胶塞桶和与无菌制剂直接接触的敞口包装容器的区域及无菌装配或连接操作的区域,应当用单向流操作台(罩)维持该区的环境状态。单向流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s(指导值)。应当有数据证明单向流的状态并经过验证。
通过对不同过无菌制剂药品生产管理规范与技术要求,不难发现,对于无菌工艺暴露与人员无菌操作区域,需要达到以下技术要求:
流型:流线平行度,保证尘源散发的尘粒不作垂直与流向的传播,关键区域不得有涡流
速度均匀性:线之间质点横向交换最小,出风口风速为0.45±20% m/s。
最低送风速度:能控制污染范围,抑制污染气流上升,快速自净,一般最低不低于0.36 m/s。
气流遇到阻碍,或者当有高温、压差波动、或者气流速度过快等破坏气流分层因素存在,就会产生紊流或湍流。通常会以下情况可能会有紊流产生:
当单向流流向设备操作面时,特别是遇到凹形或异形设备会改变气流运行方向的物体时;
冻干机、灭菌柜、灌装管路等设备灭菌,无菌工艺表面大量产热时;
设备保护罩开启或关闭时;
单向流风速改变或风速均匀度改变时;
人员肢体或物体介入单向流及进行操作或运动时。
气流流向与烟雾测试
因此关键区域的气流流型是一个关键的技术要求。由于气流本身无法直接肉眼观测,因此常用通过加入其他低速可视物质,如烟或雾,令其与气流一起运动,以观测气流的形态,确认单向流在静态(非生产状态)和动态(设备和人员正常运行条件下)都能够进行持续保护,这个通常称为可视化气流流型试验,因通常采用烟雾进行,也通常称为烟雾试验。
烟雾试验是一个简单地、直观可视、便捷多能的检测方法和工具,可用于洁净区不同区域和位点研究单向流情况、观察不同操作对单向流的影响,从而在洁净室与HVAC系统评价、无菌工艺设备设计、无菌操作及程序、环境监测点设置、无菌工艺操作培训与评价、变更偏差调查都可以发挥作用。
小结
无菌工艺生产过程中,防止无菌工艺微生物污染重要手段:直接污染消除与气流保护。有效的实施气流保护,可以最大程度的消除生产人员操作时对无菌暴露工艺区的间接污染,同时也是去除无菌暴露保护区的粒子污染。但气流保护的实现,需要根据无菌工艺操作行为进行分析,结合房间的设备与物品布置,结合房间的空间大小,合理设置层流净化系统,如层流面积、回风口位置;并同时需要通过烟雾试验证明其静态与动态下气流保护实现程度,并以此为相关人员操作与环境监控程序提供依据。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..