▎药明康德内容团队编辑
今日,美国FDA官网信息显示,拜耳(Bayer)与默沙东(MSD)联合开发的鸟苷酸环化酶(sGC)激动剂Verquvo(vericiguat)的新药申请(NDA)已经获得批准,治疗经历心力衰竭恶化事件后射血分数低于45%的症状性慢性心力衰竭患者。这是美国FDA在2021年批准的首款创新药,也是首个治疗慢性心力衰竭恶化患者的可溶性鸟苷酸环化酶(sGC)激动剂。

▲Verquvo(vericiguat)药物标签截图(图片来源:FDA官网)
射血分数降低(HFrEF)型心力衰竭,以前称为收缩性心力衰竭,其特征在于心脏在其收缩阶段充分射血的能力受到损害。HFrEF占心力衰竭患者的40-50%。每年,约有30%的症状性慢性心力衰竭患者会经历疾病的恶化,估计慢性HFrEF恶化的患者中有五分之一将在两年内死亡。
Verquvo是默沙东和拜耳联合开发的一种每日口服一次的直接水溶性鸟苷酸环化酶(sGC)激动剂。sGC对血管和心脏的功能都很重要,然而,在心力衰竭患者体内sGC不能被充分激活,从而导致心肌和血管功能异常。Verquvo通过激活sGC,恢复了关键信号途径(NO-sGC-cGMP)的功能。2014年5月,拜耳与默沙东达成研发协议,共同开发和推广Verquvo。
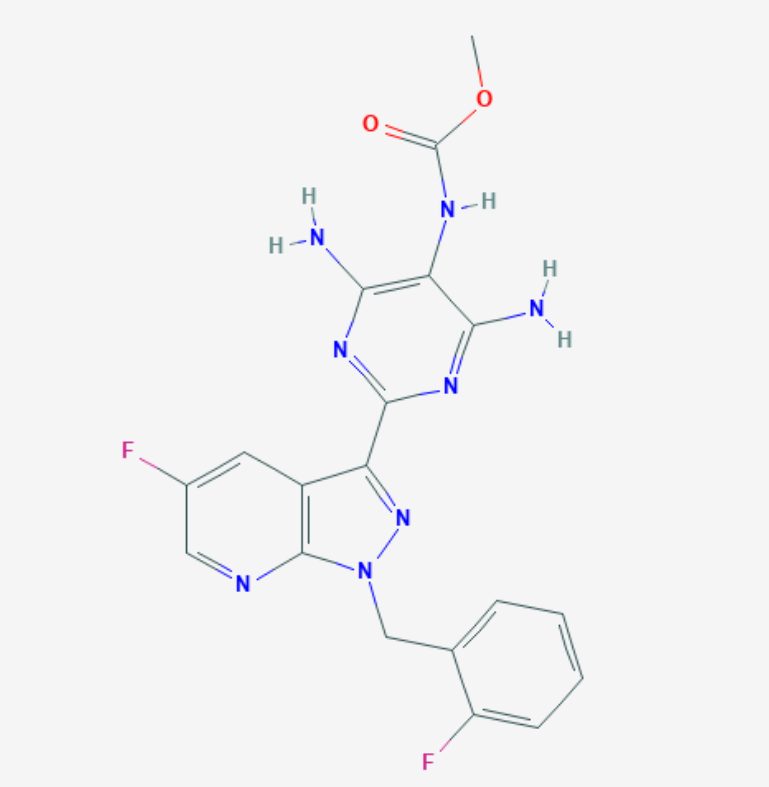
▲Verquvo分子结构式(图片来源:PubChem)
这一批准得到了名为VICTORIA的3期临床试验结果的支持。该试验专门针对慢性心力衰竭加重,心血管病死亡风险高且反复心衰住院的人群。来自VICTORIA的数据已在《新英格兰医学杂志》上发表。中位随访期为10.8个月时的结果显示,Verquvo治疗组较安慰剂组降低了患者因为心衰住院和心血管原因死亡的复合终点风险(35.5% vs 38.5%,HR=0.90,P=0.02)。
最近一年来阿斯利康(AstraZeneca)公司开发的达格列净获批成为首款治疗射血分数降低型心衰患者的SGLT2抑制剂,诺华的诺欣妥(Entresto)也获得美国FDA心血管和肾脏药物咨询委员会(CRDAC)的支持,有望在今年第一季度获批治疗射血分数保留性心力衰竭(HFpEF)患者。我们期待更多新药好药早日获批,为心衰患者造福。
注:本文旨在介绍医药健康研究,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
参考资料:
[1] 各家公司官网。
[2] Gilead and Vir Biotechnology Establish Clinical Collaboration to Explore Combination Strategies for Functional Cure for Chronic Hepatitis B Virus. Retrieved January 12, 2021, from http://investors.gilead.com/news-releases/news-release-details/gilead-and-vir-biotechnology-establish-clinical-collaboration
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..