上周,佰傲谷对新冠疫苗的研发进行了全面盘点(点击查看,关于新冠疫苗,我们应该期待什么?)并从我国的角度阐述了对于疫苗的一点看法。

巧合的是,12月17日NEJM的主编团队(Eric Rubin主编,Lindsey Baden副主编,Stephen Morrissey执行主编)在一次音频采访中围绕新冠疫苗和药物进行了讨论(DOI: 10.1056/NEJMe2035370)。
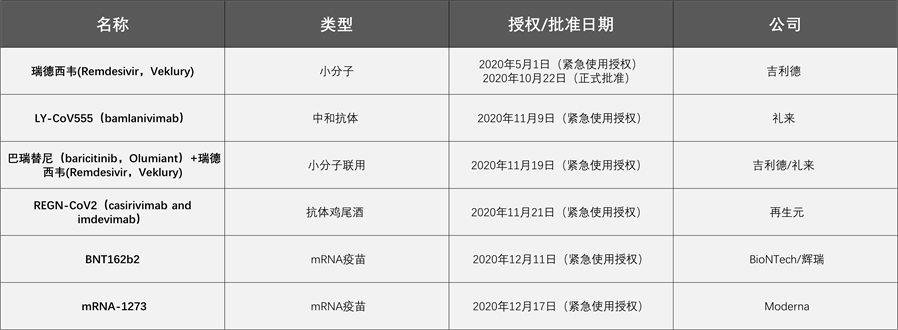
那么,让我们看看来自权威学术期刊的专业编辑们是怎么看待这些疫苗和药物的吧。
观点总结:
对疫苗
1. 目前,已经有减毒活疫苗,传统疫苗(灭活疫苗与亚单位疫苗),活载体疫苗,DNA疫苗,mRNA疫苗五类取得了较好的临床进展。
2. 受制于非特异免疫,对新冠有潜在作用的减毒活疫苗——卡介苗,可能并没有很好的效果。
3. mRNA疫苗表现良好,但在生产与分发体系建立上还不够成熟。
4. 新冠病毒突刺蛋白是公认较好的靶标。
5. 对目前所有进入晚期临床的疫苗效果都保持乐观,未来将有许多选择。
对药物
1. 巴瑞替尼+瑞德西韦的临床研究数据不具有压倒性。
2. 依然推荐地塞米松治疗重症COVID-19患者。
3. 新冠药物临床面临着研究背景(例如护理手段)快速变化的影响,导致跨时间数据集的收集成为制约和难点。
4. 如何对患者进行更详细的分类,判断患者处于疾病的哪个阶段,从而以制定更合理的用药计划,成为目前的主要挑战。
新冠疫苗
近来,已经2款新冠疫苗获得了美国EUA授权。那么,围绕疫苗的研发进展和供应等热点问题编辑们是怎么看的呢?
Eric:目前已经有几款疫苗处于临床后期研究阶段,并且有些获得了EUA授权或与之类似的授权,且正在被更广泛的使用。为了更好的理解这些疫苗,我们需要简单回顾一下疫苗背后的技术路线。这有助于我们了解这些疫苗,虽然同一路线下的不同疫苗有时候也是完全不同的。
总的来说,目前疫苗研发共有5个种类,其中4类已经获得了处于后期阶段的候选疫苗。
第一类是减毒活疫苗,不过这一路径唯一进入三期临床的候选疫苗甚至都不是COVID-19疫苗,而是肺结核卡介苗(有研究显示卡介苗可以显著降低SARS-CoV-2的感染率)。该方案试图通过增加非特异性免疫来防止各类感染。不过由于不会增加特异性防护能力,这类疫苗应该无法产生较高的保护水平。所以虽然这种方法在我们获得专门的COVID-19疫苗前具有一定吸引力,但我认为随着更多疫苗出现,人们很快就会对这类疫苗失去兴趣。
第二类是非常传统的疫苗,通过全病原体灭活,重组蛋白或其他亚单位,并与佐剂共同使用来预防疾病。这类疫苗已经有多个候选,并且有的已经开始分发使用。尽管这类疫苗正在三期临床,但由于没有结果目前依然很难了解其有效性和安全性。这类传统疫苗的早期数据显示了良好的免疫反应。尽管大规模生产和工艺再现方面可能存在挑战,从而导致不同批次间的差异问题,但这类传统疫苗也有十分丰富的生产经验。
第三类是活载体疫苗,有着更多的候选产品。所有处于后期临床的活载体疫苗全部使用的是腺病毒载体,一种被认为无法使人致病的病毒。不过,也有其他进展不够迅速但是采用了其他载体的活载体疫苗。无论采用哪种病毒载体,这类疫苗都重组了新冠病毒突刺蛋白基因。新冠病毒突刺蛋白是除了全病原体灭活疫苗外,其他类型疫苗所普遍采用并且已经被证实有效的靶点。
同样,与灭活病毒疫苗类似,活载体疫苗也在三期临床结果发出前开始分发使用。不过这类疫苗中的一款已经得出了三期结果(牛津/阿斯利康的AZD1222)。一项规模相对较大的临床结果在数周前发表于The Lancet(DOI:https://doi.org/10.1016/S0140-6736(20)32661-1)上。从该试验看来,疫苗似乎是安全有效的,但到底多有效依然不清楚。这款疫苗在试验执行过程中出现了一些问题,导致对总体结果的分析有些困难。其有效性为70%,看起来不如mRNA疫苗。值得注意的是,该疫苗是目前唯一一款采用单剂方案进行大规模临床试验的疫苗,而不是其他疫苗普遍选用的两剂方案。
第四类是DNA疫苗,目前只有一款候选(Inovio的INO-4800)进展较快,不过该疫苗的三期临床正遭到FDA暂停。
第五类是mRNA疫苗,美国两款(Moderna的mRNA-1273;BioNTehc/辉瑞的BNT162b2),中国至少一款。目前,两款美国的mRNA候选疫苗在临床受试群体中展现了很高的疗效且相对安全,但是都遇到了生产和分发问题。不过作为最早一批mRNA疫苗,目前的生产与分发都还没有形成一套大规模的高效体系。不过随着时间推移,情况将会越来越好。美国两款mRNA疫苗都需要低温冷藏,其中一种还需要超低温。这使得分发成分更加昂贵,对物流等后勤工作提出了挑战,特别是很多地方并没有足够且良好的冷柜。
Lindsey:我更关注的是疫苗所针对靶标。我们必须首先明白到底是病原体的哪一部分可以引发人体的免疫反应,从而达到预防效果。正如Eric所说,新冠病毒突刺蛋白已经被证实是一个理想靶点,这是因为自然感染个体产生免疫反应,病毒结构生物学研究结果和历史经验告诉我们部分针对病毒外壳的中和抗体往往可以有效预防疾病。我认为这十分关键,并且两个mRNA疫苗的研究都证明了激发对突刺蛋白的免疫反应会对健康产生正面影响。
第二个关注点是递送系统,这涉及到我们如何让突刺蛋白以一种理想的方式进入免疫系统,从而引起相关免疫反应,无论是更强的抗体反应,还是更强的CD4+,CD8+ T细胞混合反应。我们知道与病原体接触的组织,比如鼻黏膜会出现免疫反应,产生抗体,这都是不同递送系统可以利用的特性。另外,学术界和医疗界通常不考虑递送系统在医药工业端的特性。生产这些递送系统需要什么?通过高质量生产工艺,能够多快将这种产品规模化到临床应用级别?是否能满足更多需求?
第三我们必须思考,在大流行面前,我们在制定应对措施方面学到了什么?我们如何平衡速度与科学的关系,以及如何向研究人员,企业,群众等传达这种新的应对模式。这对我们解决此次大流行和应对下次都十分重要。
Eric:我想补充的是现在有许多疫苗平台和很多不同的疫苗技术,但实际上都使用了类似的概念,即指示免疫系统对病毒突刺蛋白做出反应。现在概念已经得到验证是可行的,并且我们知道的许多疫苗技术,也许是所有处于晚期阶段的疫苗都确实能引起良好的免疫反应。因此我非常乐观的认为我们将会有很多选择。当然,细节很重要,由于这些疫苗所引发的不良反应都是不同的,而且整体疗效可能也有变化。我的猜测是,这些疫苗中的大多数都是有效的,这非常重要。
Lindsey:我谨慎乐观认为你是正确的。我认为对这种病原体进行免疫预防足以预防一些更严重的疾病。所以我也很乐观,即使事与愿违,所有这些工作都会在某种程度上发挥作用。此外,你说的也十分重要,疫苗原理是什么,分发是否容易,副作用有哪些?总的来说这些都是我们在大规模接种计划前应该考虑的因素。我们越快的进行某种免疫保护,就越有希望减缓疾病传播。
治疗药物
2020年12月11日,NEJM发表了巴瑞替尼+瑞德西韦治疗由COVID-19导致住院成人患者的临床结果(DOI:10.1056/NEJMoa2031994)。由此,编辑们首先围绕巴瑞替尼进行了讨论。
巴瑞替尼是一款已获批用于治疗类风湿关节炎的JAK抑制剂。JAK是促炎症级联反应中的一个关键信号转导分子,通过阻断该靶点,就可以影响并阻止下游信号转导,防止炎症反应。
此次研究发现,巴瑞替尼+瑞德西韦可缩短COVID-19住院患者的恢复时间,改善临床状态,特别是在高流量氧气或无创通气治疗患者中疗效更佳。
Eric :使用巴瑞替尼原因与其他药物类似,例如地塞米松(被证明可以少中重度COVID-19患者死亡率[DOI: 10.1056/NEJMoa2021436])与托珠单抗(未能在临床中提高患者患者生存率[DOI: 10.1056/NEJMoa2030340])。与以上两种药物类似,巴瑞替尼有希望在疾病的炎症阶段发挥最大作用——即病毒复制已经减少时,病毒本身已不是病理反应的主要驱动因素,而是某种不适当的炎症级联反应。不过,临床使用上,目前我们面临的主要困难是如何确定患者是否已经进入不适当炎症级联反应这一阶段。
回到巴瑞替尼,与其他研究不同,此次临床采取了巴瑞替尼+瑞德西韦的联合疗法。好处是,原则上联合用药可以对处于不同感染阶段的患者都发挥作用。
此次研究是一项大规模多中心临床,登记标准相当宽松,几乎所有中度或以上肺炎住院患者都符合要求,除了患者不能使用类固醇治疗COVID-19外。
研究中,患者首先使用瑞德西韦,之后随机分配到巴瑞替尼与安慰剂进行对照研究。本次研究共入组了超过1000名受试者,其中2/3为中度,其余为重度(10%需要呼吸支持)。结果显示,使用巴瑞替尼后,患者的平均恢复时间小幅减少为7天,而相应对照组为8天。
值得注意的是,次要终点方面巴瑞替尼组28天死亡率为5.1%,对照组为7.8%(死亡风险比0.65),一定程度上降低了患者的死亡风险,但由于该结果置信区间相当宽泛(95% CI, 0.39 to 1.09),我们很难推断如果在一项专门关注死亡率的研究中,该结论是否还能成立。本次研究中没有发现特别的安全信号,但长期使用巴瑞替尼有感染风险,不过在此次短时间的研究中并不是问题。
此次研究在地塞米松治疗新冠(RECOVERY临床)的临床结果发布前就启动了,但两项研究很难比较。唯一值得参考的是地塞米松减少死亡率的人群与使用巴瑞替尼获益的人群类似,但我们依然不知道这些药物在其中扮演了什么角色,也不知道随着时间推移,其他辅助支持疗法(护理方法等)在不同的研究地点存在哪些变化。
我应该会继续推荐使用地塞米松救治病情较重的患者,不仅因为更加便宜,而且因为其临床证据更有力。至于巴瑞替尼则可能更适合用于一个细分类型的患者,例如对皮质类固醇不耐受的患者。
Lindsey:此次临床研究(指巴瑞替尼+瑞德西韦)的难度非常大,原因是研究不仅涉及对疾病发病机制的深入理解,还有对试验设计所蕴含复杂因素的评估权衡。例如,本次试验框架中包含了针对直接抗病毒反应药物(瑞德西韦)和免疫调节剂(巴瑞替尼)两种不同机制药物的研究,并且患者的病理情况可能发生在感染的不同时期,这让弄清楚如何使用或联用这些不同药物变得十分复杂。
我也认为本次研究的数据不具有压倒性。研究终点的选择从其本身看来是有意义的,但不如死亡率改善有说服力。此外,本次研究已经告诉人们,这一途径与疾病发病机制相关,但结果是否足够清晰以至于可以支持临床使用还尚不清楚。
Eric:事实上,已经有多个类似的药物临床研究展现出一定收益,但是我们依然很难从这些数据中对个别患者如何用药进行判断。而这很大程度上不仅因为Lindsey所提到的生物学问题,还包括这些临床都是在不同的时间开始,且临床启动时对疾病的了解程度也不一致。我们也很想对其中一些疗法进行比较,但我们并不知道哪一种疗法会在特定的时间发挥作用。
Lindsey:Eric强调了一个长期过程。即便听起来好像只差几个月,但2020年12月的患者治疗与护理和2020年5月也有着很大的不同。事实上,就算患者在同一医院,同一重症监护病房,接受同一个医疗团队的救治,几个月来其所受到的护理方法也有了很大变化。因此,除非临床研究开始前就考虑到了这一因素,或者收集了同一时期的对照数据,否者很难推测这类跨时间的数据集。
“转自:佰傲谷BioValley”。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..