日前,Blueprint Medicines在2020年欧洲过敏与临床免疫学会(EAACI)会议上,公布了该公司精准蛋白激酶抑制剂avapritinib,在治疗惰性系统性肥大细胞增多症(SM)患时的最新结果。试验结果表明, avapritinib能够显著改善SM患者的皮肤症状。
SM是一种由KIT D816V突变驱动的罕见疾病,特征是肥大细胞失控增殖和活化。该疾病可导致虚弱的全身、胃肠道和神经认知症状,包括危及生命的过敏反应。常见皮肤症状为瘙痒、潮红和色素性皮肤病变,可显著影响生活质量。目前,尚没有获批针对KIT D816V突变的靶向疗法。
AYVAKIT(avapritinib)是一种激酶抑制剂,它已经获得FDA批准治疗胃肠道间质瘤(GIST)成人患者,他们携带 PDGFRA 外显子18突变,包括PDGFRA D842V突变。Avapritinib同时对KIT D816V具有强力的特异性抑制效应。 基石药业已经获得avapritinib在大中华区临床开发和推广的权益 。
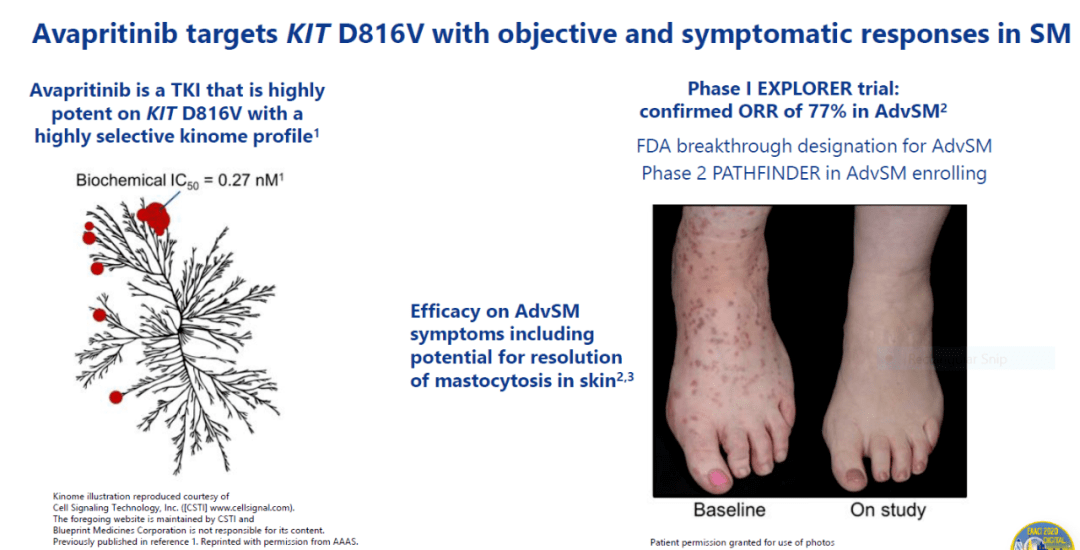
图片来源:参考资料[2]
PIONEER是一项随机双盲、含安慰剂对照、允许注册性研究的2期临床试验,评估avapritinib在惰性SM患者中的疗效。该试验包括三个部分:第一部分为剂量探索部分,第二部分为注册性研究,第三部分为长期治疗研究。此次公布的是第一部分的研究结果。
试验结果表明 ,在接受治疗24周后,avapritinib治疗组患者达到60%的缓解率(缓解的定义为全面症状评分降低超过30%),而对照组的缓解率为0%。此外,多种其它对症状的检测方式也一致地检测到avapritinib的疗效。
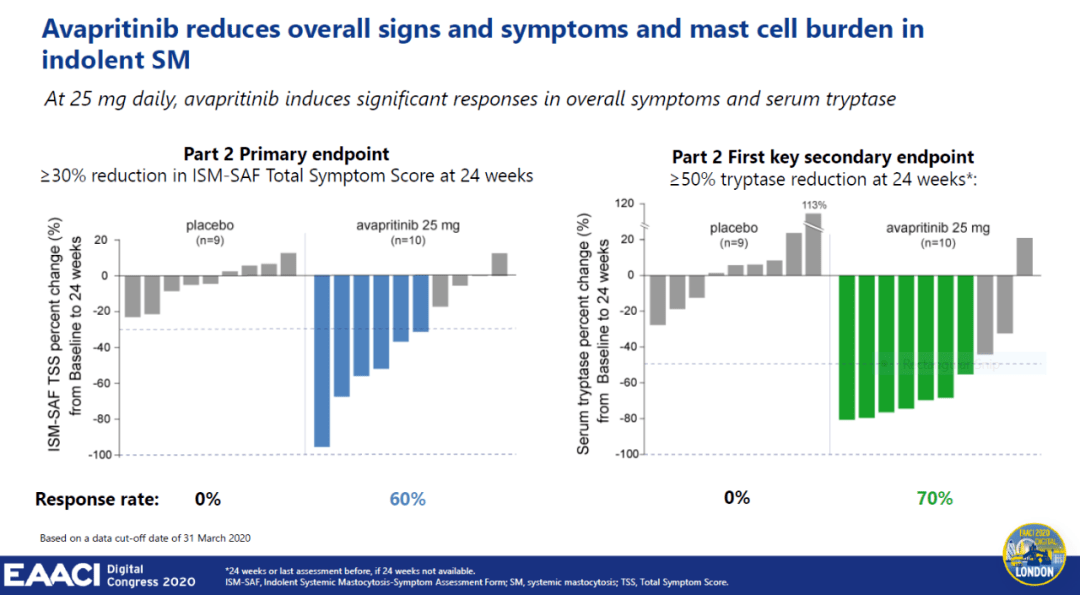
图片来源:参考资料[2]
基于这些数据和美国FDA的反馈,Blueprint Mdeicines已经选择24周时的缓解率作为支持注册的PIONEER临床试验的主要终点。第二部分计划注册约200名患者,初步患者筛选将在今年6月开始。
“我们致力于迅速推进avapritinib的开发,以满足惰性系统性肥大细胞增多症患者未竟需求,目前他们缺乏具有针对性的治疗,”Blueprint Medicines首席医学官Andy Boral博士说:“Avapritinib可以强效靶向系统性肥大细胞增多症的根本驱动因素,它有可能从根本上改变这种疾病的治疗方式。”
[1] Blueprint Medicines Presents Updated Part 1 Data from PIONEER Trial of Avapritinib Showing Robust Reductions in Cutaneous Disease Symptoms in Patients with Indolent Systemic Mastocytosis. Retrieved June 6, 2020, from https://www.blueprintmedicines.com/wp-content/uploads/2020/06/Blueprint-Medicines-EAACI-Data-Press-Release-June-6-2020.pdf
[2] Avapritinib reduces cutaneous symptoms and mast cell burden in patients with indolent systemic mastocytosis in the PIONEER study. Retrieved June 6, 2020, from https://www.blueprintmedicines.com/wp-content/uploads/2020/06/Blueprint-Medicines-EAACI-2020-Avapritinib-Reduces-Cutaneous-Symptoms-Mast-Cell-Burden-Indolent-SM-Presentation.pdf
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..