患者权益组织癌症研究之友(the Friends of Cancer Research)与IQVIA公司和其它的医疗保健研究组织合作开展研究,确定在什么情况和什么时候可以信任真实世界数据(RWD)。
近日,患者权益组织癌症研究之友(Friends of Cancer Research)公开发表该组织与其它机构合作开展的真实世界证据(RWE)试点计划初步研究结果。相关论文在线发表于美国临床肿瘤协会(American Society of Clinical Oncology,ASCO)创办的《临床肿瘤学杂志·临床肿瘤信息学 》(JCO Clinical Cancer Informatics)上。这项研究计划,旨在评估对使用免疫疗法治疗的晚期非小细胞肺癌患者,使用RWD估算真实世界终点的能力。

论文第一作者,是癌症研究之友组织负责科技政策的副总裁Mark Stewart博士。其他论文作者,包括IQVIA公司负责真实世界解决方案的高级副总裁Nancy Dreyer博士,论文投稿时尚在Flatiron公司的Amy Abernethy博士,以及FDA CDER肿瘤卓越中心副主任Sean Khozin博士等。
相关研究的数据源
这项前期研究,检查了从不同的数据来源采集RWD的运作能力,探索从不同医疗保健数据组织的数据来源抽提真实时间终点的潜在运用,同时评价了RWE终点的实际运用情况。
来自于6个不同的数据源提供方的研究者,遵循相同的方案,采用医保报销(administrative claims)和电子病历数据,评价真实世界终点。这些真实世界终点,包括在真实世界情况下,使用PD-1/PD-L1抑制剂治疗的晚期非小细胞肺癌晚期患者的总生存期(real world overall survival,rwOS)、距离下次治疗时间、距离停药时间(time to treatment discontinuation,rwTTD)、进展时间、以及无进展生存期。这些不同的数据集,源自2011年1月至2017年10月间接受治疗的269名至6,924名非小细胞肺癌患者。所涉患者均做匿名处理。
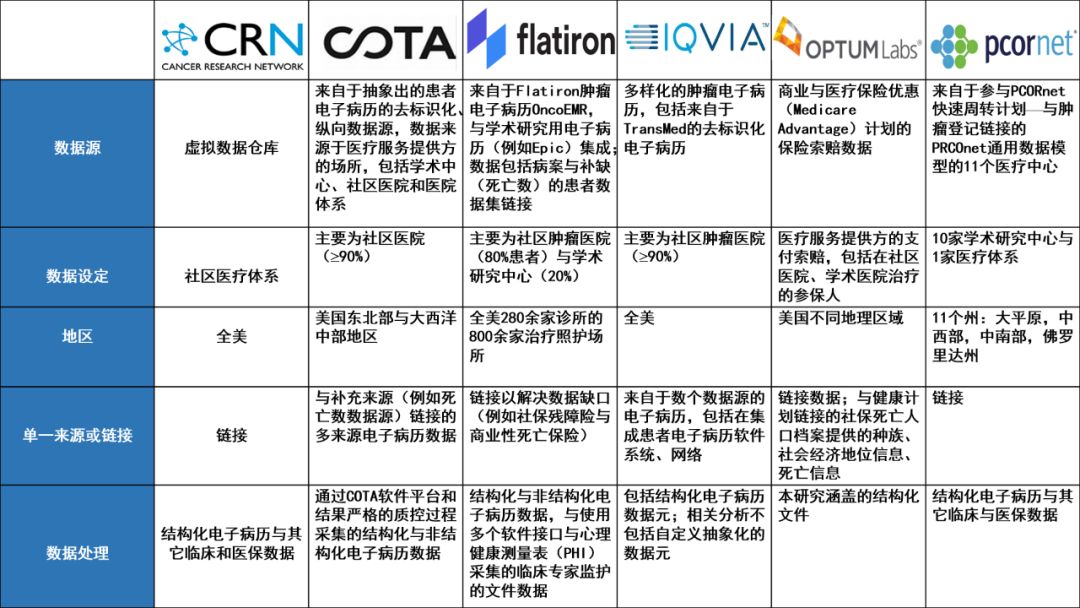
▲试点研究数据来源(图片来源:参考资料[1])
相关研究结果
真实世界的中间终点(rwTTD和距离下次治疗时间)与rwOS之间的相关性为中度到高(范围为0.6到0.9)。在所有的真实世界终点中,rwTTD最为一致;启动PD-L1治疗后1年的rwOS范围为40%至57%。此外,通过电子病历与保险索赔数据评价rwOS,结果落入相关临床试验中观察到的OS中位值范围内。研究广泛采用具有持续数据监护(ongoing data curation)的数据源,确保在相关研究开始之前,就具备必要的准确性和可用性。
结果显示,这些真实世界终点“在总体上保持相互一致,并与随机临床试验中观察到的结果一致,证实了RWE用于支持监管与支付方决策的潜在有效性。所观察到的差异,似乎反映了采用真实世界方法与采用临床研究方法的实际差异。”
图片来源:Pixabay
RWE:用在哪?如何用?
依据《21世纪医疗法案》规定, FDA需要了解在什么情况下和什么时候可以信任RWD。FDA还需要确定何时开展一项或多项传统的随机试验。
参加这项研究的Dreyer博士表示,“了解证明RWE有效性的重要性,尤其是在存在大量未竟需求和复杂疗法的肿瘤领域,是验证运用RWE作为创新药品批准和推进个体化医疗的有效手段。”
该试点项目的目的,是汇集来自于不同组织的电子病历、癌症登记和医保报销来源的RWD,评估采用 RWD解决临床相关问题的可行性和使用,例如,确定未竟需求,把握新疗法的临床试验结果,适应症扩展,不良事件和用药注意事项等。试点项目成功地将经验丰富的数据提供方聚集在一起,通过通用的架构,评估是否可以从接受 PD-1/PD-L1治疗的 NSCLC 患者的RWD中总结出可以采用的终点。初步研究结果证明了从不同数据集中抽取一些真实世界终点的能力,接下来的研究,将进一步刻画这些终点的作用。接下来的2.0版试点项目,将要弄清在什么情况下,以及如何使用RWE评价非小细胞肺癌的治疗有效性。

▲参加下一步研究的组织、机构(图片来源:药明康德内容团队整理)
展望下一步工作
IQVIA公司的Dreyer博士表示,“作为这项工作附带产生的结果,正在了解RWE与理想化情况下的传统临床试验的证据有何不同。RWE是随机临床试验的补充,由于参与临床试验的患者的治疗方式,与常规治疗不同,因此结果也可能不同。”
IQVIA公司先进证据生成中心副总裁Jennifer Christian博士表示,下一步的工作,将涉及到刻画数据源及其所覆盖人群的差异性。将使用随机化临床试验作为比较基准开展敏感性分析,必要时扩展至其它治疗域和国家,评估相关框架。作为相关计划的一部分,还将与癌症研究之友和英国的Health Data Insight组织合作,使用英国公共卫生系统癌症登记和分析服务,比较来自美国以外的数据。Christian博士认为,尽管预期会有所差异,这些差异是否是数据记录工作附带产生的结果,还是获益和风险方面的差异所致?明晰这些差异的具体来源,将是有用的。
免责声明:本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。
[1] Mark Stewart, Andrew D. Norden, Nancy Dreyer, et al. An Exploratory Analysis of Real-World End Points for Assessing Outcomes Among Immunotherapy-Treated Patients With Advanced Non–Small-Cell Lung Cancer. Aug 15, 2019. Retrieved Sept 28, 2019 from https://ascopubs.org/doi/full/10.1200/CCI.18.00155
[2] IQVIA Collaborates with Cancer Researchers to Advance Use of Real World Evidence. Sept 18, 2019. Retrieved Sept 28, 2019 from https://www.iqvia.com/newsroom/2019/09/iqvia-collaborates-with-cancer-researchers-to-advance-use-of-real-world-evidence
[3] Melissa Fassbender. Pilot project to answer where and how RWE can be used. Sept 27, 2019. Retrieved Sept 28, 2019 from https://www.outsourcing-pharma.com/Article/2019/09/27/Pilot-project-to-answer-where-and-how-RWE-can-be-used
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..