3 月 24 日,药物临床试验登记与信息公示平台官网显示,甘李药业登记了一项在不使用气道正压通气治疗的肥胖的中度至重度阻塞性睡眠呼吸暂停受试者中评价 GZR18(博凡格鲁肽)注射液疗效与安全性的多中心、随机、双盲、平行、安慰剂对照的 Ⅲ 期临床研究(登记号:CTR20261125)。
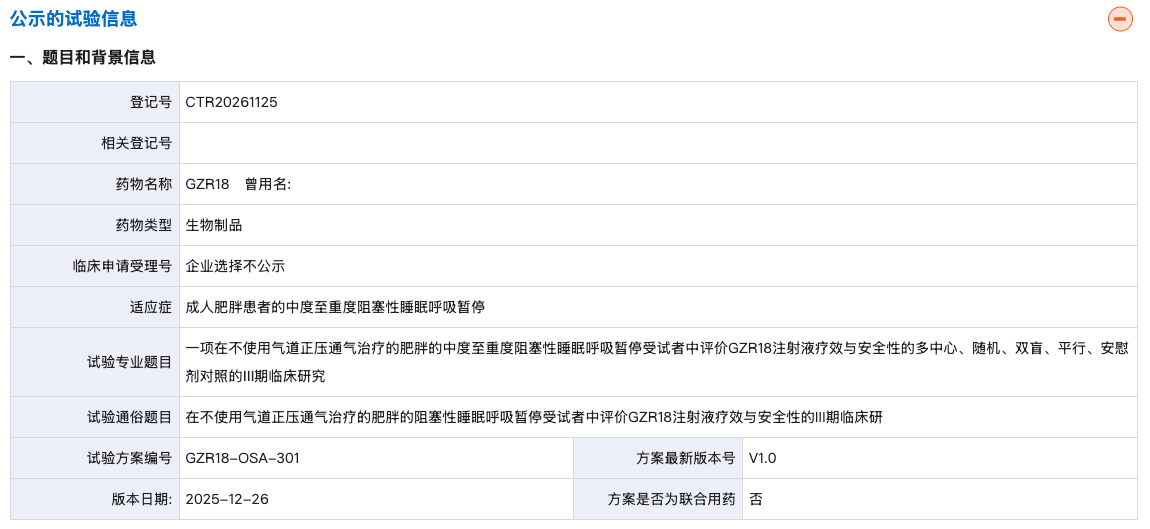
来源:药物临床试验登记与信息公示平台官网
该研究计划在国内入组 140 名受试者,主要终点是治疗 52 周后,呼吸暂停低通气指数(AHI)相对基线的变化。次要终点包括 AHI 相对基线变化的百分比、AHI 较基线下降 ≥ 50% 的受试者比例、体重相对基线变化的百分比等。
博凡格鲁肽是甘李药业自主研发的 GLP-1RA 双周制剂,目前已经开展了 6 项 III 期临床,除此次登记的外,其他研究如下图所示。
作为潜在全球首个 GLP-1RA 双周制剂,博凡格鲁肽已经达成了 2 项出海授权合作,分别将拉丁美洲地区、印度地区的开发和商业化权益授权给了 Laboratorios Carnot 和印度鲁宾。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..