3 月 17 日,药物临床试验登记与信息公示平台官网显示,宜联生物登记了一项在既往一线治疗失败的局部晚期或转移性食管鳞癌参与者中开展的评价 YL201 对比研究者选择的化疗的疗效和安全性的随机、对照、多中心 III 期临床研究(TAISHAN-303)。
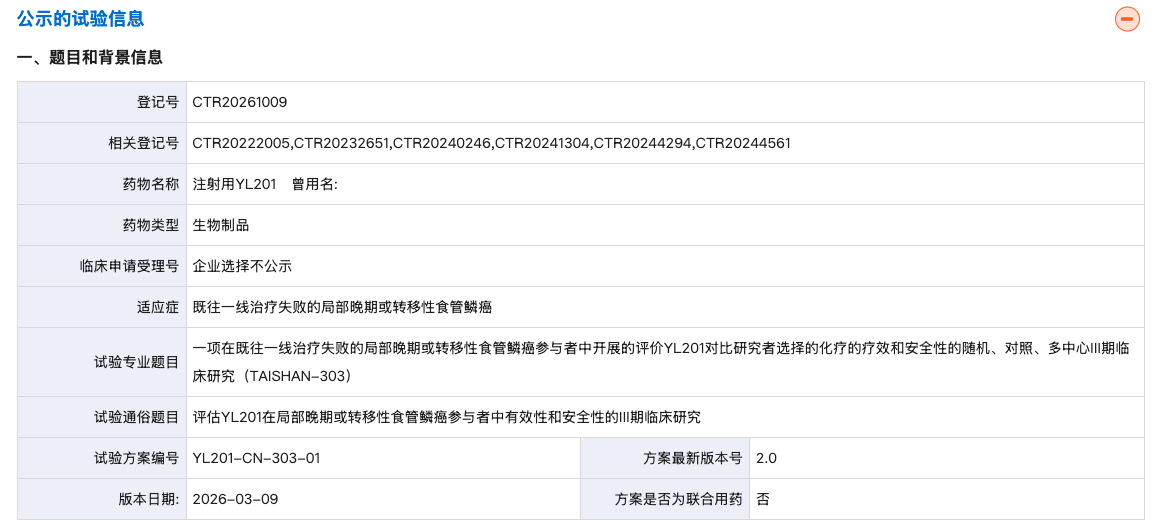
来源:药物临床试验登记与信息公示平台官网
该研究计划入组 440 名受试者,随机分组接受 YL201、紫杉醇+多西他赛+伊立替康治疗。主要终点是 OS。次要终点包括研究者评估的 PFS、ORR、DCR、DoR、TTR,AE、SAE、AESI的发生类型、发生率和严重程度,以及生命体征、临床实验室结果等相较基线的变化等。
这是 YL201 开展的第三项 III 期临床试验,其他两项适应症分别为三线鼻咽癌和二线广泛期小细胞肺癌。
YL201 是宜联生物基于自主创新 TMALIN® 技术平台开发的一款靶向 B7-H3 的 ADC 药物,此前已经四次获得药监局授予的突破性疗法资格。
2026 年 1 月,罗氏引进了该产品在全球范围内(不包括中国大陆、香港特别行政区和澳门特别行政区)的开发、生产和商业化权益,首付款和近期里程碑付款为 5.7 亿美元。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..