3 月 18 日,中国药物临床试验登记与信息公示平台显示,文达医药登记了一项评价 WD-890 片治疗中重度斑块状银屑病有效性和安全性的 III 期临床研究。
根据 Insight 数据库,这是第 5 款进入 III 期临床的国产 TYK2 抑制剂。
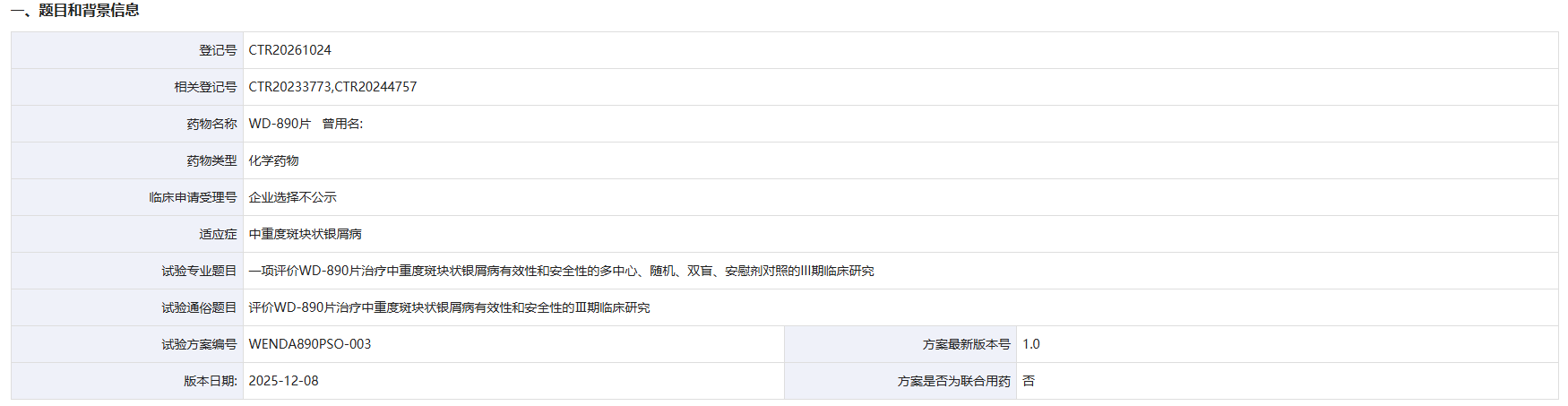
截图来源:药物临床试验登记与信息公示平台
WD-890 片是一种口服、高选择性、变构 TYK2(JH2)抑制剂,由文达医药研发,主要用于治疗银屑病、红斑狼疮等多种自身免疫性疾病。
2025 年 12 月,文达医药宣布 WD-890 片治疗银屑病 II 期临床取得积极结果。该研究由中国医学科学院皮肤病医院陆前进教授牵头、全国多家临床试验中心开展,共招募 143 名患者,分为 4 组,包括 WD-890 片低、中、高剂量组和安慰剂组。
数据显示,经过 16 周治疗后,WD-890 片的低、中、高剂量组分别有 60.0%、86.1% 和 86.1% 的患者达到主要终点 PASI 75(较基线皮损改善至少 75%),显著优于安慰剂组(p<0.001)。
在其他疗效指标方面,WD-890 片的低、中、高剂量组的 PASI 90 应答率分别为 42.9%、63.9%、66.7%;sPGA 0/1 应答率分别为 42.9%、77.8%、66.7%。
在安全性方面,WD-890 片总体安全性、耐受性良好,绝大多数不良事件为轻度或中度,未报告药物相关的严重不良事件。其安全性特征与已上市 TYK2 抑制剂相似,未发现新的安全性信号,未观察到新的与主要不良心血管事件/静脉血栓栓塞/机会性感染相关等的安全性信号。
本次启动的是一项多中心、随机、双盲、安慰剂对照的 III 期临床研究,旨在评价 WD-890 片治疗中重度斑块状银屑病有效性和安全性。该研究拟在国内入组 375 人,主要终点是第 16 周的 PASI 75 应答率和第 16 周的 sPGA 0/1 应答率。
Insight 数据库显示,目前全球仅有 BMS 的氘可来昔替尼一款 TYK2 抑制剂上市,获批适应症包括斑块状银屑病、脓疱性银屑病、红皮病型银屑病和银屑病关节炎。2025 年,该药的全球销售额为 2.91 亿美元,同比增长 18.29%。
除此之外,此前还有 5 款 TYK2 抑制剂已经进入 III 期临床,分别来自翰森制药(HS-10374)、诺诚健华(ICP-488)、武田(Zasocitinib)、Alumis(Envudeucitinib)、益方生物(D-2570)。本次文达医药的 WD-890 成为第 5 款进入 III 期临床的国产 TYK2 抑制剂。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..