3 月 14 日,CDE 官网显示,恒瑞有两款 1 类新药上市申请获得受理,分别为舒地胰岛素诺利糖肽注射液、富马酸立康可泮胶囊。
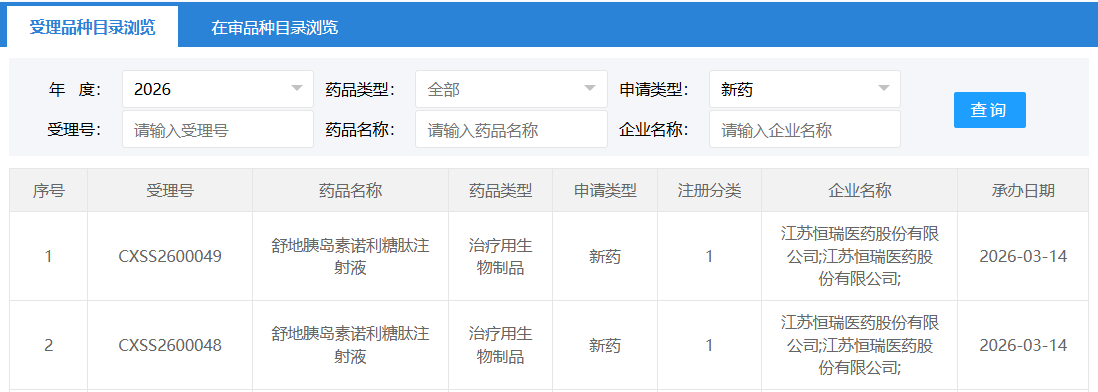
截图来源:CDE 官网
舒地胰岛素诺利糖肽
舒地胰岛素诺利糖肽(研发代号:HR17031)是一款由长效基础胰岛素类似物(INS068)和 GLP-1 受体激动剂(SHR20004)组成的固定复方制剂。本次为该药首次申报上市,适应症为:用于血糖控制不佳的成人 2 型糖尿病患者,在饮食和运动基础上联合其他口服降糖药物,改善血糖控制。
此次申报上市是基于两项在成人 2 型糖尿病(T2DM)患者中开展的多中心、随机、开放、阳性药平行对照的关键 Ⅲ 期临床研究 HR17031-301、HR17031-302。这两项研究分别针对口服降糖药治疗血糖控制不佳及基础胰岛素治疗血糖控制不佳的 T2DM 患者,旨在评价舒地胰岛素诺利糖肽注射液和对照药物的有效性和安全性。
HR17031-301 研究由北京大学人民医院纪立农教授担任主要研究者,随机入组 401 例受试者。HR17031-302 研究由天津医科大学朱宪彝纪念医院陈莉明教授担任主要研究者,随机入组 393 例受试者。两项研究结果均显示,舒地胰岛素诺利糖肽注射液在主要终点上均显著优于试验对照组,且在 2 型糖尿病患者中长期安全性与耐受性良好。
立康可泮
立康可泮是恒瑞研发的一款以补体活化系统旁路途径中 B 因子为靶点的口服小分子抑制剂。补体 B 因子抑制剂可通过靶向因子 B 抑制 AP 能同时控制血管内溶血和血管外溶血,弥补了 C5 补体抑制剂治疗的不足,同时口服给药也提高了患者的用药依从性。
2026 年 1 月,立康可泮的首个上市申请获得 CDE 受理,用于治疗既往未接受过补体抑制剂治疗的阵发性睡眠性血红蛋白尿症(PNH)成人患者,该申请已被 CDE 纳入优先审评。
根据立康可泮的研究进度,Insight 数据库推测该药本次申请的新适应症可能为既往稳定使用 C5 补体抑制剂后仍贫血的阵发性睡眠性血红蛋白尿症。2026 年 1 月,恒瑞已在国内完成立康可泮针对该适应症的多中心、单臂、开放 III 期研究。
根据 Insight 数据库,在 CFB 抑制剂赛道,全球和国内都仅有诺华的伊普可泮获批上市。伊普可泮于 2023 年底首次获批,2024 年销售额为 1.29 亿美元,2025 年销售额同比增长 291% 达到 5.05 亿美元。
在国内,除了伊普可泮,目前还有 3 款 CFB 抑制剂申报上市,都是国产药物,分别来自朗来科技(MY008211A)、海思科医药(HSK39297)、恒瑞医药(立康可泮)。这三款药物的首发适应症都是 PNH,且均已被纳入优先审评。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..