3 月 3 日,CDE 官网显示,礼来的来瑞奇珠单抗注射液上市申请获受理,注册分类为 3.1 类。根据公开信息和临床试验进展,Insight 数据库推测本次申报适应症为特应性皮炎。
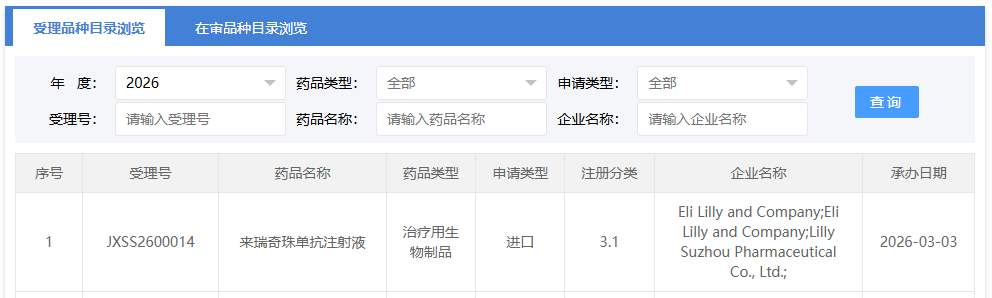
来源:CDE 官网
来瑞奇珠单抗(Lebrikizumab)是一种白细胞介素-13(IL-13)抑制剂,可以高亲和力选择性阻断 IL-13 信号 。IL-13 是特应性皮炎的一种主要细胞因子,驱动皮肤中的 2 型炎症循环,导致皮肤屏障功能障碍、瘙痒、皮肤增厚和感染。
来瑞奇珠单抗的开发经过了一系列曲折的过程。该药最早由罗氏原研,2008 年就开启了首个临床试验,但在首发适应症哮喘上并不顺利,于 2016 年在两项 III 期临床上一胜一败。2017 年 8 月,罗氏将该药授权转让给 Dermira 公司;2019 年,Dermira 公司将欧洲地区的选择权转让给 Almirall 公司;2020 年,礼来收购 Dermira 公司,囊获这一产品。
在海外,来瑞奇珠单抗于 2023 年至 2024 年相继在欧盟、日本和美国获批上市,用于治疗成人及 12 岁以上儿童中重度特应性皮炎患者。
来瑞奇珠单抗的批准主要基于 ADvocate 1、ADvocate 2 和 ADhere 研究的结果,这些研究主要评估入组患者在 16 周时的皮肤症状清除情况。结果显示,经过 16 周的治疗,来瑞奇珠单抗组有 38% 的患者皮肤症状清除或几乎清除(IGA 0 或 1),而安慰剂组为 12%。在症状清除或几乎清除的患者中每月一次用药,77% 的患者维持缓解达到一年。
在国内,礼来于 2024 年登记了一项多中心、随机、双盲、安慰剂对照、III 期试验,旨在中至重度特应性皮炎受试者中评价来瑞奇珠单抗联合/不联合外用皮质类固醇治疗时的有效性和安全性。研究的主要终点是第 16 周达到 EASI-75 的受试者比例。具体研究结果尚未披露。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..