本期看点:
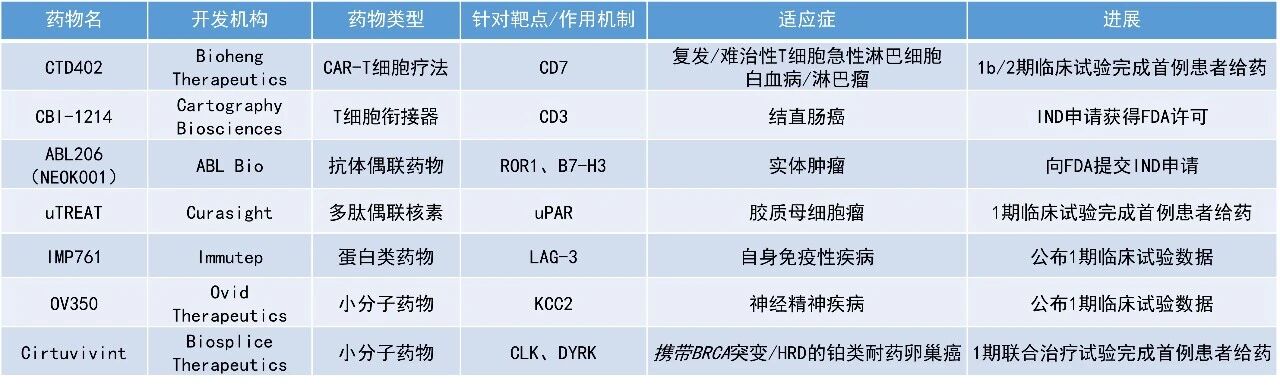
1. 靶向新型肿瘤抗原LY6G6D的T细胞衔接器CBI-1214的IND申请已获得美国FDA批准,并被授予快速通道资格。
2. 选择性泛CLK/泛DYRK激酶抑制剂cirtuvivint与PARP抑制剂olaparib联用治疗携带BRCA突变和/或同源重组缺陷(HRD)的铂类耐药卵巢癌女性患者,该1期联合治疗试验已完成首例患者给药。
CBI-1214:IND申请获得FDA许可
Cartography Biosciences公司宣布,其候选药物CBI-1214的IND申请已获得美国FDA批准,并被授予快速通道资格。公司计划在2026年第一季度启动CBI-1214用于治疗结直肠癌(CRC)的1期临床试验。
CBI-1214是一种T细胞衔接器,靶向一种名为LY6G6D的新型肿瘤抗原。该抗原在健康组织中几乎不表达,却特异性地存在于微卫星稳定型(MSS)和微卫星不稳定性低(MSI-L)的结直肠癌亚型中——这两类患者占CRC患者的绝大多数,且具有巨大的未竟医疗需求。CBI-1214通过蛋白工程优化,旨在增强其抗肿瘤活性,有望成为高度特异性的肿瘤抗原疗法。
Cirtuvivint:1期联合治疗试验完成首例患者给药
Biosplice Therapeutics公司宣布,其开展的一项1期临床试验已为首位患者给药,该试验旨在评估小分子药物cirtuvivint与PARP抑制剂olaparib联用治疗携带BRCA突变和/或HRD的铂类耐药卵巢癌女性患者。该研究尤其针对既往已接受过PARP抑制剂治疗的患者。Cirtuvivint是一种选择性泛CLK/泛DYRK激酶抑制剂,通过调控RNA选择性剪接(包括参与致癌通路的转录本)发挥抗肿瘤作用。
临床前研究表明,cirtuvivint可通过抑制CLK/DYRK激酶,间接阻断肿瘤细胞在PARP抑制剂压力下激活的“备用生存通路”——WNT/TCF信号通路。在多种BRCA突变或HRD的高级别浆液性卵巢癌耐药模型中,cirtuvivint不仅抑制WNT/TCF转录活性、降低核内β-catenin水平,还诱导DNA损伤、降低肿瘤细胞存活能力,并与olaparib协同延缓肿瘤进展、延长生存期(无论在免疫正常或免疫功能低下的动物模型中均有效)。此外,该药还能改善肿瘤免疫微环境,例如减少免疫抑制性PD-1/PD-L1表达细胞。这些数据为临床探索cirtuvivint联合olaparib以克服或延缓PARP抑制剂耐药提供了有力依据。
IMP761:公布1期临床试验数据
Immutep公司宣布,其在健康受试者中开展的首个人体、安慰剂对照、双盲1期临床试验取得积极进展,该试验旨在评估IMP761——一种潜在“first-in-class”的LAG-3激动型抗体,用于治疗自身免疫性疾病。IMP761通过特异性沉默聚集在病灶部位的自身免疫记忆T细胞,有望从根源上干预多种自身免疫疾病,并恢复免疫系统平衡。
该研究的单次递增剂量部分已顺利完成2.5 mg/kg和7 mg/kg两个剂量组的给药。IMP761展现出良好的安全性,未出现超出轻度的治疗相关不良反应。同时,观察到IMP761具有明确的剂量依赖性免疫抑制效应,在第2天、第9天和第23天,IMP761显著且持久地抑制了受试者对强异源抗原引发的三种T细胞介导的皮内反应。T细胞活性的显著降低凸显了IMP761在治疗自身免疫疾病中的潜在疗效。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..