11 月 21 日,CDE 官网显示,和黄医药酒石酸凡瑞格拉替尼片拟纳入优先审评,适应症为:用于既往接受过系统性治疗且经检测确认存在有 FGFR2 融合或重排的晚期、转移性或不可手术切除的肝内胆管癌(ICC)成人患者的治疗。
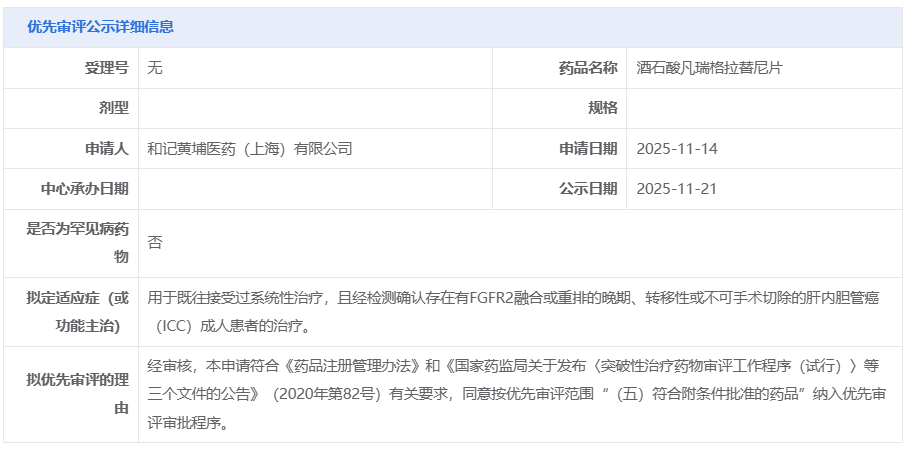
截图来源:CDE 官网
根据和黄医药公开资料,Insight 数据库推测凡瑞格拉替尼是和黄医药开发的在研1 类新药 Fanregratinib(HMPL-453)。
HMPL-453 是一种新型、高选择性且强效的 FGFR 1、2 和 3 抑制剂。异常的 FGFR 信号传导已被发现是肿瘤生长(通过组织生长和修复)、促进血管生成及抗肿瘤治疗抗性产生的诱因,异常的 FGFR 基因改变被认为是多种实体瘤肿瘤细胞增殖的驱动因素。
和黄医药拟开发 HMPL-453 用于治疗间皮瘤、肝内胆管癌等实体瘤。
在国内,和黄医药正在开展一项单臂、多中心、开放标签的 II 期注册研究(CTR20201011),旨在评估 HMPL-453 用于治疗伴有 FGFR2 融合/重排的晚期肝内胆管癌患者的疗效、安全性和药代动力学。研究的主要终点是客观缓解率 (ORR) 。次要终点包括无进展生存期 (PFS) 、疾病控制率 (DCR) 、缓解持续时间 (DoR) 和总生存期 (OS) 。
这项 Ⅱ 期试验已完成患者招募,和黄医药预计将在 2025 年年底左右公布研究的临床数据,若取得积极结果,该研究将用于支持 HMPL-453 向中国 NMPA 提交新药上市申请。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..