本期看点:
1. ALK选择性抑制剂neladalkib治疗晚期ALK阳性非小细胞肺癌,在一项1/2期临床试验中的客观缓解率(ORR)达31%,并在脑转移病灶中观察到明确疗效,其颅内ORR(IC-ORR)达63%。
2. 大环MEK抑制剂PAS-004用于治疗MAPK通路驱动的晚期实体肿瘤取得了积极的1期临床试验数据,BRAF突变患者的疾病控制率(DCR)为71.4%。
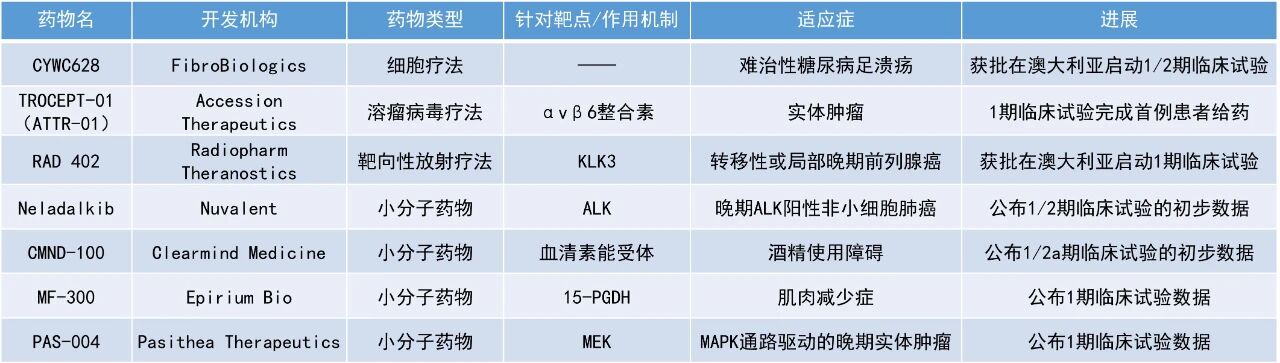
Neladalkib:公布1/2期临床试验的初步数据
Nuvalent公司公布了其在研ALK选择性抑制剂neladalkib的关键性临床研究积极主要结果。这次所公布的结果来自全球性ALKOVE-1临床1/2期试验中,既往接受过酪氨酸激酶抑制剂(TKI)治疗的晚期ALK阳性非小细胞肺癌患者队列。同时,公司也公布该研究中针对未接受过TKI治疗的ALK阳性晚期NSCLC患者2期探索性队列的初步数据。数据显示,在253例TKI既往治疗患者中,经盲法独立中央评估(BICR)确认的ORR为31%(95% CI:26–37),其在12个月和18个月时的持续缓解率分别为64%和53%。在63例曾接受过TKI但未接受lorlatinib治疗的患者亚组中,ORR达到46%(95% CI:33–59),患者在12个月和18个月的持续缓解率分别为80%与60%。
此外,研究显示,neladalkib在脑转移病灶中亦观察到明确疗效。在24名具有脑转移病灶,且曾接受过TKI但未曾接受过lorlatinib治疗的患者中,其IC-ORR达63%(95% CI:41–81),患者在12个月和18个月的持续缓解率分别皆为92%(95% CI:57–99)。Neladalkib并展现出良好的安全性特征。仅有5%的患者因治疗伴发不良事件(TEAEs)停药,整体耐受性与其具ALK选择性、避免TRK抑制的设计一致。
PAS-004:公布1期临床试验数据
Pasithea Therapeutics公司公布了其大环MEK抑制剂PAS-004用于治疗MAPK通路驱动的晚期实体肿瘤的积极1期临床试验数据。与目前FDA批准的MEK抑制剂不同,PAS-004是大环化合物,环化可增强药物与靶受体的结合,被认为有望改善药代动力学和安全性。
此次公布的结果显示,在21例疗效可评估的患者中,DCR为42.8%(9/21),其中,BRAF突变患者的DCR为71.4%(5/7)。一例BRAF V600E突变黑色素瘤患者(15 mg剂量组)实现未确认的部分缓解(肿瘤缩小31.9%),已持续治疗超过11个月;另一例同类患者(30 mg剂量组)获得持续超过6个月的疾病稳定(肿瘤缩小1.6%)。PAS-004的安全性和耐受性良好,所有治疗相关不良事件均为1–2级,无眼部或心脏毒性,且皮疹、恶心、腹泻和呕吐为轻度。
MF-300:公布1期临床试验数据
Epirium Bio公司宣布,其潜在“first-in-class”的口服15-羟基前列腺素脱氢酶(15-PGDH)抑制剂MF-300,在针对肌肉减少症的1期临床试验中取得积极结果。5-PGDH是一种能将前列腺素E2(PGE2)转化为非活性代谢物的酶。MF-300旨在可逆地结合到15-PGDH的PGE2结合位点上,阻止该酶转化PGE2。临床前研究表明,MF-300能增强老年小鼠及其他神经源性萎缩临床前模型的肌肉力量并改善肌肉质量。
该临床研究在82名健康成人中评估了其安全性、药代动力学(PK)和药效学(PD)。研究结果显示,MF-300在多次给药后吸收迅速,暴露量呈剂量依赖性增加,半衰期支持每日一次给药;其暴露水平达到临床前研究中与疗效相关的阈值,提示有望实现临床获益。安全性方面未出现预期外或剂量限制性毒性、严重不良事件或提前停药。PD分析证实药物有效作用于靶点:尿液中PGE2升高,同时其主要代谢物PGE-MUM显著降低。PGE-MUM下降的幅度,与之前在老年小鼠实验中看到的、能带来肌肉质量提升和肌力增强的PGE-MUM降低程度是匹配的。总体而言,该研究在安全性、PK和PD所有预设指标上均达成成功标准,为MF-300的后续临床开发奠定了坚实基础。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..