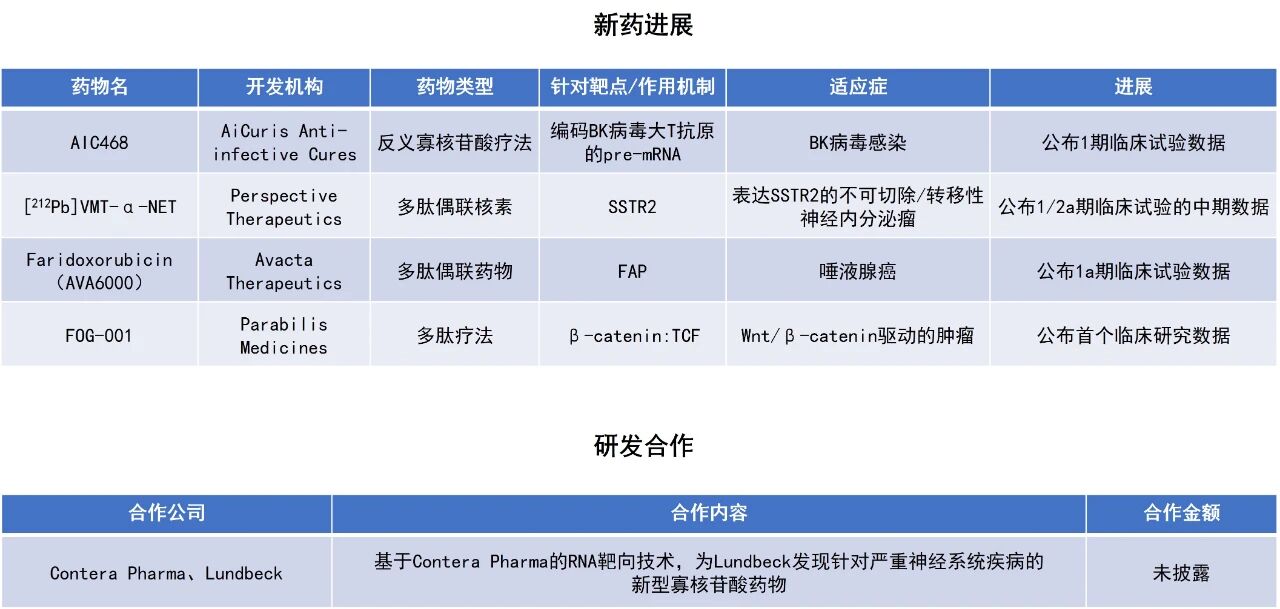
近期,全球多肽和寡核苷酸(TIDES)领域迎来系列进展。靶向“不可成药”靶点的多肽偶联药物FOG-001公布首个临床研究的亮眼数据,在硬纤维瘤患者中的疾病控制率(DCR)达100%,客观缓解率(ORR)达80%。在研多肽偶联药物AVA6000的1期临床试验结果积极,唾液腺癌队列的DCR达91%。多肽偶联核素疗法[212Pb]VMT-α-NET在一项1/2a期临床试验中,使87.5%的不可切除/转移性神经内分泌瘤(NET)患者没有疾病进展。本文将节选其中部分重要进展做简单介绍,仅供读者参阅。
FOG-001:公布首个临床研究数据
Parabilis Medicines公司公布了其在研疗法FOG-001的首个临床数据,证实其成功靶向了此前被认为是“不可成药”的Wnt/β-catenin信号通路中的关键节点——β-catenin与T细胞因子(TCF)的相互作用。该通路是30多年前发现的核心致癌驱动因素,每年与数百万癌症病例相关,但目前尚无针对它的获批疗法。FOG-001是该公司基于其Helicon肽平台开发的候选药物,通过阻断β-catenin与TCF转录因子家族的结合,直接抑制由Wnt通路激活驱动的肿瘤形成。该平台利用稳定的α-螺旋肽,克服了传统小分子药物的局限性,能够进入细胞并与相对平坦的蛋白质表面紧密结合。
在一项针对多种Wnt/β-catenin驱动肿瘤的1/2期临床试验中,截至2025年8月中旬,已有12名患有硬纤维瘤的患者接受了FOG-001治疗。在10名至少有1次后续影像评估的患者中,所有剂量组均观察到肿瘤缩小,DCR达100%。在5名有1次以上影像评估的患者中,ORR为80%(4/5),且无论既往是否接受过γ分泌酶治疗均有效果。安全性方面,FOG-001表现出可接受的安全性和耐受性。
Faridoxorubicin(AVA6000):公布1a期临床试验数据
Avacta Therapeutics公司公布了其主打在研多肽偶联药物AVA6000的1a期临床试验积极数据。AVA6000是Avacta研发管线中的首个多肽偶联药物,由多柔比星与Avacta专有的pre|CISION多肽偶联而成,该多肽可在肿瘤微环境中由成纤维细胞激活蛋白-α(FAP)特异性切割。FAP在大多数实体瘤中,与健康组织相比表达水平显著升高。Avacta的多肽偶联药物利用这一特征在肿瘤微环境中特异性释放活性药物,从而降低系统暴露和毒性,为患者提供更好的治疗效果。
在1a期研究中,无论是每三周一次还是每两周一次的给药方案,AVA6000均显示出良好的安全性和耐受性。即使剂量升高至每三周385 mg/m²(约4倍常规阿霉素剂量),也未达到最大耐受剂量(MTD),且即使在累积剂量高达550 mg/m²下,也未观察到严重的心脏毒性,表明与传统阿霉素治疗相关的毒性显著降低。唾液腺癌患者队列尚未达到中位无进展生存期(PFS),DCR为91%。
[212Pb]VMT-α-NET:公布1/2a期临床试验的中期数据
Perspective Therapeutics公司公布了其候选多肽偶联核素疗法[212Pb]VMT-α-NET的1/2a期临床试验的最新中期数据。该研究旨在评估[212Pb]VMT-α-NET在表达SSTR2的不可切除/转移性神经内分泌瘤患者中的疗效和安全性。
截至2025年9月12日的数据,该疗法安全性良好,在接受至少一种治疗的总共55名患者中,没有观察到剂量限制性毒性,也没有因不良事件而停药。队列1和队列2的25名患者中有20名(80%)没有疾病进展。中位随访时间为41周时,在所有肿瘤中均表达SSTR2的16名队列2的患者中,有7名达到了研究者评估的客观缓解,ORR为44%,87.5%(14名)的患者没有疾病进展,并继续接受研究。
AIC468:公布1期临床试验数据
Aicuris Anti-infective Cures公司公布了其用于治疗BK病毒(BKV)感染的新型反义寡核苷酸(ASO)疗法AIC468的积极1期临床试验数据。AIC468旨在治疗肾移植患者中的BK病毒再激活,该病症可能带来重大的健康风险。该候选药物通过抑制编码病毒大T抗原的pre-mRNA的剪接,来阻断病毒在感染细胞内的复制。AIC468的1期结果显示出良好的安全性和药代动力学特征,支持进一步的临床开发,用于治疗肾移植受者的BKV感染
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..