截至6月30日,FDA已经批准了16款创新药,其中包括9款化药新药和7款生物药新药,First-in-class药物占据半壁江山(8款)。
从适应症上看,肿瘤药物获批最多,一共有7款,免疫领域有3款,其他领域各1款。与此同时,罕见病领域研发依旧火热,一共有4款药物上市。
值得一提的是,今年上半年的新药获批数量明显少于去年,2024年同期已有21款新药获批,主要是化药新药上市数量减少(去年同期有14款化药新药上市),这一现象反映了FDA审批标准的严格性在持续强化。
表1 2025年上半年,FDA批准新药盘点
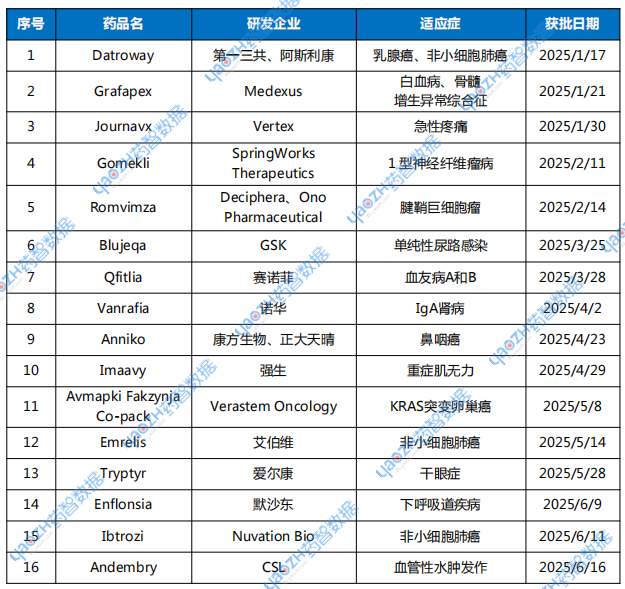
数据来源:药智数据、FDA官网
肿瘤领域:ADC爆发、靶向治疗再升级
2025年上半年,ADC在肿瘤治疗领域迎来新突破。两款关键ADC的获批填补了实体瘤靶向治疗的空白,而首款KRAS突变卵巢癌疗法的问世则标志着协同抑制策略的成熟,共同推动肿瘤领域精准治疗进入新阶段。
Datroway:乳腺癌与肺癌的双重突破
阿斯利康与第一三共联合开发的Datroway成为上半年焦点。该药物由人源化的、靶向在乳腺癌和肺癌中高表达的Trop-2的单克隆抗体与DNA拓扑异构酶I抑制剂(DXd))连接。搭载的拓扑异构酶I抑制剂DXd,活性比传统化疗药伊立替康高10倍,且具备强膜渗透性,可触发“旁观者效应”,在杀伤靶细胞后扩散至邻近肿瘤细胞,克服肿瘤异质性难题。
Datroway于2025年1月获得FDA批准,用于治疗既往接受过内分泌治疗和化疗的HR阳性、HER2阴性不可切除或转移性乳腺癌成人患者,并在6月获得FDA加速批准治疗NSCLC。
Emrelis:攻克肺癌难治亚型
艾伯维的Emrelis于5月获批,聚焦c-Met高表达非鳞状NSCLC,该亚型预后极差且缺乏靶向方案,通过抗体靶向c-Met受体,释放微管蛋白抑制剂MMAE直接破坏癌细胞分裂,是首个批准用于治疗c-Met过度表达的经治疗晚期NSCLC的疗法。
Avmapki Fakzynja Co-pack:KRAS耐药困境的破局者
Verastem Oncology的Avmapki Fakzynja Co-pack由Avutometinib和Defactinib组成。其中Avutometinib是具有口服活性的MEK1抑制剂,Defactinib是FAK和Pyk2的抑制剂。FAK/RAF/MEK抑制可协同诱导黑色素瘤细胞体外凋亡,促进体内肿瘤消退,延长已有脑转移瘤小鼠的存活时间。该药物于5月8日获FDA批准,用于治疗复发性低级别浆液性卵巢癌(LGSOC)成年患者,这些患者曾接受过系统性治疗并且其肿瘤携带KRAS突变。
罕见病迈向“精准治疗”时代
长久以来,罕见病治疗常囿于“药物匮乏”的困境,传统疗法往往仅能缓解症状或效果有限。然而,2025年上半年获批的4款创新疗法,正推动罕见病治疗领域迈入“精准治疗”新时代。
Andembry:预防遗传性血管性水肿发作的首款因子XIIa靶向疗法
Andembry是一种抗FXIIa的单克隆抗体,特异性抑制血浆蛋白FXIIa。当FXII被激活时,会启动导致水肿形成的级联反应。通过靶向FXIIa,Andembry能在反应最初阶段就阻断级联反应的信号传导。该药于6月16日获得FDA上市,用于预防成人和12岁及以上儿童患者遗传性血管性水肿(HAE)发作,它是首款只需每月一针、靶向血浆蛋白因子XIIa(FXIIa)的HAE发作预防疗法。
Qfitlia:可治疗所有血友病类型的siRNA疗法
3月28日,FDA批准赛诺菲和Alnylam联合开发的siRNA疗法Qfitlia上市,用于预防或减少12岁以上血友病A和血友病B患者的出血事件。Qfitlia通过降低抗凝血酶水平,从而促进凝血酶生成,重新平衡止血功能并预防出血。由于这一独特作用机制,它可以治疗多种不同类型的血友病,大大扩展了它的应用范围。在两项3期临床试验中,它只需每月一次皮下注射,就可将患者的年化出血率降低90%。在有些患者中,给药次数可降低到每两个月一次。
Gomekli:潜在“best-in-class”别构小分子抑制剂
Gomekli是一种口服别构小分子MEK抑制剂,靶向MEK1和MEK2。2月11日,FDA批准Gomekli上市,用于治疗年龄不低于2岁的1型神经纤维瘤病相关丛状神经纤维瘤(NF1-PN)成人和儿童患者。它是首个获批可同时用于治疗成人和儿童NF1-PN的药物,有望成为儿童NF1-PN患者的“best-in-class”疗法。此外,FDA还授予了该药物快速通道资格,用于治疗2岁及以上的神经纤维瘤病1型相关的丛状神经纤维瘤患者。它的新药申请也曾获得FDA授予的优先审评资格。
Rommviva抗肿瘤口服小分子疗法
Rommviva是一种口服酪氨酸激酶抑制剂,专门设计用于选择性和强效抑制CSF1R,有效抑制CSF1R的自磷酸化及下游信号传导,从而抑制肿瘤细胞的增殖和存活。该药品由Deciphera Pharmaceuticals开发,2024年4月Ono Pharmaceutical与Deciphera达成并购协议,斥资24亿美元收购了Deciphera公司并囊获这款疗法。2025年2月14日,美国FDA批准Romvimza(vimseltinib)上市,用于治疗腱鞘巨细胞瘤(TGCT)患者。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..