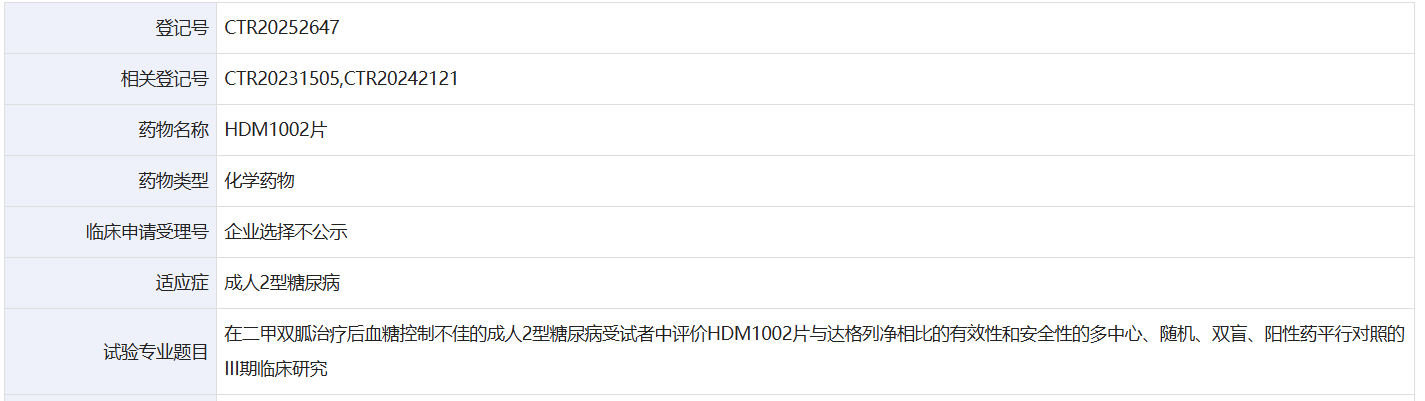
7 月 7 日,中国药物临床试验登记与信息公示平台显示,中美华东登记了一项国内 III 期临床研究,以在二甲双胍治疗后血糖控制不佳的成人 2 型糖尿病受试者中评价 HDM1002 片与达格列净相比的有效性和安全性。研究的主要目的是证实 HDM1002 片控制血糖的疗效非劣效于达格列净。
HDM1002 片是由中美华东自主研发并拥有全球知识产权的 GLP-1 受体小分子激动剂,具有口服活性、强效、高选择性。
今年 3 月,HDM1002 片已启动用于超重或肥胖人群的体重管理的中国 Ⅲ 期临床研究(CTR20251246),试验的主要目的是在减少饮食热量摄入和增加体力活动基础上。这项研究已在国内完成首例受试者入组,主要指标预计将于明年 6 月 30 日完成。
Insight 数据显示,目前全球共有 33 款在研的小分子 GLP-1R 口服药物(仅统计活跃管线),进度最快的在 Ⅲ 期阶段,有 4 款产品,分别来自礼来(Orforglipron)、恒瑞(HRS-7535)、闻泰医药/箕星药业(VCT220)、华东医药(HDM1002)。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..