5 月 9 日,NMPA 官网显示,翰森制药「甲磺酸阿美替尼片」(阿美乐®)获批一项新适应症(受理号:CXHS2400060),用于具有表皮生长因素受体(EGFR)外显子 19 缺失或外显子 21(L858R)置换突变阳性的非小细胞肺癌(NSCLC)成人患者肿瘤切除术后的辅助治疗。


阿美替尼由翰森制药研发,该药创新性地引入环丙基结构,具有良好的脂溶性和稳定性,能更好地透过血脑屏障,且不良反应发生率低。阿美替尼是国产首款三代 EGFR-TKI,早在 2020 年 3 月就已经获批上市,同年通过谈判进入医保目录。
翰森针对阿美替尼进行了广泛而深入的适应症布局,陆续获批了二线适应症、一线适应症、维持/巩固治疗,现今又获批了辅助疗法适应症。
在已获批适应症之外,翰森还探索了阿美替尼联用化疗(培美曲塞和铂类)一线治疗 NSCLC,该项适应症也已经在 2024 年 11 月报上市(CXHS2400127),Insight 数据库预计将于今年下半年获批。
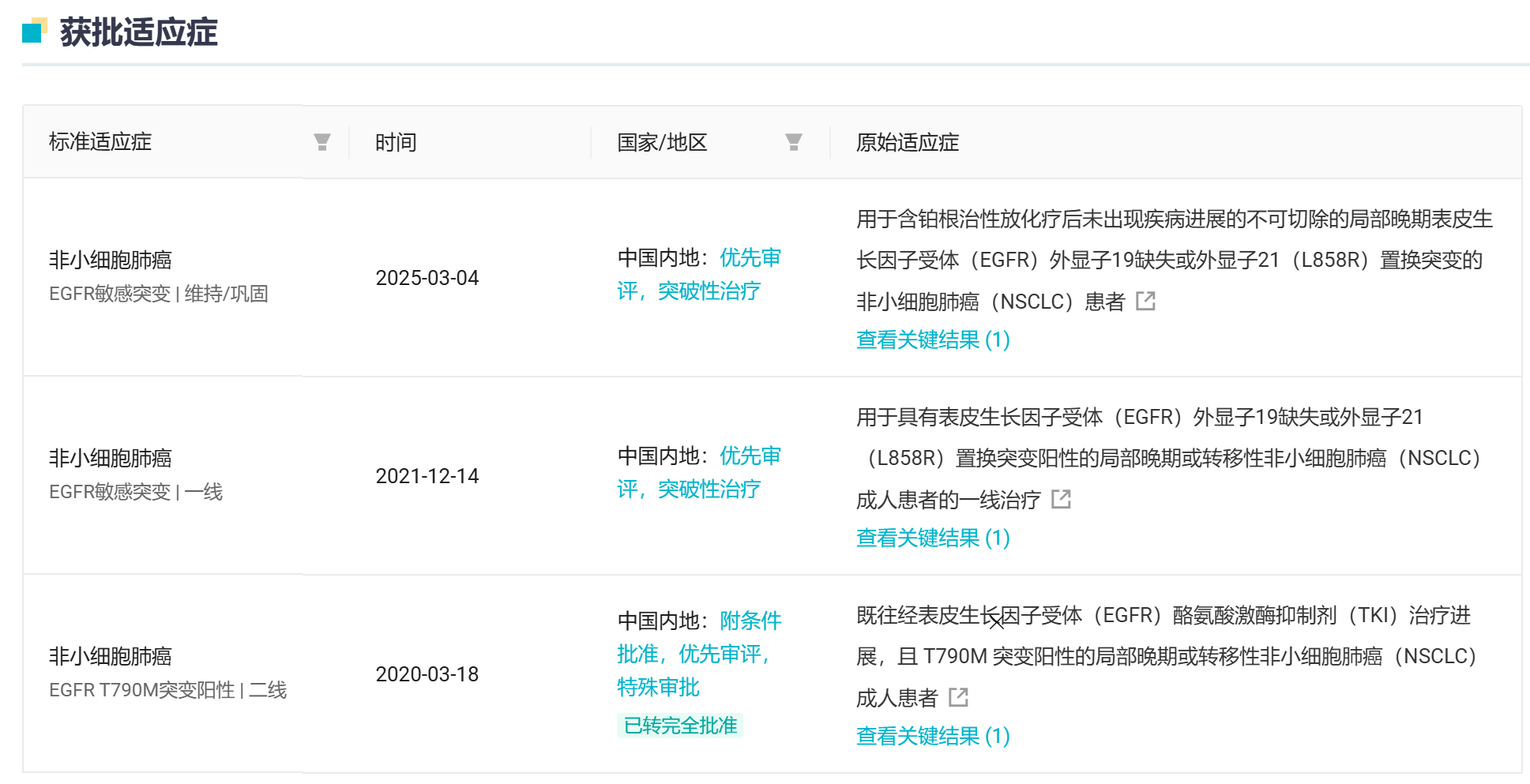
阿美替尼此前已上市适应症
本次上市批准是基于 III 期临床试验 HS-10296-302 研究(NCT04687241)的积极数据。这是一项随机、对照、双盲、多中心 III 期临床研究,旨在评估甲磺酸阿美替尼对比安慰剂用于表皮生长因子受体敏感突变阳性 II-IIIB 期 NSCLC 辅助治疗的有效性和安全性。
结果显示,阿美替尼组未达到 BICR 评估的 mDFS,而安慰剂组为19.4个月(HR 为 0.166,p<0.0001)。阿美替尼组 2 年 DFS 率为 88.2%,安慰剂组为 40.6%。研究者评估的 DFS 与 BICR 评估结果一致。数据截止时,OS 数据尚不成熟(奥莫替尼和安慰剂 OS 成熟度:2.8% vs. 3.8%)。
在安全性方面,阿美替尼和安慰剂组导致剂量中断、剂量减少及停药的不良事件发生率分别为 12.3% vs. 17.8%、9.4% vs. 1.9% 和 0.9% vs. 0。未观察到新的安全风险。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..