3月13日,ICH发布了M13B指南草案《口服固体速释制剂的生物等效性 - 其它规格的生物等效性豁免》,计划将于2026年11月定稿并在各监管区域实施。
ICH M13B指南是M13系列的第二份指南,旨在解决口服速释制剂其它规格的体内生物等效性(BE)研究的豁免,描述在科学和技术层面证明其它规格的生物等效性。该指南将提供建议,当药品的至少一个规格的BE符合ICH M13A,可获得一个或多个其它规格的BE研究豁免,减少体内BE研究的额外需求,支持简化全球药物研发。
M13B指南所描述的生物等效性豁免标准是围绕PK剂量比例,原料药与辅料配方比例,及其它规格与生物批次规格相比溶出曲线相似性,但未详细讨论其它规格证明生物等效性的替代方法,例如体外-体内相关性(IVIVC)或其它建模方法。
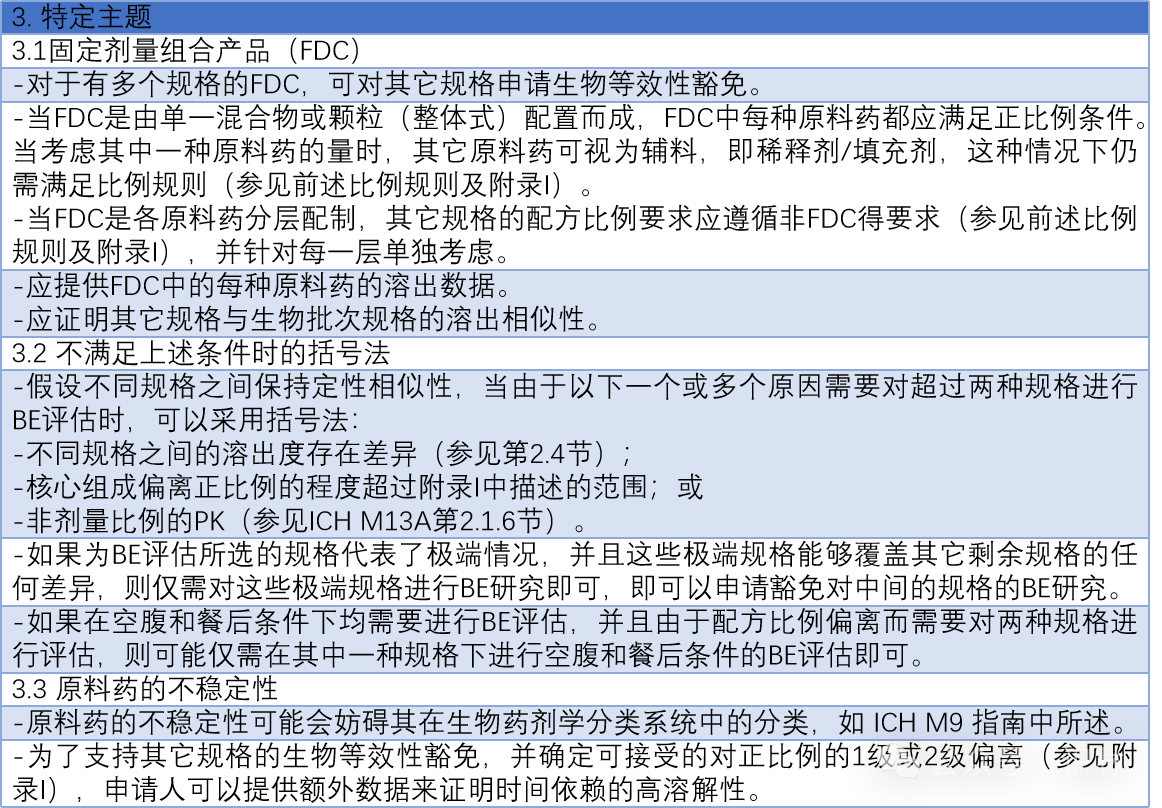
按照指南章节,总结主要内容如下:

四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..