2月20日,中国国家药监局药品审评中心(CDE)最新公示,阿斯利康(AstraZeneca)申报的硫酸氢司美替尼胶囊的上市申请获得受理。公开资料显示,司美替尼是由阿斯利康和默沙东(MSD)公司共同开发的MEK抑制剂,此前已经在中国获批治疗3岁及3岁以上伴有症状、无法手术的丛状神经纤维瘤(PN)的1型神经纤维瘤病(NF1)儿科患者。根据公开资料可以推测,本次在中国申报的新适应症可能为:治疗患有症状性、不可手术丛状神经纤维瘤(PN)的1型神经纤维瘤病(NF1)成人患者。
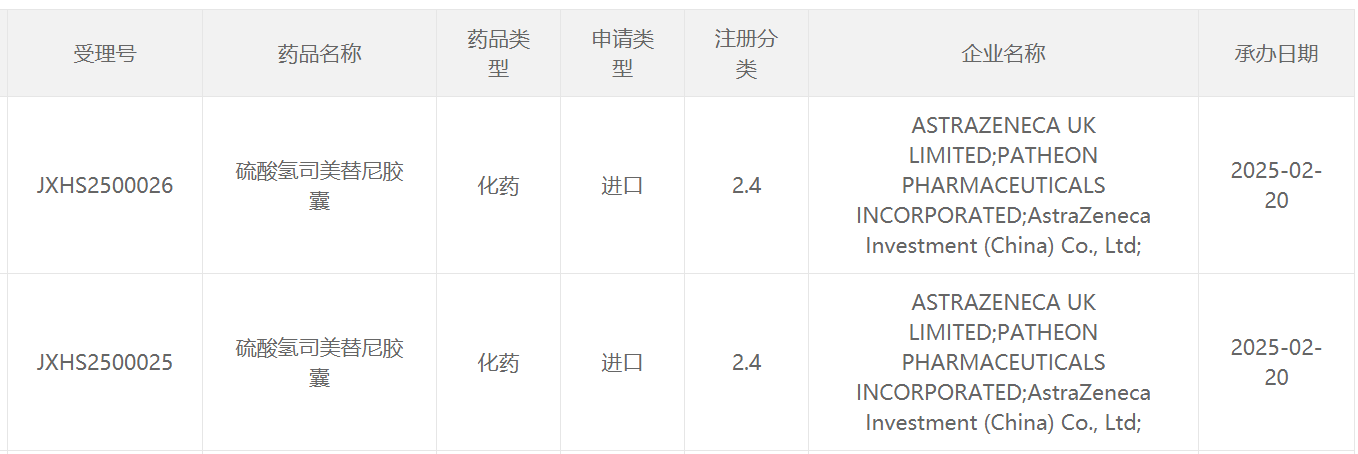
截图来源:CDE官网
司美替尼(selumetinib)是一种激酶抑制剂,可阻断参与促进细胞生长的特定酶(MEK1和MEK2)。在NF1中,这些酶过度活跃,导致肿瘤细胞以不受调节的方式生长,产生所谓的丛状神经纤维瘤(PN)。通过阻断这些酶,司美替尼减缓了肿瘤细胞的生长,从而减缓了PN的生长。
2017年7月,阿斯利康和默沙东宣布开展全球战略合作,共同推动司美替尼的开发和商业化。司美替尼此前已在美国、欧盟(EU)、日本、中国获得批准,用于治疗有症状、不能手术的小儿NF1型PN患者。
2024年11月,阿利斯康和默沙东联合公布KOMET临床3期试验的积极顶线结果。KOMET研究旨在评估司美替尼在患有症状性、不可手术丛状神经纤维瘤的NF1成年患者中的疗效和安全性。该研究结果显示,司美替尼在这些成年患者中,相较于安慰剂,在主要终点客观缓解率(ORR)方面表现出统计学显著和具有临床意义的改善,能够使患者的肿瘤体积显著缩小。试验中,ORR定义为在第16个周期(每周期28天)由独立中央审评(ICR)根据神经纤维瘤和施万细胞瘤的应答评估标准(REiNS)确认的完全缓解(PN消失)或部分缓解(肿瘤体积减少至少20%)的患者百分比。
根据中国药物临床试验登记与信息公示平台官网,KOMET研究也已经在中国开展,并已在中国完成受试者招募。
NF1是一种罕见,不可治愈的遗传性疾病。NF1是因为合成神经纤维瘤蛋白的NF1基因发生突变引起的。该基因突变可扰乱RAS/MAPK信号通路(RAS-RAF-MEK-ERK),进而导致肿瘤的生长。约一半的NF1患者可能为丛状神经纤维瘤,会引起疼痛、神经功能障碍、骨骼畸形,严重时可危及生命。由于大多数NF1患者不可手术,或手术风险大且复发率高,NF1的药物治疗需求非常迫切。
随着新药研发的进展,NF1的临床治疗也正在迎来越来越多的选择。比如,几日前(2月12日),美国FDA批准了SpringWorks Therapeutics公司的MEK抑制剂mirdametinib上市,用于治疗年龄不低于2岁的1型神经纤维瘤病相关丛状神经纤维瘤(NF1-PN)成人和儿童患者;复星医药自主研发的新型MEK1/2选择性抑制剂复迈替尼(FCN-159)也已经在中国申报上市,并被纳入优先审评,用于治疗2岁及2岁以上儿童NF1相关的丛状神经纤维瘤(PN)。此外,还有多款已获批上市的药物如抗PD-1单抗类药物正在针对NF1适应症开展临床探索。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..