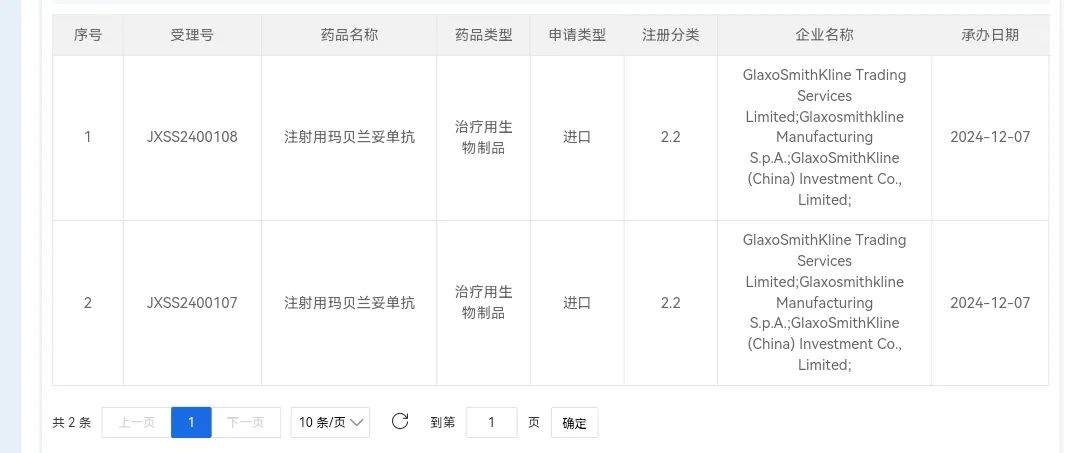
12 月 07 日,CDE 官网显示,葛兰素史克的注射用玛贝兰妥单抗(Belantamab mafodotin )上市申请获得受理。此前,该申请已被纳入优先审评,适应症为与硼替佐米+地塞米松联合治疗既往接受过至少一种治疗的多发性骨髓瘤(MM)成年患者。
Belantamab mafodotin 是一款靶向 BCMA 的抗体偶联药物(ADC)。2020 年 8 月,基于关键性 Ⅱ 期临床 DREAMM-2 研究的结果,该药先是获得 FDA 加速批准上市,而后获得 EMA 附条件批准上市,作为单药疗法治疗复发/难治性多发性骨髓瘤成人患者,成为了全球首个获批上市的 BCMA ADC。
不过,FDA 的加速批准和 EMA 的附条件批准都是有「条件」的,Belantamab mafodotin 的结果需要在后续 Ⅲ 期临床试验 DREAMM-3 中得到进一步证实才可以。DREAMM-3 试验旨在评估Belantamab mafodotin 单药与泊马度胺联合低剂量地塞米松治疗复发/难治 MM 患者的疗效和安全性,主要终点是 PFS,次要终点包括总生存期、安全性、ORR、反应持续时间和微小残留病评估。
然而,2022 年 11 月,GSK 宣布 DREAMM-3 研究未达到其无进展生存期 (PFS) 的主要终点。基于此,GSK 主动撤回了 Belantamab mafodoti 在美国的上市申请。随后,欧盟 EMA 也撤回了 Belantamab mafodoti 的上市许可。
虽然在日本和欧盟的上市不顺利,但研究显示 Belantamab mafodoti 还可以使部分多发性骨髓瘤患者受益。
例如,在 Ⅲ 期临床试验 DREAMM-7 中,研究人员评估了 Belantamab mafodotin +硼替佐米+地塞米松与达雷妥尤单抗 +硼替佐米+地塞米松 联合治疗复发/难治性多发性骨髓瘤患者的疗效和安全性,这些患者之前至少接受过一线治疗,主要终点是 PFS。
2024 年 ASCO 年会上公布的数据显示,在意向治疗人群 (ITT) 中:
中位 PFS 方面,Belantamab mafodotin 组为 36.6 个月,显著高于达雷妥尤单抗组的 13.4 个月;
与标准治疗达雷妥尤单抗组合相比,将患者病情进展或死亡风险降低了 59%;
ORR 方面,Belantamab mafodotin 组为 82.7%(vs 达雷妥尤单抗组 71.3%);
Belantamab mafodotin 组治疗在总体生存率方面呈现出强劲、具有临床意义的趋势,死亡风险降低了 43%。
此外,在 III 期临床试验 DREAMM-8 中,研究人员又评估了 Belantamab mafodotin + 泊马度胺+地塞米松联合治疗与硼替佐米+ 泊马度胺+地塞米松联合治疗复发/难治 MM 的疗效和安全性,这些患者之前曾接受过至少一线治疗。
与 DREAMM-7 试验中研究的患者群体相比,DREAMM-8 中的患者接受的预先治疗更多,因为所有患者都曾接受过来那度胺治疗,75% 患者对来那度胺有耐药性,25% 患者曾接受过达雷妥尤单抗治疗,其中大多数对达雷妥尤单抗有耐药性。
今年 ASCO 上公布的 DREAMM-8 研究数据显示:
在主要终点 mPFS 方面,试验组尚未达到,对照组为 12.7 个月;
次要终点方面,试验组 ORR 为 77%(vs 对照组 72%),CR 为 40%(vs 对照组 16%),mDoR 尚未达到(vs 对照组 17.5 个月),12 个月 PFS 率为 71%(vs 对照组 51%),OS 随访仍在进行中。
DREAMM-8 研究认为,在复发/难治 MM 中,Belantamab mafodotin 组具有统计学意义和临床意义的 PFS 优势,而且还带来了更深层次和更持久的反应,显示出良好的 OS 趋势,并且具有可控的安全性。
基于 DREAMM-7 和 DREAMM-8 的积极研究数据,今年 7 月和 9 月,欧洲 EMA 和日本厚生劳动省 (MHLW) 已分别接受了 Belantamab mafodotin 与硼替佐米+地塞米松 (BorDex) 或泊马度胺+地塞米松 (PomDex) 联合治疗复发或难治性多发性骨髓瘤的上市申请。
本次在中国申报上市并被纳入优先审评意味着,其将有望在国内加速获批,早日惠及国内患者。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..