2024年8月30日,中国生物制药领域的又一重要进展引起了广泛关注。据中国国家药监局药品审评中心(CDE)最新公示,三生制药提交的关于其重组人血小板生成素注射液(商品名为特比澳®),旨在治疗拟接受择期侵入性手术的慢性肝病相关血小板减少症患者的新适应症上市申请,已经成功获得中国国家药品监督管理局药品审评中心的受理。这一信号,不仅标志着三生制药在血液系统疾病治疗领域的持续创新与突破,更为长期受困于慢性肝病的广大患者群体带来了希望与期待。
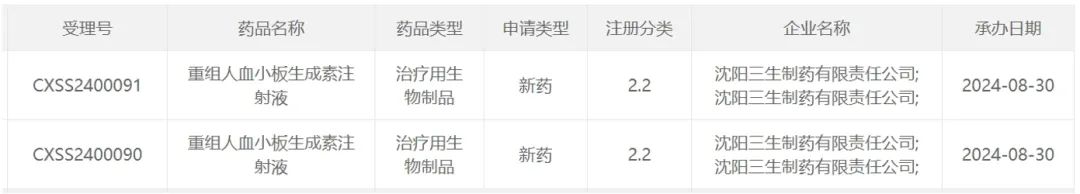
图源:CDE官网
三生制药加速新药研发与上市步伐
三生制药作为国内先进的生物制药企业之一,其自主研发的重组人血小板生成素注射液(特比澳®)已在中国市场上市多年,并广泛应用于治疗化疗引起的血小板减少症及免疫性血小板减少症(ITP)。此次新适应症申报的受理,无疑是对三生制药研发实力和市场洞察力的又一次肯定。
根据最新市场消息,三生制药在研发领域不断深耕细作,其丰富的研发管线涵盖了血液及肿瘤科、自身免疫性疾病、眼科、肾科、皮肤科以及代谢科等多个关键治疗领域,均有多项在研项目同步推进。截至目前,已有12款新药推进至临床3期或新药上市申请(NDA)申报阶段,其中特比澳®的新适应症申报更是备受瞩目。随着国家对创新药支持力度的不断加大和医药市场的持续扩容,三生制药有望在未来几年内实现更多新药的上市,进一步巩固其在生物制药领域的优势地位。
新适应症疗效显著,安全性良好
本次申报新适应症的临床研究数据充分展示了特比澳®在治疗慢性肝病相关血小板减少症患者中的卓越疗效和良好安全性。据三生制药此前公布的研究结果,一项旨在验证特比澳®在拟择期行侵入性手术的慢性肝病相关血小板减少症患者中维持围手术期血小板计数≥50×109/L效果的3期临床研究已圆满结束,该临床研究成功达成了其预设的主要终点。具体研究数据显示,接受特比澳?治疗的试验组患者在围手术期维持血小板计数达到或超过50×10^9/L的比例高达85.00%,相比之下,对照组的比例仅为12.50%。这一结果意味着试验组与对照组之间的应答率差值显著,高达67.90%。这一结果表明,特比澳®在提升患者血小板计数、降低手术出血风险方面具有显著优势。
此外,研究还显示,试验组与对照组在不良事件的发生率及严重程度上并无明显差异,进一步证明了特比澳®在慢性肝病相关血小板减少症患者中的安全性。对于这类患者而言,血小板减少是常见的并发症之一,不仅增加了手术相关出血事件的风险,还限制了其他治疗手段的应用。因此,特比澳®新适应症的获批上市,无疑将为这类患者提供更加安全、有效的治疗选择。
结语与期待
三生制药提交的「重组人血小板生成素」新适应症上市申请,不仅彰显了企业在研发领域的实力与成就,更是向广大患者传递了对其健康福祉深切关怀与坚定承诺的积极信号。随着医药科技的不断发展和政策的持续支持,我们有理由相信,未来将有更多像特比澳®这样的创新药物涌现出来,为各种疾病的治疗带来新的希望和解决方案。
参考文献:
1. 中国国家药监局药品审评中心官网.
2. 三生制药官网
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..