8 月 16 日,CDE 官网显示,阿斯利康在国内递交了度伐利尤单抗注射液的新适应症上市申请(JXSS2400066/7)。度伐利尤单抗是一款 PD-L1 抑制剂,此前已在国内获批 3 项适应症。Insight 数据库推测,该药本次申报的新适应症可能为:治疗新诊断的晚期高级别上皮性卵巢癌患者。
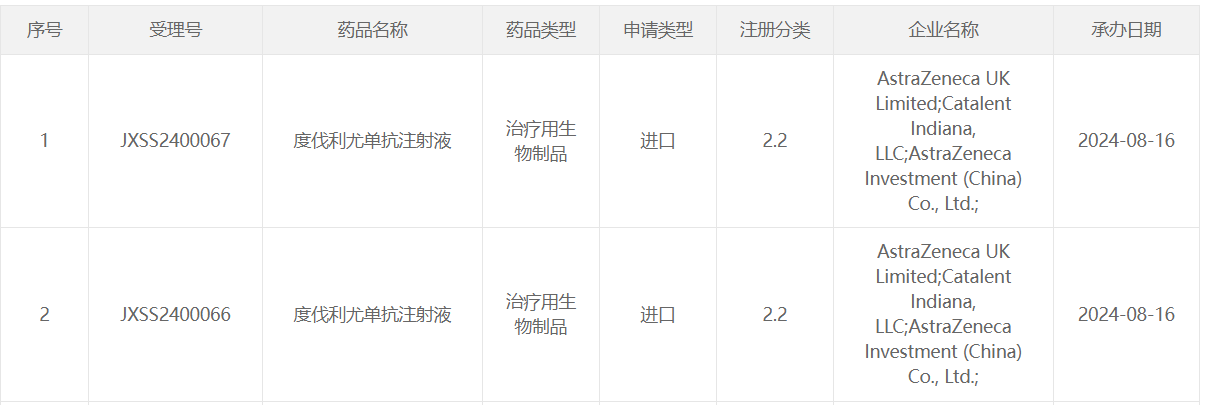
截图来自:CDE官网
度伐利尤单抗目前已在美国、日本、欧盟、中国内地等多个国家和地区获批上市。在国内,该药此前已获批 3 项适应症,分别用于治疗III 期非小细胞肺癌(2019 年 12 月获批)、广泛期小细胞肺癌(2021 年 7 月获批)、局部晚期或转移性胆道癌患者(2023 年 11 月获批)。
根据度伐利尤单抗正在开展的临床研究进度, Insight 数据库推测其本次申报的新适应症可能为:联合奥拉帕利、贝伐珠单抗和铂类化疗用于治疗新诊断晚期高级别上皮性卵巢癌(无肿瘤 BRCA 突变)患者。
在 2023 年 ASCO 年会上,阿斯利康曾公布了 DUO-O III 期临床研究中期分析结果。DUO-O 是一项随机、双盲、安慰剂对照的多中心 III 期研究,在中国、美国、德国、法国、日本等多个国家开展,旨在评估在初诊非 BRCA 突变的晚期卵巢癌患者中继度伐利尤单抗+含铂类化疗+贝伐珠单抗后予以度伐利尤单抗+贝伐珠单抗联合或不联合奥拉帕利维持治疗的疗效与安全性。
DUO-O III 期临床研究中期分析数据显示(NCT03737643、CTR20210499):
与化疗联合贝伐珠单抗治疗相比,奥拉帕利+度伐利尤单抗+化疗+贝伐珠单抗联合治疗可使疾病进展或死亡的相对风险降低 37%,中位 PFS 分别为 19.3 个月和 24.2 个月。
而在同源重组缺陷(HRD)阳性亚组患者中,与化疗和贝伐珠单抗单独治疗相比,奥拉帕利+度伐利尤单抗+化疗+贝伐珠单抗联合可使疾病进展或死亡的相对风险降低 51%,中位 PFS 分别为 23.0 个月和 37.3 个月。
在对 HRD 阴性亚组患者进行的探索性分析发现,与化疗和贝伐珠单抗治疗相比,奥拉帕利+度伐利尤单抗+化疗+贝伐珠单抗联合使用的疾病进展或死亡的相对风险降低了 32%,中位 PFS 分别为 17.4 个月和 20.9 个月。
在 2024 年 6 月举行的欧洲肿瘤学会妇科肿瘤年会 (2024 ESMO GC )上,研究人员又公布了 DUO-O III 期临床研究的更新数据。更新数据显示:
与对照组相比,在度伐利尤单抗 + 卡铂/紫杉醇 +贝伐珠单抗随后进行度伐利尤单抗+卡铂/紫杉醇+ 奥拉帕利维持治疗,可继续改善患者的 PFS。
在非 BRCA 基因突变 HRD+ 人群中,中位 PFS 为 45.1 个月,这是迄今为止在这些患者一线治疗中观察到的最长 PFS,并且具有相关的良好 OS 趋势。非 BRCA 基因突变 HRD+ 和非 BRCA 基因突变意向治疗人群(ITT)中的 PFS2 均有所改善。
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..