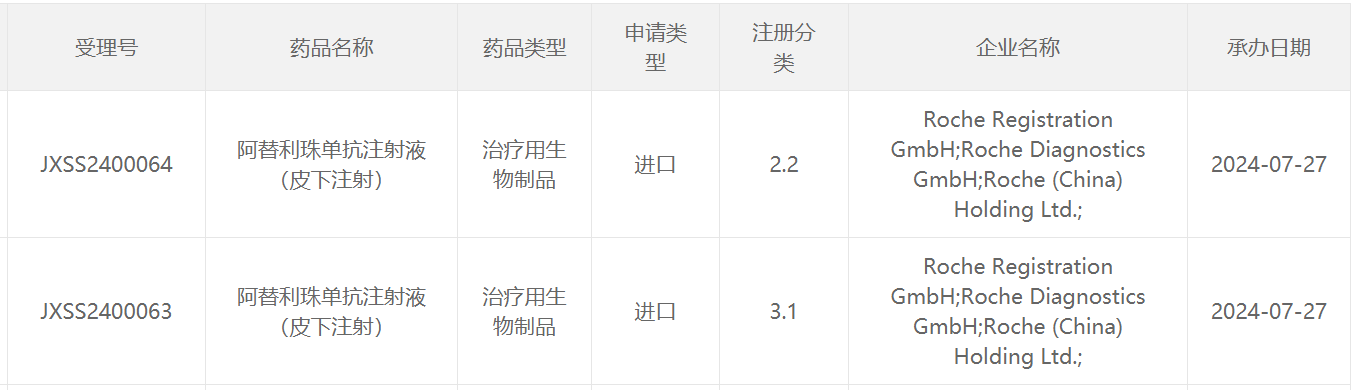
7月27日,中国国家药监局药品审评中心(CDE)官网公示,罗氏(Roche)申请的阿替利珠单抗注射液(皮下注射)上市申请已获得受理。公开资料显示,阿替利珠单抗是一款PD-L1抑制剂,此前已在全球范围内获批多项适应证。
本次申报上市的为该产品的皮下注射剂型。根据罗氏此前公开新闻稿介绍,皮下给药阿替利珠单抗可将每次注射的治疗时间缩短至4~8分钟(一般为7分钟),而标准静脉输注则需要30-60分钟。
根据中国药物临床试验登记与信息公示平台官网,罗氏正在开展一项国际多中心(含中国)1b/3期临床研究(IMscin001研究),旨在既往接受过治疗的局部晚期或转移性非小细胞肺癌患者中研究皮下注射阿替利珠单抗相比静脉注射阿替利珠单抗的药代动力学、疗效和安全性。
在该研究中,阿替利珠单抗注射液的给药方法为皮下注射,每三周一次。研究拟在中国入组58人,在国际范围内已入组371人。
本次,皮下注射阿替利珠单抗在中国申请上市,意味着该产品的皮下注射剂型也有望在不久的将来惠及中国患者。
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..