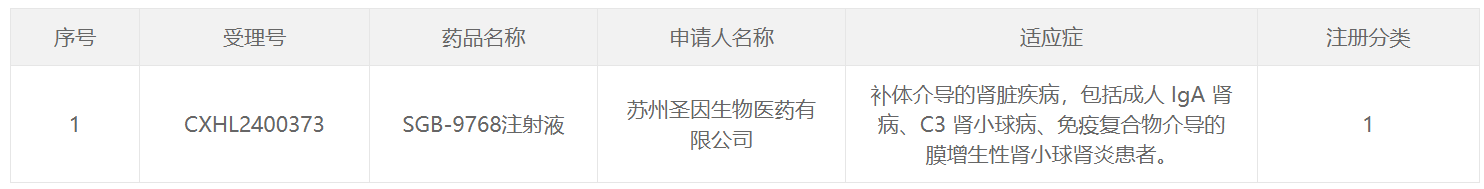
截图来源:CDE官网
补体在人体内发挥着重要的免疫和生理功能,然而,补体调控异常或过度活化会诱导炎症并破坏自身组织,与部分血液学、眼科学、肾脏学等领域疾病的发生发展密切相关,例如年龄相关性黄斑变性、重症肌无力、阵发性睡眠性血红蛋白尿、非典型溶血尿毒综合征、C3肾小球病、IgA肾病、血栓性微血管病等。
补体系统包含30多种可溶性蛋白、膜结合蛋白和补体受体成分。其中,补体C3含量较高,也是所有补体激活通路的共同途径成员,因此成为颇有潜力的疾病治疗靶点。
根据圣因生物新闻稿介绍,SGB-9768是一种靶向补体C3的siRNA-GalNAc结合物,采用了该公司创新技术递送到肝脏细胞,通过RNAi抑制肝脏C3的合成。临床前研究数据显示,该产品能有效并持续地减少C3合成。GalNAc递送siRNA药物的安全性、有效性、稳定性已得到大量数据验证。此外,SGB-9768可实现每3个月或6个月给药一次的频率,具有治疗频率较低、患者依从性好、药效持久的优势。
圣因生物此前新闻稿表示,SGB-9768是该公司在免疫相关疾病领域首个获批进入临床阶段的候选药物,也是该公司第2款进入临床研究阶段的siRNA药物。该公司靶向肝细胞PCSK9的siRNA疗法SGB-3403此前已经在中国和澳大利亚进入临床试验阶段。此外,今年5月,圣因生物与信达生物共同开发的用于治疗高血压的siRNA药物SGB-3908注射液也已经在中国申报临床。
参考资料:
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..