5 月 28 日,据 CDE 官网显示,博安生物度拉糖肽注射液(BA5101)上市申请已获受理,用于成人 2 型糖尿病患者的血糖控制。
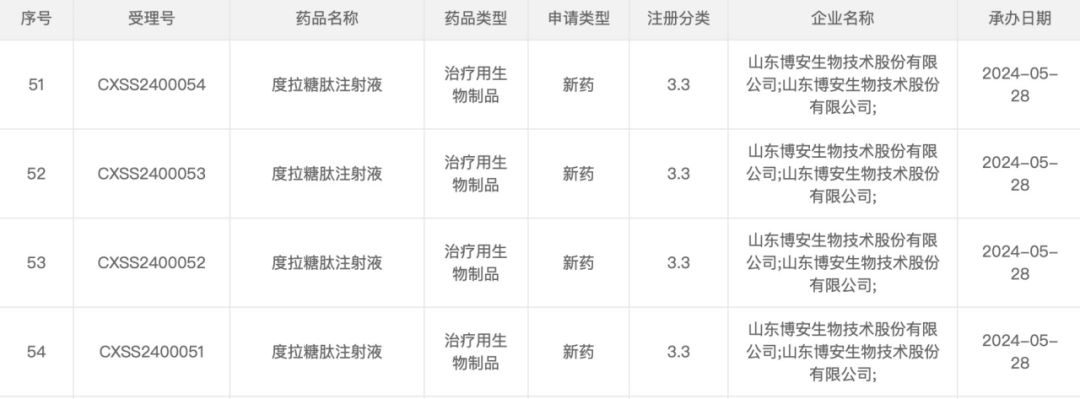
截图来自:CDE官网
糖尿病不仅是发达国家的「富贵病」,包括中国在内的发展中国家也面临重大负担。根据国际糖尿病联盟(IDF)最新数据显示,中国是全球糖尿病患者最多的国家,患者数量占全球的四分之一以上,预计到 2045 年将增至 1.74 亿人。度拉糖肽注射液此次申报上市获受理,是应对这一严峻公共卫生挑战的重要一步。
度拉糖肽是一种长效胰高血糖素样肽-1(GLP-1)受体激动剂。与其他降糖药相比,度拉糖肽能够改善胰岛 β 细胞功能,稳定且有效地降低血糖及糖化血红蛋白(HbA1c)水平。此外,其独特的作用机制不易引起低血糖,还能降低体重、血脂和远期心血管疾病风险,并对肾脏有保护作用。每周给药一次的方式还减少了患者的服药负担,提高了用药依从性。
目前,BA5101 从临床前研究到临床阶段的试验已顺利完成,成为全球首个完成 Ⅲ 期临床试验的度拉糖肽生物类似药。
在中国男性受试者中进行的 Ⅰ 期临床试验证实,BA5101 与原研药物在药代动力学(PK)特征、安全性和免疫原性方面高度相似。
在中国成人 2 型糖尿病患者中进行的随机、开放、平行、阳性对照 Ⅲ 期临床试验表明,BA5101 能够快速、稳定地降低血糖和糖化血红蛋白,其疗效和安全性与原研药物一致。
查询 Insight 数据库得知,目前全球有 9 款在研的度拉糖肽注射液生物类似药,BA5101 是中国首款申报上市的产品。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..