近日,E药经理人发布“2023中国医药创新企业100强”榜单。先声药业入选,并跻身创新第一梯队。近年来,先声药业运用“自研+BD”双轮驱动加协同创新模式,创新药收入占比从45%到超过70%,成为国内传统药企创新转型最快的公司之一。先声做对了什么?
过去数年,不管是跨国药企还是中国的传统制药公司,都面临着一种类似的困境,希望能获得穿越产业周期和自身核心产品周期的能力。为此,跨国药企正想尽办法,比如辉瑞凭借自身的BD实力力挽狂澜、获得进入创新下一程的筹码;诺和诺德凭借临床开发实力发掘处女地,顺势完成产品迭代……而对国内传统药企来说,则在由仿入创的过程中努力前行,并着力于打造自己的差异化优势。
总体看这些“渡劫”成功者,往往是集中资源将过往沉淀的优势发挥到最大,先声药业正是国内的领先者。转型节奏快、创新成色好,让先声在一众国内传统药企中脱颖而出,成为业内运用“自研+BD”协同创新转型最快的公司之一。
一般来说,行业判断制药公司创新转型程度主要有两个指标:一是创新药收入占比;二是研发管线的创新程度。而一个制药公司的“创新指数”包含三个维度:创新药收入占比、研发投入占比、在研管线核心产品的市场峰值。两个指标有一个交集:创新药收入占比,这一直观数据被广泛用于评价、判断一家制药企业的“创新成色”,而目前国内绝大多数企业不超过50%(被看作创新驱动的临界值)。
2020年先声药业于港交所上市时,因为当时创新药收入占比只有45%,港交所拒绝先声药业招股书中“我们是一家创新药企”的表述,要求必须修改为“我们是一家仿制药为主的制药企业”。随后的2021年,先声药业创新药收入占比首次突破50%,并在2023上半年达到71.4%。在2023年中期业绩报告中,先声药业终于可以自信地写上“本公司是一家创新与研发驱动的制药企业”。
从45%到71.4%,这是一个不可小觑的成绩,需要诸多资源协调运转方可实现。
首要是创新,自主创新和外部创新,缺一不可。其次是创新药的商业化能力和临床开发能力,这是保障,也直接关系到创新成果的快速转化与成果。三年里,先声药业先后推动了先必新、恩维达、科赛拉、先诺欣四款创新药上市,并且自研上市的先必新已成为20亿元单品,其余3款合作创新药也都在上市当年成为销售数亿的品种。资本寒冬下,这些突出的能力,使得先声成为更多Biotech 公司优选的合作伙伴。
在创新转型赛场中,先声做对了什么?先声的下一站又在哪?
迭代:自研再向前,BD能力凸显
成立于1995年的先声,前七年的基本形态是“总经销总代理”的商业化运营为主。随后必存(2003年上市)、恩度(2006年上市)两个产品改变了先声的发展轨迹,让先声药业意识到了自主研发和一个好产品的意义和价值。之后先声发起了一系列围绕创新的变革,进入了全新的赛道,艾得辛和先必新陆续上市,且在先声既往商业化能力的沉淀下都取得了不错的市场表现。
将优秀的基因迅速复刻并放大是先声擅长的,在商业化上如此,研发创新亦如此。在十多年自主研发的过程中,先声不仅积淀了相关能力,还拥有了一套“如何评价和判断一个创新药项目是否适合先声、引进后如何快速推进、上市后如何快速上量”的方法论,这让先声在寻求BD合作的时候,有了属于自己的独特判断力。
事实上,BD能力强,并不意味着一家制药企业缺乏创新力。一项可靠的数据是,全球TOP10药企的管线几乎半数以上都依赖于外部创新,辉瑞甚至达到80%。当下,BD已经成为获得产品、扩建管线最为快速的方式,是药企构建创新能力的“第二能力”,也成为创新竞争的“第二战场”。
时间往前追溯4年,彼时的2019年国家带量采购政策刚刚开展,创新药尚处于爆发前期,凭着对行业的敏感以及一直根植于心的危机感,任晋生意识到“先声的创新转型必须要坚定更坚定、快点再快点”。这一年先声在保持内部研发投入力度的同时,大幅增加了对BD的投入。据统计,当年先声与海外创新公司达成了4笔FIC/BIC潜力创新药的早期交易。此后,先声一直活跃在国内生物医药领域BD交易的一线。
也许,这组数字能更直观地呈现先声的决心。2022年先声研发投入达到17.28亿元,排在国内创新药研发的TOP10。从相对值来看,自2020年以来,先声每一个完整年度的研发费用率都超过了25%,最高到28.3%(2021年),完全媲美研发实力强的跨国药企(如再生元等)。据统计,2021年全球TOP10药企里研发占比的中位数为20%。
有了决心和投入,还要找到对的人。除了丰富的行业从业经验外,“多元化”也是先声研发和BD管理团队的标签之一。其中包含先声药业执行董事唐任宏(此前曾在诺和诺德、阿斯利康任职),首席投资官周高波(此前担任麦肯锡全球合伙人)等,研发和BD彼此协同,团队成员和视野覆盖全球主要生物医药产业创新高地。
基于上述努力,先声的研发管线从2020年仅有10项I期临床,目前已迅速发展为正就19种创新药开展临床研究,其中处于NDA/关键临床阶段候选药物3种,I/II期阶段候选药物11种、临床前候选药物约40种、研发管线超60项的规模。这些管线聚焦于肿瘤、神经系统、自身免疫及抗感染领域,梯度合理,可以保证先声未来一段时间内每年有一个以上创新药/新适应症上市或获批。
坚定:好项目的核心是“更有效和差异化”
先声是最早有意识通过协同创新快速构建创新药管线的Pharma之一。因为出发早、投入大、执行力强,协同创新成果对其贡献正日益凸显。
在具备了所有的内外部因素后,还需要一个坚定不移且行之有效的策略。先声要求将“聚焦更有效,坚持差异化”作为核心要求,拒绝同质化竞争;另一面,BD创新要与聚焦领域的已上市产品/在研管线相互补充,或者产生协同效应。这两点说来容易,但落到执行却很难。很多Biotech往往会进入以纯技术为导向的误区,从而忽略峰值销售或者赛道的拥挤,而这两者直接关系到产品的商业价值。
在先声看来,“产品立项不能单纯以技术为导向,要以市场为导向,要能帮助到更多患者。当然科学也很重要,只有差异化才能覆盖更广泛的患者群体”。据一份公开资料,先声的BD策略中,针对早期(临床前/I期)管线产品,先声主张深刻理解疾病生物学机制,考虑其是否能与自研管线PK,风险获益是否可控,以及能获得的权益范围;针对后期(II期/III期/NDA)管线产品,则更关注标的产品是否与公司专注的疾病领域协同、竞争位置是否靠前,以及是否具备差异化优势和高商业价值(峰值>15亿元)。
值得关注的是,先声的开放式创新正在越来越多元。任晋生认为,创新不仅是分子结构的创新,合作模式和管理也要创新,核心是面对一个个“陌生”,未来会以多种合作形式并存。近两年,先声BD的重心发生了两个转变:一是增加了对国内创新项目的引进,或者直接负责商业化国内Biotech公司即将上市产品;二是更重视产学研的转化。据先声药业官网,公司已经和中国药科大学、清华大学、美国麻总百瀚(顶级医疗机构)等达成FIC/BIC新药的合作,持续扩充研发管线。
通过协同创新策略,先声在短时间内收获了兼顾质量和创新的差异化产品。不管是全球首个在化疗前给药并具有全系骨髓保护作用的CDK4/6抑制剂科赛拉,还是全球首款可皮下注射的PD-L1抑制剂,也是国内首个泛瘤种适应证的免疫治疗药物恩维达;抑或是首款国产自研的3CL靶点抗新冠药先诺欣,都在短期内成为先声创新药组合的一员。
在先声近60条创新药研发管线里,亟待兑现的“更有效和差异化”高潜新药更多。比如新一代抗失眠药达利雷生,去年11月引进,有望在2024年递交NDA,该药物是目前唯一被欧洲药品管理局批准改善日间功能的DORA类失眠药物,上市后将成为先声药业神经系统创新药的有力补充;以及苏维西塔单抗(新一代重组人源化抗血管内皮生长因子单克隆抗体)等等。
在有了好的产品后,现在,接力棒就交到了先声最擅长的环节:商业化。
练兵:不仅仅是商业化
不是所有药企都能做好协同创新,无论是Biotech,还是传统的制药公司。产品的“好”是基础,更需要强的商业化能力保障产品的价值得到最大化释放。这也是药企依赖协同创新成功转型的关键。
先声的独特在于,在创新转型过程中他多年沉淀下来的商业化能力得到了同步“进化”。这一能力在其自主研发的新药先必新上得到验证,并发挥得淋漓尽致。
于先声而言,先必新不仅是一个辉煌的案例,更是有着战略意义的产品,帮助其渡过新旧产品交替期,并成为先声打造神经领域优势地位的重要一环。
据了解,先必新于2020年7月获批上市,从获得批件到发货仅用时13天,从首次发货到全国覆盖仅用时80小时;获批5个月后纳入医保目录,成为进医保最快的创新药之一;进院时,利用既有在中枢神经系统的市场积累,快速覆盖核心医院,据披露其在2023年上半年已经惠及患者约56万人,覆盖超过4200家医疗机构。
2022年底,先必新的销售额已经超过了20亿元,距离拿到上市批件仅仅两年多时间,创下同类创新药纪录。中信证券预计,该产品销售峰值有望达50亿元。
如果说先必新证明了先声药业“自研+自销”的能力,那么恩维达(PD-L1)则是先声与Biotech协同创新、取得双赢的典型案例。恩维达自2021年11月底获批,销售迅速起量。从思路迪的数据来看,2021年至2022年,该公司营收分别为6026万元、5.67亿元,一年增幅超过8倍,其中离不开恩维达的贡献。今年1-6月,恩维达又实现销售3.5亿元。在竞争激烈的PD-(L)1市场,这样的商业化表现相当难得。
在这波浪潮里,先声还迭代了一个难得的能力——临床能力。众所周知,创新药的临床开发能力是所有药企通往创新的Big Pharma之路不可或缺的一项,但对国内众多药企来说仍是短板,尤其是传统的制药公司,临床效率的提升非常艰难。
曲拉西利的快速上市,正是先声临床实力和市场准入能力的综合体现。2022年7月12日,曲拉西利(科赛拉)在中国附条件获批,距离美国首次上市仅仅17个月,开发速度在业界遥遥领先。据统计,2019-2021年,在中国交易总金额前100位的合作引进创新药产品中,曲拉西利上市开发速度位列第一。
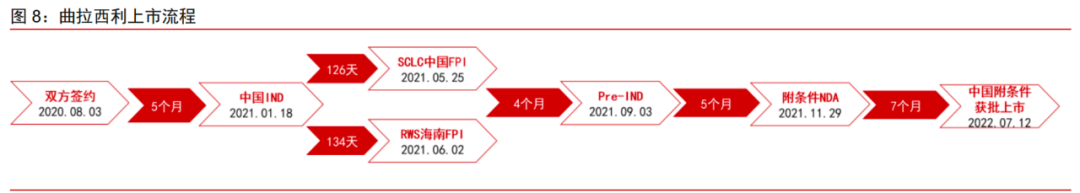
来源:中信证券
成功结果的背后,离不开临床方案的充分讨论与设计。据了解,曲拉西利的上市同时利用了3项不同的临床试验数据:III期安全性导入阶段数据+博鳌真实世界研究数据+境外数据。这一模式后来也应用到达利雷生的临床当中,并被行业广泛借鉴。
更离不开先声临床团队的超强执行力。先诺欣是证明后者的又一个显著案例。一般来说,生物医药光是临床阶段就需要3~6年,但先诺欣自获得IND到附条件获批上市仅仅用时10个月,虽然这个过程有新冠疫情国家急需相关药物的特殊性,但是先诺欣能成为国内首个获批的3CL靶点国产口服新冠药,自然有其核心能力和优势。
此外,先声还借助BD产品深度参与到全球临床开发中,建设全球化的临床能力。继SCLC适应证后,先声与G1 Therapeutics密切合作,负责全球大型临床试验的中国患者,入组人数相比国内单独开展的大型临床更少,临床推进速度和经济效率更高;同时与G1 Therapeutics的全球前沿开发计划维持同步,更快将更多适应证推向商业化。目前,先声药业已经开始了先必新和先必新舌下片两个产品的美国临床工作。
在一次又一次BD合作中,先声完成了创新药临床能力和商业化能力的“练兵”,这两种能力已经逐步内化为先声护城河的核心组成部分。
革新:向国际化进发
一切看起来都很顺利,但是如果你问任晋生,先声的创新转型成功了吗?他会坦诚地回答:还在路上。
任晋生认为,创新转型说到底,本质上还是团队的转型,人的能力、知识、理念的转型。原来的公司如果100%或者80%都是仿制药,那他的知识、能力、经验都是围绕仿制药建立的,从仿制到创新,高管团队、中层管理人员和研发人员,人员结构都要做很大的改变。
过去数年,先声依此逻辑对产品到人员结构进行了持续迭代,这场自上而下的全系统革新只有两个目标:创新、国际化。
完成创新转型并不是先声的终点。任晋生认为,创新转型成功的标准应该是,制造出除了在中国市场,还在海外市场成功上市,并且有足够规模的创新产品。如果是冷门产品,帮助的患者不多,也谈不上成功。
如今,先声的团队,尤其研发团队创新含量和国际化含量都很高。截至上半年先声已建立超过1000人的研发团队,其中硕士和博士人才比例大幅提高,超过了60%,海外背景人才已超过10%。同时,诸多创新药经验丰富、多元背景的高管团队加入先声。
先声要出海,更要有节奏、有策略的出海。先声的国际化先从合作和研发开始。要想真正“走出去”,还是要先站稳中国市场,再考虑外部合作,包括License in/out,都是国际化的一部分。比如现在产品一般在美国、欧洲完成了二期临床,三期是全球多中心,中国公司可以在不同的阶段参与进去,学习他们的能力,锻炼自己的团队。至于真正建立全球商业化能力,还需要时间的积累。
他还透露,未来先声将继续在上海,南京,北京和波士顿四个创新中心加大投入。海外方面,将在现有的波士顿创新中心的基础上,从临床研发和合作研发开始扩大布局。
现在的先声,无论是从创新药收入占比上,还是从研发投入、创新人才上,创新进展都可圈可点,出海的种子也已播下。
今年以来,大家越发感受到成熟稳重的Big pharma的创新韧性,行业也正从刚设立时的新鲜和火热开始慢慢走向稳重和成熟,时代和Big pharma在慢慢靠拢,这也使得他们开始迎来自己的高光时刻。
关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..