10月11日,默沙东启动了肿瘤新抗原mRNA疫苗V940(mRNA-4157)的第二项III期临床试验(V940-002)。第一项III期临床试验已于今年7月启动(见:默沙东启动肿瘤mRNA疫苗+K药首个III期临床)。

该研究旨在评估mRNA-4157联合帕博利珠单抗(Keytruda,K药)对比安慰剂联合K药辅助治疗完全切除II期、IIIA期、IIIB期非小细胞肺癌(NSCLC)患者的有效性和安全性。

该研究拟纳入868例NSCLC患者,预计于今年11月启动并于2030年6月完成。试验组患者需接受至多9剂次mRNA-4157(肌肉注射,每3周1次)和至多9次K药(静脉注射,每6周1次)治疗。研究的主要终点为无疾病生存期(DFS)。
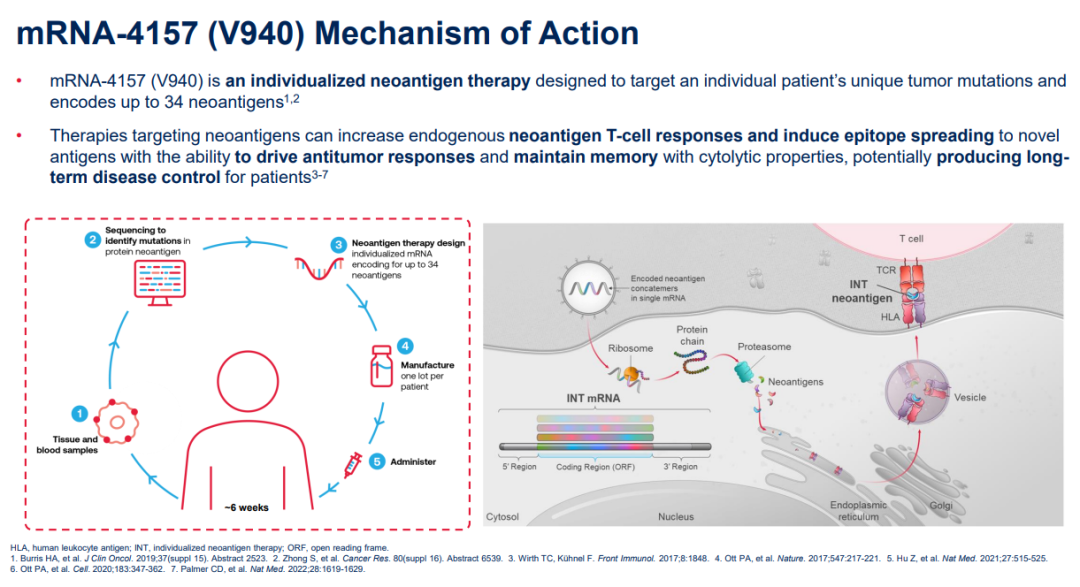
mRNA-4157是Moderna针对每个癌症患者的独特肿瘤突变开发的一款个性化肿瘤新抗原疫苗,可以增强T细胞对内源性新抗原的免疫应答以及诱导肿瘤表位扩散至能够驱动抗肿瘤反应的新抗原。
来源:Moderna官网
mRNA-4157的制备过程需耗时约6周,包括肿瘤组织和血样提取、测序鉴定蛋白新抗原突变、设计表达新抗原(多达34种)的mRNA序列和生产这4个步骤。
2016年6月,默沙东豪掷2亿美元首付款投资Moderna开发mRNA-4157。2017年8月,mRNA-4157第一次进入I期临床(KEYNOTE-603)。两年后,Moderna传来积极结果,至少接受1剂次mRNA-4157(0.04-1.0mg)和K药治疗的20例实体瘤患者中,有6例实现客观缓解。
2020年11月,KEYNOTE-603研究的HPV-头颈部鳞状细胞癌亚组也取得了积极的进展。在10例接受联合治疗的患者中,5例实现客观缓解,PFS达到9.8个月,数据相比以往K药单药治疗组好(14.6%客观缓解,PFS仅2.0个月)。
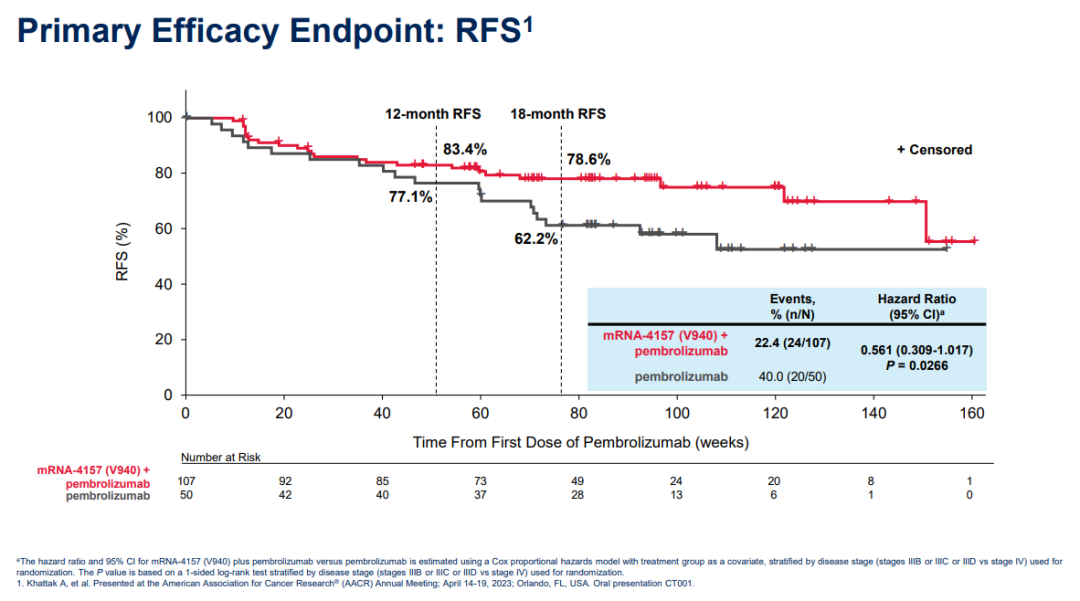
2022年12月,默沙东宣布mRNA-4157联合K药辅助治疗完全切除的III/IV期黑色素瘤的IIb期研究(KEYNOTE-942)达到无复发生存期(RFS)主要终点,可显著降低患者44%的复发或死亡风险。基于该研究结果,FDA于今年2月授予该联合疗法突破性疗法资格,EMA于今年4月授予其优先药物(PRIME)资格。
来源:Moderna官网
可以说,mRNA-4157一路走来顺风顺水,经费有默沙东支撑,疗效数据也没翻车过,给mRNA疫苗的肿瘤应用前景带来了不少积极的信号。
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..