今年可以称得上是NASH药物开发的元年,在近期的新药研发报道上,已经有很多的产品进入到了NDA阶段,近几十年来各大药企的研究几乎只轮不反,NASH药物的研发任务可以称得上艰巨,不仅仅是各大药企的挑战之一,同时也是医学的短板!在全球制药企业的攻坚克难下,40年的研究将重睹天日!
Madrigal Pharmaceuticals近日宣布,美国FDA已接受其在研药品resmetirom治疗伴有肝纤维化的非酒精性脂肪性肝炎(NASH)成人患者的新药申请(NDA),并授予优先审评资格。FDA预计于2024年3月14日前完成审评。
01
Resmetirom破釜沉舟
Resmetirom(MGL-3196)是一种每日一次、口服、甲状腺激素受体(THR)-β选择性激动剂,旨在靶向NASH的关键基础病因。甲状腺激素通过激活肝细胞中的β受体,在肝功能中发挥核心作用,影响从血清胆固醇、甘油三酯水平到肝脏中脂肪病理性积聚等一系列健康参数。
公司为resmetirom设计了四项III期临床试验,即MAESTRO-NASH、MAESTRO-NAFLD-1、MAESTRO-NAFLD-OLE和 MAESTRO-NASH-OUTCOMES,用于证明其治疗 NASH 的安全性和有效性。Resmetirom已被证明安全性和耐受性良好,对THR-α受体无活性,不会影响骨骼或心脏参数,以及不会影响甲状腺轴激素。
同时在2023年4月,resmetirom被美国FDA授予治疗伴肝纤维化的NASH成人患者的突破性疗法认定。
MAESTRO-NASH是一项多中心、随机、双盲、安慰剂对照的临床研究,旨在研究Resmetirom对经肝活检确认的NASH患者的治疗效果。该试验设计的部分目的是支持加速批准药物,该研究批准招募超过1000名经肝活检确认的NASH肝纤维化患者,这些患者将按照1:1:1随机分成三组并分别接受每日一次服用80mg。
在2022年12月,Madrigal宣布 Resmetirom的两种每日口服剂量均达到了MAESTRO-NASH主要终点。
Resmetirom在80毫克和100毫克两个剂量下,安全且耐受良好,与之前的II期和III期临床数据一致。
MAESTRO-NAFLD-1研究主要针对NAFLD人群开展,以安全性作为主要研究终点,同时设置包括肝脏脂肪含量(MRI-PDFF)及血脂、非侵入性检测(NITs)改变等作为次要终点;
根据2022年1月公布的研究数据,结果根据评估显示,接受剂量为100 mg的resmetirom治疗52周后,患者肝脏脂肪水平平均降低51%。肝纤维化、肝脏体积和脾脏体积也显著降低。同时LDLc血脂水平显著改善。在安全性上,近1000例患者接受每日80 mg 或100 mg resmetirom治疗52周,安全性和耐受性良好。
02
MEASTRO-NASH 三期临床试验
两个给药组达到52周主要终点NASH消减的比例分别为26%及30%,安慰剂组为10%;两个给药组达到52周主要终点纤维化改善的比例分别为24%及26%,安慰剂组为14%。在关键次要终点上,80 mg给药组在24周的LCL-C平均改变为 -12%,100 mg组为 -16%,而安慰组的改变为平均1%。与安慰组相比,所有给药组的指标都有统计学意义 。
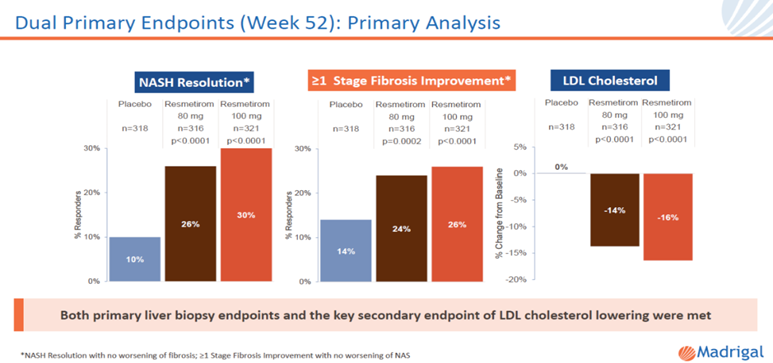
▲Resmetirom在关键性3期临床试验中的主要终点数据(图片来源:Madrigal公司官网)
03
NASH的攻克之路
一个世界性的卫生保健问题,也是一个日益严重的流行病。非酒精性脂肪性肝炎(NASH)是非酒精性脂肪肝病(NAFLD)的更高级形式。是一种与胰岛素抵抗和遗传易感密切相关的代谢应激性肝损伤,表现为5%以上的肝细胞脂肪变合并小叶内炎症和肝细胞气球样变性。NASH是导致肝硬化的主要原因之一, 据估计,全球超过 20%的成年人患有NAFLD,NASH患者10~15年内肝硬化发生率高达15%~25%。

来源:凯莱英药闻
其特点是通过新的脂肪生成在肝细胞中积累甘油三酯。摄取葡萄糖和游离脂肪酸(FFAs)并将其纳入脂质合成途径,从而促进了脂肪生成。且经常合并其他代谢性的疾病,比如肥胖,高血糖,胆固醇,高血压等。这些疾病也进一步增加了患心血管疾病的风险。运动和饮食是目前治疗非酒精性脂肪肝的标准方法,但是依从性仍然是一大难题!配合性的治疗可能达不到标准,从而治疗效果也会大打折扣。
04
非酒精性脂肪肝发病机制
非酒精性脂肪肝(NAFLD)是一种渐进性疾病,开始是简单的脂肪变性(非酒精性脂肪肝(NAFL)),并可演变为更复杂的形式,即非酒精性脂肪肝炎(NASH),其特点是脂肪变性、饱和脂肪酸(SFAs)的积累、果糖摄取量增加导致的新脂肪生成的增加。促进了肝脏炎症以及受压肝细胞的死亡,这些肝细胞还释放促炎症介质,如ATP、细胞外囊泡和趋化因子,进一步强化了炎症过程并导致纤维化的发展。如此恶性循环从而促使向肝硬化过渡进一步发展为肝硬化,并在某些情况下发展为肝细胞癌(HCC)。
据不完全统计,全球NASH患病人数从2016 年的3.1 亿人已上升到2020 年的3.5 亿,四年间增长了4000多万人。2021-2030 年,全球NASH患病人数将持续增长,预计2030 年将达到4.9 亿人。中国NASH患病人数2020 年已达到3870 万人,2021-2030 年,中国的NASH患病率将以更快的速度增长,预计2030 年将达到5,550 万人。
NASH机制进展至“多重平行打击”理论,风险因素包括胰岛素抵抗、慢性炎症、纤维化、免疫和肠道菌紊乱,氧化应激、激素失调等,涉及肝脏、肠道和脂肪组织中的各种细胞。研发主要针对三种不同的致病过程——脂肪变性、炎症和纤维化,从致病源种延伸出四种不同的治疗路径:
(1)针对代谢靶点,改善对胰岛素的敏感性,抑制参与脂肪生成的酶;
(2)针对炎症或细胞损伤靶点,抑制炎症细胞募集或阻断验证信号传导;
(3)靶向肝-肠轴,调节胆汁酸肠肝循环和信号传导;
(4)直接针对肝星状细胞的抗纤维化靶点,减少肝脏中胶原蛋白沉积。
截至目前为止,NASH药物研发治疗领域仍然是仍然处于短板区域。FDA还没有正式批准用于治疗的NASH药物,用于治疗非酒精性脂肪肝炎的药物除了在印度获批上市的Saroglitazar 外,其余700+药物均处于临床前或临床研究阶段。其中有超过两百个项目仍然处于临床开发阶段。
且用于治疗 NASH 的主要临床研究药物均为小分子化药,另外,也有少量合成多肽、单克隆抗体、融合蛋白以及siRNA 类药物等。
随着创新的业务逐渐走向商业化,全球非酒精性脂肪肝病市场规模也是逐渐增长。据弗若斯特沙利文报告,预计2030 年将达到322 亿美元;中国NASH市场规模也将达到355亿元。
同时印度药企Zydus-Cadila Group开发的Saroglitazar magnesium是全球唯一获批上市的NASH治疗药物,但该药物仅在印度获批上市,美国尚未批准用于治疗NASH的药物上市。
以下是NASH适应症处于III期以上的在研药物

来源:凯莱英药闻
从靶点来看,包括FXR、FGF21、GLP-1R、PPAR、ASK1、THR-β等。其中比较热门的靶点当属THR-β激动剂!
05
THR-β激动剂道阻且长
THR-β在肝脏中高度表达,且THR-β激动剂被证实在人体中具有降低低密度脂蛋白(LDL)、甘油三酯(TG)和肝脏脂肪变性的活性。通过促进脂肪酸的分解和刺激线粒体的生物发生,THR-β有助于减少脂肪毒性并改善肝功能,进而减少肝脏脂肪。
06
THR-β激动剂作用机制

来源:药闻窗
THR-β(甲状腺激素受体β亚型)在人体肝脏中高表达,能够调节脂代谢,降低LDL-C、甘油三酯和致动脉粥样硬化性脂蛋白。同时,THR-β可以通过促进脂肪酸的分解,从而减少脂肪毒性并改善肝功能。进而减少肝脏脂肪。
而NASH患者肝脏的THR-β功能会弱于健康人,从而也加重了线粒体功能异常和脂肪毒性。
因此,THR-β激动剂具备单药调控多种肝脏通路来治疗NASH的潜力,包括:
1.调控脂肪合成
2.调控脂肪酸氧化作用
3.调控胆固醇代谢,
4.调控线粒体功能,
5.通过抑制TGF-β信号通路发挥抗炎和抗纤维化作用。
据不完全统计,目前在研的THR-β激动剂约40余种。
结语
这也不难怪在业内的人士戏称,“NASH的研发难于上青天。”也正是因为发病机制的复杂性,从而难以在新药的疗效上和安全性赋予它更强大的性价比。再加上药监局对新药的临床实验,重点的评判标准是较为严格,导致在过去的几十年中已经有上百款的NASH新药研发走向失败。其中也不缺乏有实力的巨头药企,也在NASH上栽过跟头!目前对NASH的研发也是投入了不少的人力物力,也希望各大药企能够奋勇争先,啃下这块硬骨头!
资料来源:1.公司官网
2.《NASH新药有望明年第一季度诞生!THR-β激动剂Resmetirom上市申请获FDA优先审评》
3.《非酒精性脂肪肝炎-NASH》
4.《肝脂肪降低51%!潜在首款NASH疗法获FDA优先审评资格》
5.《NASH新药有望明年第一季度诞生!THR-β激动剂Resmetirom上市申请获FDA优先审评》
四川省医药保化品质量管理协会关于2026
各会员单位: 当前,制药行业正..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会举办2026
持续提升合规 智慧拓建高质 四川..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..