8月17日,中国国家药监局药品审评中心(CDE)官网公示,和黄医药申报的沃利替尼片拟被纳入突破性治疗品种,针对的适应症为特定的胃癌或胃食道连接部腺癌患者。公开资料显示,这是和黄医药开发的MET抑制剂赛沃替尼(沃利替尼为曾用名),此前已在中国获批治疗非小细胞肺癌。
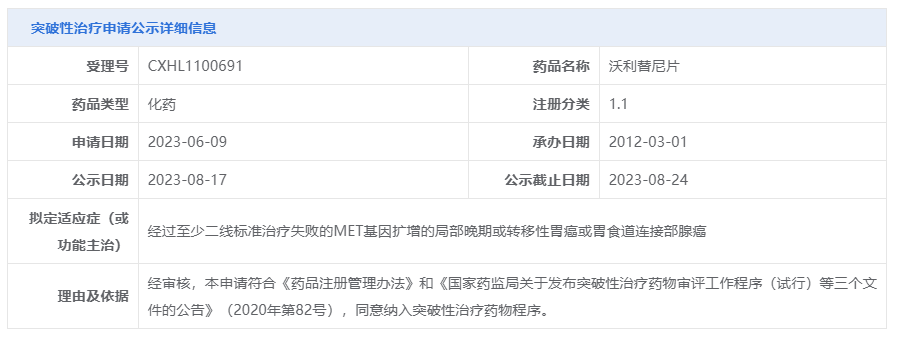
截图来源:CDE官网
根据和黄医药公开资料,赛沃替尼(savolitinib)是一种强效、高选择性的口服MET酪氨酸激酶抑制剂,在晚期实体瘤中表现出临床活性。该药可阻断因突变(例如外显子14跳跃突变或其它点突变)、基因扩增或蛋白质过表达而导致的MET受体酪氨酸激酶信号通路的异常激活。2021年,赛沃替尼在中国获批上市,用于治疗接受全身性治疗后疾病进展或无法接受化疗的MET外显子14跳跃突变的非小细胞肺癌患者。值得一提的是,和黄医药已与阿斯利康(AstraZeneca)达成合作,共同开发赛沃替尼并促进其商业化。
目前,赛沃替尼正作为单药疗法或与其他药物的联合疗法,开发用于治疗包括肺癌、肾癌和胃癌在内的多种肿瘤类型。本次拟纳入突破治疗的临床试验申请针对的适应症为:经过至少二线标准治疗失败的MET基因扩增的局部晚期或转移性胃癌或胃食道连接部腺癌。

2023年4月,和黄医药宣布已启动赛沃替尼在中国用于治疗伴有MET扩增的胃癌患者的2期临床试验。这是一项单臂、多中心、开放标签的2期注册研究,旨在评估赛沃替尼用于治疗伴有MET扩增的胃癌和胃食管结合部(GEJ)腺癌的疗效、安全性和耐受性。研究的主要终点为独立审查委员会(IRC)评估的客观缓解率(ORR)。次要终点包括无进展生存期(PFS)、各种不良事件的发生率等。
在2023年召开的美国癌症研究协会(AACR)年会上,和黄医药公布了赛沃替尼单药治疗伴有MET扩增的晚期或转移性胃癌或胃食管结合部腺癌患者的2期研究的初步疗效和安全性数据。试验数据显示,截至中期分析时,QD(每天一次)方案入组了20例患者。平均相对剂量强度为93.07%。中位暴露持续时间为2.09个月。经IRC确认的ORR为45%,在16例MET高表达患者中达到50%,而在4例MET低表达患者中仅观察到1例部分缓解(PR)。4个月时的缓解率持续时间为85.7%,中位随访时间为5.5个月。
安全性方面,最常见的≥3级的治疗相关不良事件(TRAE)为血小板计数降低、超敏反应、贫血、中性粒细胞减少和肝功能异常。在所有患者中,仅1例患者因4级肝功能异常停止治疗,无患者因TRAE死亡。
研究认为,赛沃替尼单药治疗在MET扩增的胃食管结合部腺癌或胃癌患者中具有可管理的安全性,并显示出良好的疗效,尤其是在MET高表达的患者中。研究人员正在开展BID(一日两次)方案,以进一步评估赛沃替尼在MET高表达患者中的疗效和安全性。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网. Retrieved Aug 17, 2023, from https://www.cde.org.cn/main/xxgk/listpage/da6efd086c099b7fc949121166f0130c
[2]和黄医药在与国家药监局的沟通后启动HMPL-453治疗肝内胆管癌研究及赛沃替尼治疗胃癌研究的注册阶段的患者招募. Retrieved Apr 04, 2023, from https://mp.weixin.qq.com/s/IUu6PvEBIhUJ_aoE09d8kQ
[3]和黄医药将于美国癌症研究协会(AACR)2023年年会公布最新研究结果. Retrieved Apr 12, 2023, from https://www.hutch-med.com/sc/hutchmed-highlights-presentations-at-aacr-2023/
[4]CT152 / 14 - A multicenter Phase II study of savolitinib in patients with MET-amplified gastroesophogeal junction adenocarcinomas or gastric cancer. From AACR Annual Meeting 2023 Itinerary Planner | Presentation (abstractsonline.com)
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..