8 月 11 日,据 Insight 数据库显示,礼来在国内首次公示启动了口服小分子 GLP-1R 激动剂 Orforglipron 的全球多中心 III 期临床 ATTAIN-1(试验登记号:CTR20232459)。这也是 Orforglipron 在国内启动的首个 III 期临床试验。
根据过往时光轴,这项临床早在 2023 年 5 月 12 日就在 ClinicalTrials.gov 上登记,并在 6 月 5 日开始受理入组,全球已入组 124 人,目标入组人数 3000 人,主要指标完成日期预计在 2025 年 9 月 12 日。
ATTAIN-1 全球临床试验进展时光轴
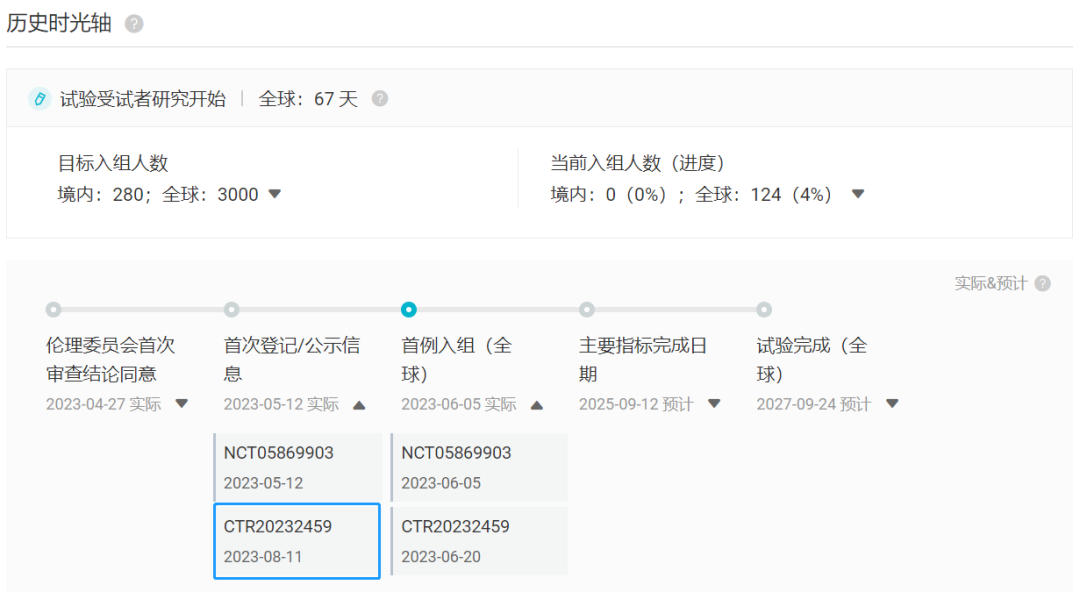
截图来自:Insight 数据库网页版(http://db.dxy.cn/)
礼来是 GLP-1 赛道的佼佼者,布局面面俱到。从度拉糖肽(Trulicity)开始,到同赛道遥遥领先的 GLP-1R/GIPR 双重激动剂替尔泊肽(Tirzepatide,Mounjaro),再到 GLP-1R/GIPR/GCGR 三重激动剂 Retatrutide,现今也处于 III 期临床,同类最快。不止如此,今日在华启动临床的 Orforglipron 也是全球首个启动 III 期临床的口服小分子 GLP-1RA。这也许就是近日市值攀升 5000 亿美元的底气所在。
梳理礼来 Orforglipron 和 Retatrutide 两款新药的 III 期临床,我们也可以看到,随着长期在代谢领域的深耕和市场洞察,GLP-1 赛道研发风向已变,临床阶段药物首先攻占的适应症从 2 型糖尿病转向了肥胖。在口服药物 Orforglipron 的 5 项 III 期临床登记中,有 3 项都以减重为主要目标,其中 ATTAIN-1 针对肥胖或伴有体重并发症的超重,ATTAIN-2 针对超重的 2 型糖尿病患者,在日本开展的 ATTAIN-J 纳入了 BMI ≥35 的更严重肥胖人群。
ACHIEVE 系列的 2 项 III 期临床,一项针对 2 型糖尿病,一项针对超重 2 型糖尿病患者心血管风险。
Orforglipron 全球已登记的 III 期临床
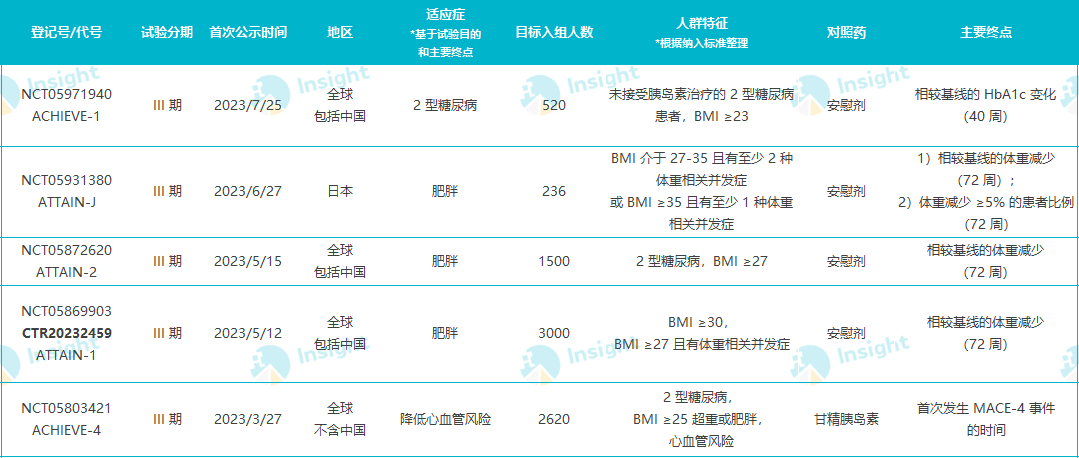
表格数据整理自 Insight 数据库,下同
Retatrutide 开展的 4 项 TRIUMPH 系列 III 期临床均针对肥胖,其中 TRIUMPH-3 针对至少 1 种心血管疾病的严重肥胖患者(BMI ≥35),另外 3 项则探索了超重/肥胖人群膝骨关节炎和阻塞型睡眠呼吸暂停(OSA)。
Retatrutide 全球已登记的 III 期临床
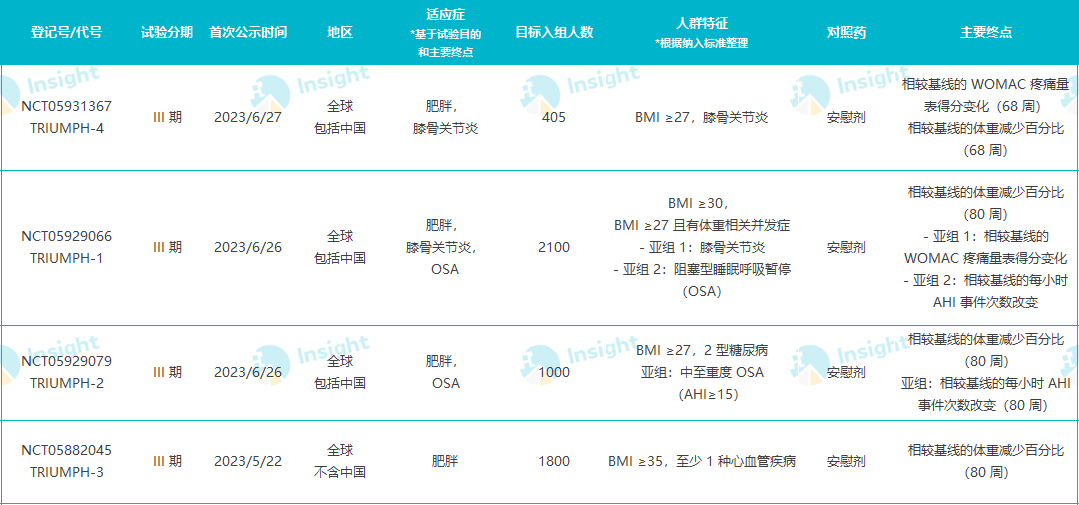
从临床试验登记的时间来看,这些试验的开启密集于今年 5-6 月,在这两个月礼来仅针对这两款新药就启动了 7 项大 III 期临床。全部这两款药已启动 III 期临床的目标入组人数算来,就将纳入 13181 人之多。
6 月末的 ADA(美国糖尿病协会)年会上,Orforglipron 和 Retatrutide 双双亮相,已经完成了 II 期临床数据首发。其中 Orforglipron 的临床数据包含 2 型糖尿病和肥胖症,两项结果也同时发布在柳叶刀和 NEJM 上。
肥胖症方面,经过 36 周 Orforglipron 治疗,45mg 剂量组减重 14.7%,相较安慰剂组减重 12.4%。糖尿病临床中同样有减重结果披露,Orforglipron 治疗 26 周时实现 10.1kg 减重,而安慰剂和度拉糖肽组则分别为 2.2kg 和 3.9kg。
Orforglipron 减重数据
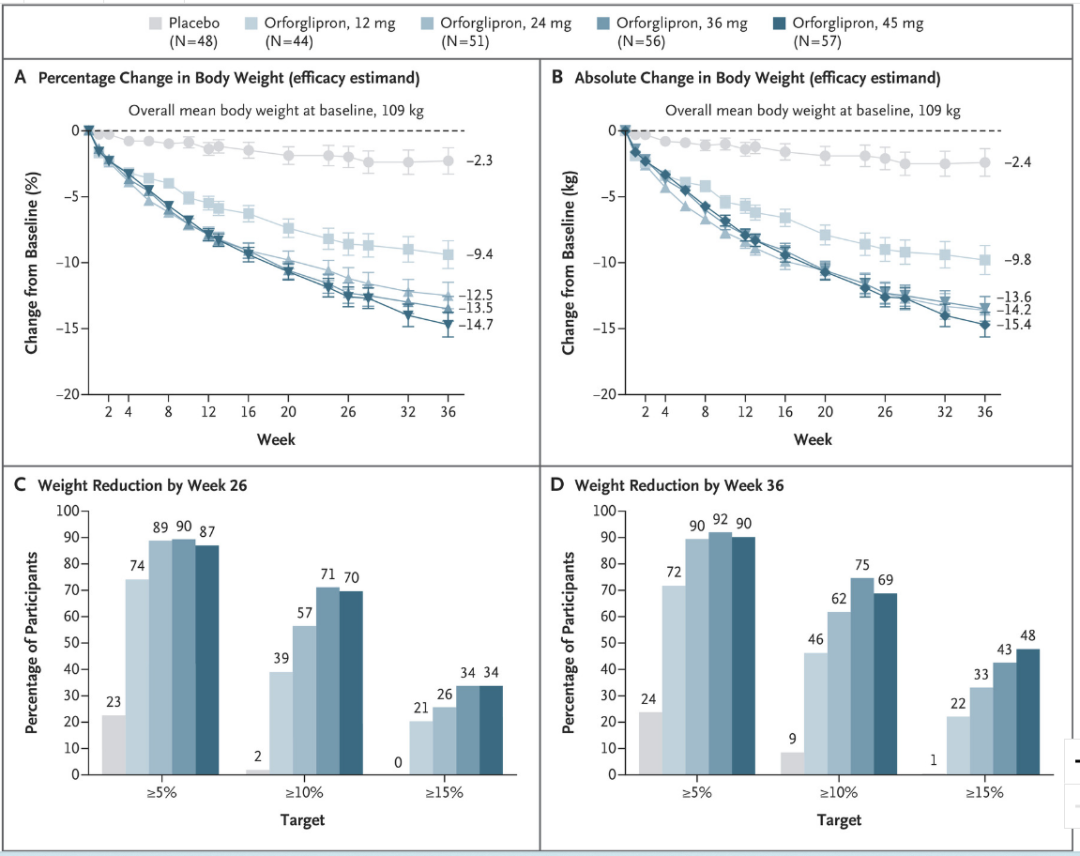
截图来自:Lancet
Retatrutide II 期临床数据也同时发表于 NEJM,这项为期 48 周的随机、双盲、安慰剂对照 II 期临床研究(登记号:NCT04881760)纳入 338 位肥胖或带有至少一项体重相关共病的超重成人患者,结果显示,治疗 24 周时 Retatrutide (1mg、4mg、8mg 或 12mg) 在肥胖或超重(糖尿病除外)成年患者中达到疗效评估的主要终点,平均体重减轻 17.5%;在治疗 48 周时,接受每周注射 12mg Retatrutide 治疗的受试者平均体重减轻 24.2%。
NCT04881760 试验结果

关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..