近日,Adicet Bio公布了其γδ-T细胞疗法ADI-001的 I 期研究数据。
ADI-001是一种即用型CD20靶向CAR γδ-T细胞疗法,用于治疗复发/难治性B细胞非霍奇金淋巴瘤患者。与其它类型的T细胞不同,γδ-T细胞不需要与主要组织相容性复合物(MHC)分子结合,可以直接识别并结合靶细胞抗原,这一特性意味着γδ-T细胞不太可能受到治疗耐药性的影响,从而针对肿瘤细胞产生强大的杀伤作用。
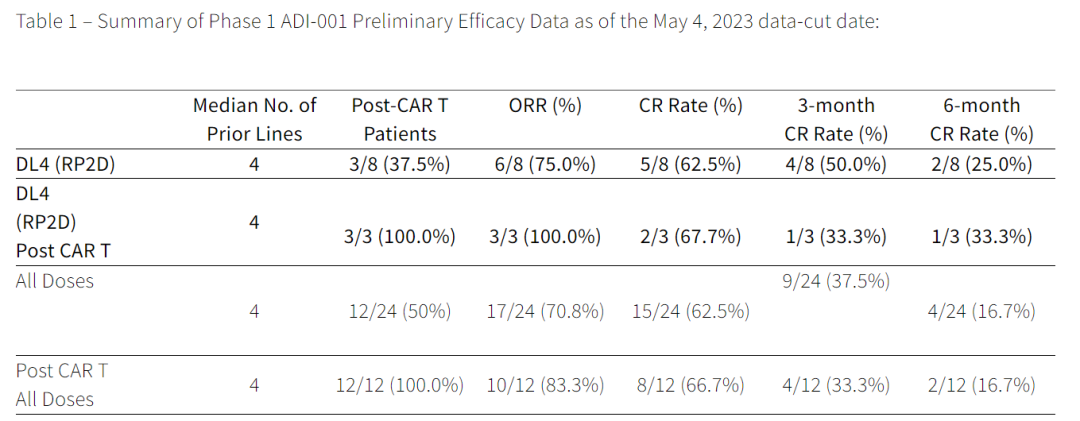
图:ADI-001有效性(截至2023年5月4日)
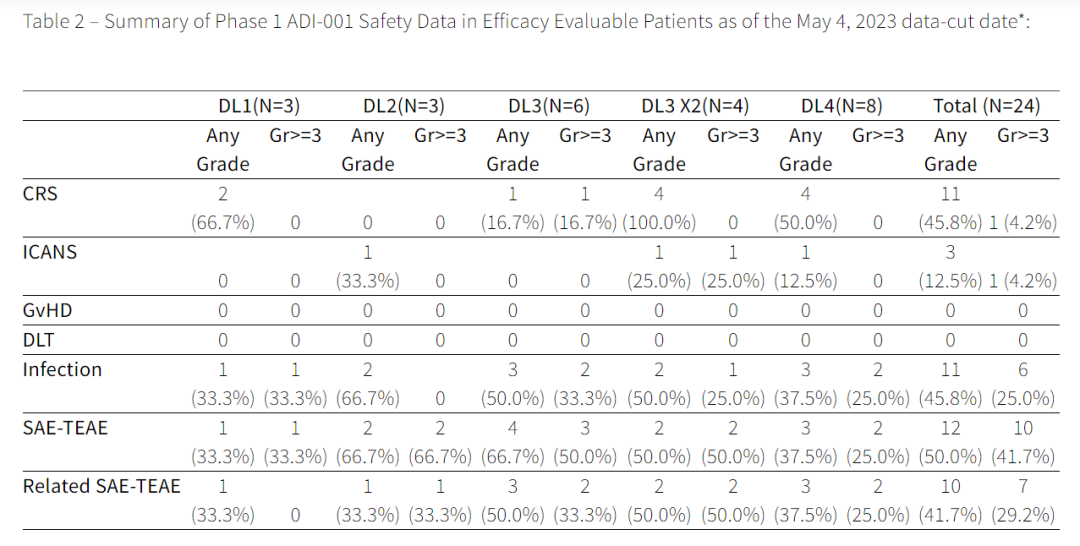
图:ADI-001安全性(截至2023年5月4日)
该公司表示,“ADI-001安全性和有效性数据令人兴奋,ADI-001 在所有剂量水平上表现出 71% 的总体缓解率 (ORR) 和 63% 的完全缓解率 (CRR) ,超出了预期。其中 50% 的患者曾接受过自体 CAR-T 疗法并失败,在这些患者中,ADI-001总体缓解率达83% ,完全缓解率达67%。并且ADI-001 通常具有良好的安全性,没有发生剂量限制性毒性或移植物抗宿主病。”
然而,关键试验的讨论晚于此前传言时间。摩根大通分析师Brian Cheng表示,“喜忧参半”的新数据留下了“关键问题”没有得到解答,由此质疑ADI-001的耐受性潜力。
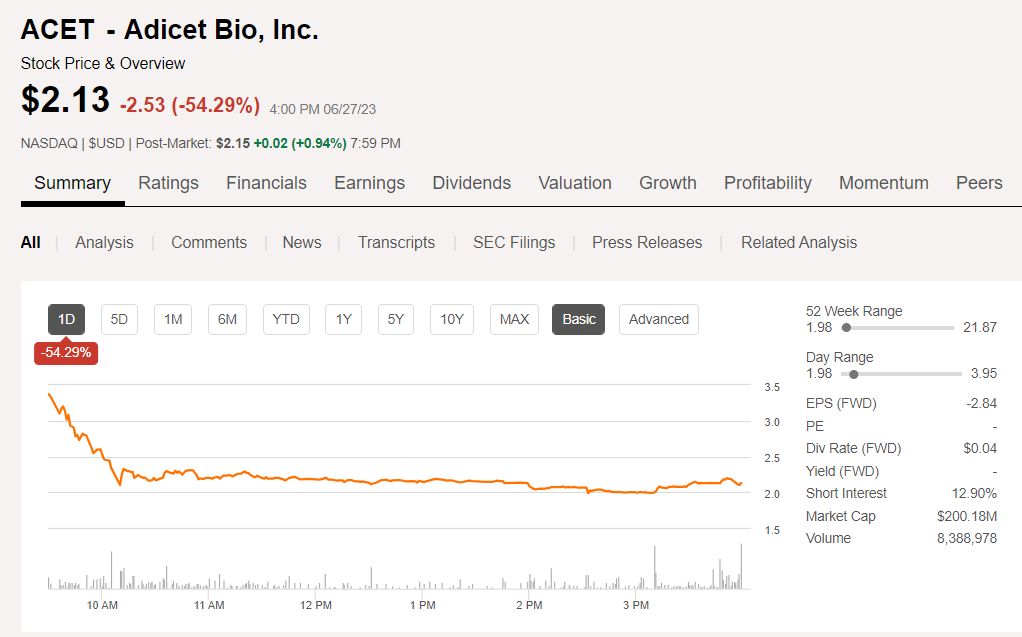
受此影响,Adicet Bio股价大跌54%,目前市值2.0018亿美元。2023年1月1日~3月31日,Adicet Bio收入为0,同比减少100.00%,净亏损达3088.10万美元,同比由盈转亏。
Adicet Bio总裁兼首席执行官Chen Schor表示,靶向CD19的自体CAR-T疗法市场正在快速增长,每年超过22亿美元。尽管如此,约 60%~70% 的患者病情仍有所进展,表明还存在巨大的未满足临床需求。
Adicet Bio计划于 2024 年上半年推进 ADI-001 治疗大B细胞淋巴瘤(LBCL)项目至关键 2 期临床研究。此外,预计 2024 年下半年,Adicet Bio更新经过 CAR-T 治疗后 LBCL 患者使用ADI-001 的疗效、6 个月CRR以及安全性等数据。
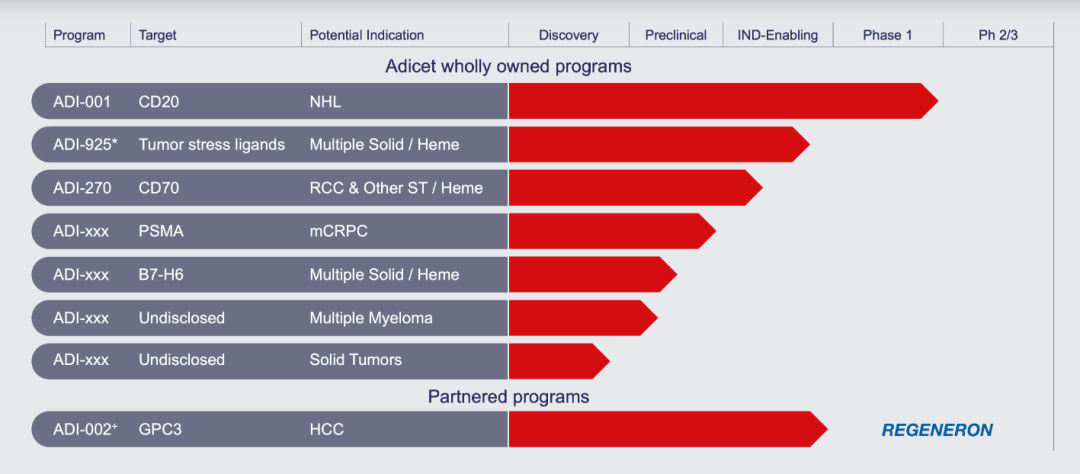
Adicet Bio研发管线 来源:官网
关于Adicet Bio
Adicet Bio于2016年7月5日成立,是一家美国细胞免疫治疗技术研发商,致力于研发治疗癌症和其他疾病的γδ-T细胞疗法。他们正在推进一系列“现成”的γδ-T细胞,利用嵌合抗原受体(CAR)和T细胞受体样抗体(TCRL)进行设计,以增强肿瘤的选择性靶向性,促进先天和适应性抗肿瘤免疫反应,并提高患者持久活性的持久性。
参考资料:
https://investor.adicetbio.com/news-releases/news-release-details/adicet-bio-reports-positive-data-ongoing-adi-001-phase-1-trial-0
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..