在最近的美国FDA咨询会议上,所有6位参会专家一致认同3期临床试验CLARITY AD的结果,这为卫材(Eisai)和渤健(Biogen)共同研发的阿尔茨海默病(AD)抗体疗法Leqembi(Lecanemab)获得完全批准提供了有力支持。因此,Lecanemab有极大的可能在今年7月份得到完全批准。
来源:渤健官网
01
FDA的完全批准对于Lecanemab的意义
Lecanemab是一款基于β淀粉样蛋白假说设计的单克隆抗体,作用于β淀粉样蛋白(Aβ)原纤维,旨在减少患者脑中淀粉样蛋白板块的积聚。在今年1月,Lecanemab获得了美国FDA的加速批准。使其在名义上实现了上市。然而,实际上这并不意味着Lecanemab已经实质性地进入了商业化阶段。
事实上,Lecanemab未能实质性商业化原因,正是源于渤健和卫材自己研发的Aduhelm(aducanumab)。Aduhelm——近20年来FDA首款批准的阿尔兹海默药物,曾为阿尔兹海默症的治疗带来片刻曙光,但最终给渤健和卫材留下一地鸡毛,亦使得基于β淀粉样蛋白假说设计的药物蒙尘。FDA审批争议,以及其明显的不良反应(淀粉样蛋白相关的影像学异常(ARIA)),最终导致了美国医疗保险和医疗补助服务中心(CMS)修改了支付范围,仅限于美国国家卫生研究院(NIH)执行的临床试验者。
这一修改同样地适用于Lecanemab,因此在其加速批准获得上市后,并不能得到美国医保支付的覆盖,故其并未实质性上市。
因此,七月的完全批准成功被纳入美国CMS支付范围,才是Lecanemab真正商业化的第一步。
02
渤健的业绩泥潭
原本寄望于Aduhelm带来丰厚利润的渤健,却最终陷入失望。根据渤健公布的2022年财报,该公司2022年全年营收101.73亿美元,同比下降7%,其中产品净销售额79.88亿美元,同比下降9.7%;净利润为29.42美元,同比增长71.43%。
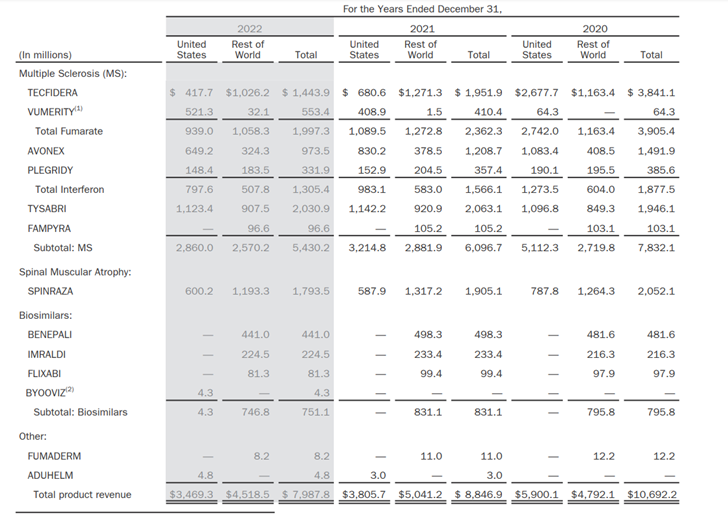
来源:渤健2022年财报
报告显示,多发性硬化产品总营收为54.3亿美元,同比下降11%。多发性硬化症药物Tecfidera,作为渤健的营收重地,销售额在2022年大幅下滑26%,同时市场份额也被罗氏的Ocrevus所夺取。业绩不佳,渤健于今年4月启动新一轮裁员,退货诺诚健华的奥布替尼,砍管线以节省开支。Tecfidera由于专利被无效,曾寄希望于Aduhelm来弥补渤健在多发性硬化症市场的颓势,但是Aduhelm在安全性争议和医保覆盖问题上的挑战,最终使得渤健的期望落空。
03
Lecanemab成为渤健翻身的关键
虽然有了Aduhelm的前车之鉴,但渤健仍决定在AD领域死磕。根本原因在于,阿尔兹海默症药物市场庞大的市场规模,且存在尚未满足的药物需求。根据阿尔茨海默病协会《2022年阿尔茨海默病事实与数据》,在美国65岁以上的阿尔兹海默症群体便高达650万,是美国第六大死因。2020年,阿尔兹海默症群体的治疗成本高达2670亿美金。根据2020年在《柳叶刀》杂志上发布的报告,全球痴呆症患者的数量约为5000万。在中国,60岁及以上的老年人中,大约有1500万人患有痴呆症,其中阿尔茨海默病患者达到了1000万。预计到2050年,我国的阿尔茨海默症患者数量将超过3000万。此外,美国药物生产与研发协会在2018年的报告中指出,从2000年到2017年,药厂在阿尔兹海默症研发上的累计投入已超越6000亿美元。因此,即使AD领域已成为无数药企的英雄冢,但千亿美金的市场的诱惑,仍使得无数药企前仆后继。
而Lecanemab与Aduhelm究竟有何不同?首先,与Aduhelm相比,Lecanemab在CLARITY AD的临床试验中已经证明了其疗效,而Aduhelm仅仅是在基于在以β样淀粉蛋白为生物标记物获批。而且由于淀粉样蛋白相关成像异常(ARIA)副作用严重,在同样的FDA咨询会议上,委员会几乎全票反对Aduhelm上市决定。显而易见,不同于本次Lecanemab的全票支持态度。
毫无疑问的是,Lecanemab如果在7月顺利获批,Lecanemab将成功实现其商业化之路。据分析师预测,Lecanemab获得BLA后,其销售峰值可能超过90亿美元。因此,Lecanemab无疑承载渤健走出业绩泥潭的希望。
04
Lecanemab和Donanemab的龙争虎斗
在阿尔茨海默症庞大的治疗市场中,竞争者从来都不乏其人。在22年年末,尽管罗氏宣布其AD药物ganteneruma三期临床失败,但今年5月礼来公布其Aβ抗体Donanemab治疗阿尔茨海默症三期临床TRAILBLAZWE-ALZ2的最新数据,使礼来达到了4000亿美元的市值。
Donanemab的三期临床研究达到iADRS主要终点,显著延缓认知功能下降。Donanemab治疗相比于安慰剂,将认知功能下降(iADRS)延缓了35%(主分析人群)。与之相对地,Lecanemab在将认知功能下降(CDR-SB)延缓了27%。仅从数字比较角度Donanemab是展现出了优于lecanemab的减缓率。然而,由于两个试验比较人群存在差异,所以直接比较这两个数字可能有一定的局限性。
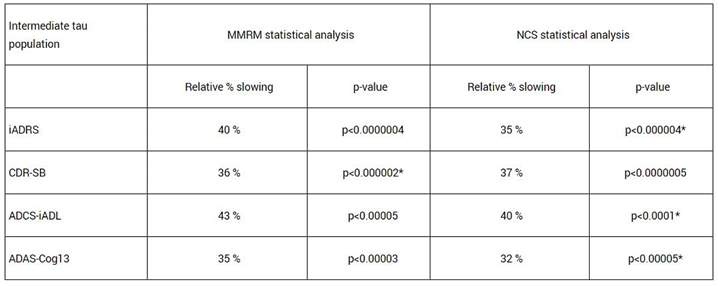
来源:礼来官网

来源:渤健官网
同时,在副作用方面,Donanemab的治疗组中有两名受试者因为淀粉样蛋白相关成像异常(ARIA)死亡。此外,相比于Lecanemab(每两周注射一次,整个三期临床试验期间持续用药),具有更长给药间隔的Donanemab(每四周注射一次,影像确认清除β淀粉样蛋白到一定程度后停药)似乎展现出了更为严重的不良反应。因此,虽然Donanemab可能展现出潜在的治疗优势,但它可能也具有更严重的副作用。
因此,如果Lecanemab能够顺利获得完全批准,那么它不仅将获得阿尔茨海默症药物市场的先发优势,而且还可能由于其较小的副作用而具有更大的优势。Lecanemab可能是开启阿尔兹海默症蓝海市场的关键。
总结
对于Aβ方向的研究,尽管在过去的几十款新药的临床研发阶段中,许多试验最终以失败或终止告终,但今年以来Lecanemab和donanemab的积极临床结果为此提供了新的信心和希望。
对于研发黑洞AD,国内药企也有在积极布局。除了绿谷药业的富有争议的GV971外,先声、恒瑞、海正、东阳光、润佳医药等都已开始对AD药物进行布局。然而,需要注意的是,这些国内药企的布局主要集中在小分子药物方向,目前仅有恒瑞医药布局有Aβ抗体SHR-1707。值得一提的是,SHR-1707的Ib期临床试验近日在中国科学技术大学附属第一医院已经完成了首例患者入组及给药。
总的来说,虽然阿尔茨海默症药物研发的道路依然充满挑战,但随着科学研究的不断进步和新药物的积极临床结果,我们对治疗这种疾病的未来充满了希望。无论是国际还是国内的药企,都在积极寻找有效的治疗手段,期待能为这个领域带来更多的突破。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..