ASCO 是全球肿瘤领域最重要、最权威的学术交流盛会之一。2023 年度 ASCO 年会将在 6 月 2 日至 6 月 6 日正式召开,而今天,会议的常规摘要已经对外公开释放。

截图来自:ASCO 官网
Insight 数据库持续关注全球新药研发关键情报,ASCO 摘要一经公布,已迅速启动相应临床结果的更新工作;同时在公众号上,我们也将随之发布系列文章和专题报告,对亮点临床结果做报道、盘点和解析。
本次国内企业已公布的新临床成果中,有哪些进展值得关注?本篇文章将以此为主题,小作摘取和介绍。*单篇文章篇幅有限,难以纳入所有重要研究结果。欢迎关注公众号,获取后续更多资讯推送。
PD-(L)1 辅助疗法的新进展
君实生物是本届 ASCO 中入选口头报告最多的国内企业。这 5 项口头报告均聚焦于特瑞普利单抗,除一项针对三阴乳腺癌(TNBC)的大会重磅研究摘要(LBA)需等待正式会议期间才会公开披露,其余摘要当前已可抢先一睹为快。
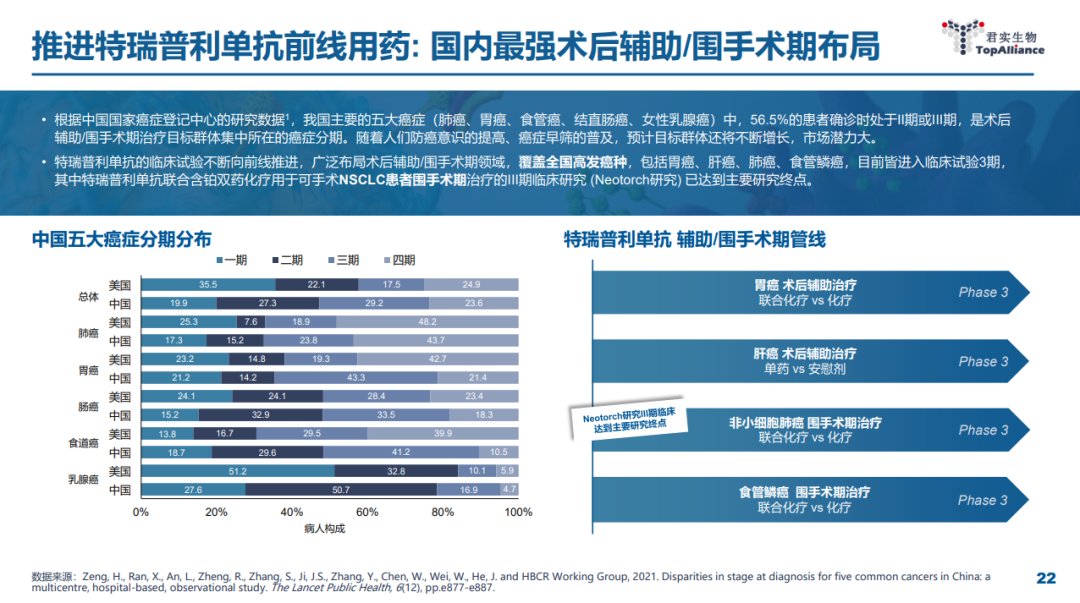
在本届 ASCO 上,特瑞普利单抗的一大看点在于辅助/新辅助治疗的数据释放。君实是国内 PD-(L)1 单抗中围手术期布局最广泛而深入的企业,已经覆盖包括胃癌、肝癌、非小细胞肺癌和食管鳞癌等国内高发癌种。
本次会议上,君实将以口头报告形式发布包括 NSCLC 围术期治疗 III 期临床、胃癌围术期治疗 II 期临床以及可切除年末黑色素瘤辅助治疗 II 期临床结果。
截图来自:君实生物 2022 年报
标题:特瑞普利单抗+含铂双药化疗 vs 化疗用于可切除 II/III 期非小细胞肺癌 (NSCLC) 的围手术期治疗:III 期 Neotorch 研究的无事件生存期 (EFS) 期中分析
试验登记号:NCT04158440
主要研究者:陆舜(上海交通大学医学院附属胸科医院)
摘要编号:#8501
2023 年 4 月 12 日,君实基于 Neotorch 研究递交了特瑞普利单抗用于 NSCLC 围手术期治疗的新适应症上市申请。在同月的 ASCO 全体大会系列(ASCO Plenary Series)中,君实已经发布了 Neotorch 研究的结果,而在 6 月的 ASCO 年会上,则将以口头报告形式发布更多详细数据。
Neotorch 研究是全球首个抗 PD-1 单抗用于 NSCLC 围手术期(涵盖新辅助和辅助治疗)治疗达到 EFS 阳性结果的 III 期临床研究。这项随机、双盲、安慰剂对照、多中心的 III 期临床研究旨在比较特瑞普利单抗联合含铂双药化疗对比安慰剂联合含铂双药化疗治疗可手术 NSCLC 患者的疗效和安全性,共纳入 404 例 III 期NSCLC患者,以 1:1 的比例被随机分配至特瑞普利单抗联合化疗组(n=202)或安慰剂联合化疗组(n=202),分别接受特瑞普利单抗或安慰剂联合化疗术前 3 周期及术后 1 周期治疗(鳞癌患者化疗方案为紫杉类+铂类,非鳞癌患者化疗方案为培美曲塞+铂类),随后接受特瑞普利单抗或安慰剂巩固治疗 13 周期。
截至 2022 年 11 月 30 日(中位随访时间 18.3 个月),结果显示:与单纯化疗相比,特瑞普利单抗疗法可显著延长患者 EFS,降低 60% 的疾病进展或死亡风险(HR=0.40,95%CI:0.277-0.565,双侧P<0.0001)。中位 EFS 分别为尚未成熟 vs 15.1 个月,P<0.0001。
同时,经盲态独立中心病理(BIPR)评估,特瑞普利单抗联合化疗组的主要病理缓解(MPR)率和完全病理缓解(pCR)率方面均优于单纯化疗组,分别为 48.5% vs 8.4%(P<0.0001)和 24.8% vs 1.0%(P<0.0001)。特瑞普利单抗联合化疗组的总生存期(OS)也显示出明显的获益趋势。
官网链接:https://meetings.asco.org/abstracts-presentations/219867
标题:抗 PD-1 单抗特瑞普利单抗联合 SOX 或 XELOX 化疗 vs 单纯 SOX 或 XELOX 化疗用于局部晚期胃或胃食管结合部癌的围手术期治疗:一项前瞻性、随机、开放 II 期研究结果
试验登记号:NCT04250948
主要研究者:徐瑞华、周志伟(中山大学肿瘤防治中心)
摘要编号:#4001
研究结果:这是一项前瞻性、随机、开放标签 II 期临床试验,旨在评估在可切除局部晚期胃或胃食管交界处癌患者围手术期化疗中加入 PD-1 单抗的疗效。这些临床病理分期 cT3-4a N+M0 的患者以 1:1 随机分配至化疗组(C)或联合疗法组(C+T),前者接受术前 3 次术后 5 次每 3 周一次的 SOX/XELOX 治疗,后者接受特瑞普利单抗联用 SOX/XELOX、随后接受特瑞普利单抗单药治疗 6 个月。主要终点为病理完全消退率/中度消退率(TRG 0/1)。
在 2019 年 10 月至 2022 年 6 月共 108 例患者纳入(C+T arm,n=54; C arm, n=54),并使用意向治疗分析进行评估。联合疗法组 TRG 0/1 比例显著高于化疗组,分别为 44.4%(24/54,95% CI:30.9%-58.6%)vs 20.4%(11/54,95% CI:10.6%-33.5%),p=0.009;同时显示出更高的 pCR 率,分别为 24.1%(13/54,95% CI:13.5%-37.6%)vs 9.3%(5/54,95% CI:3.1%-20.3%),p=0.039。
官网链接:https://meetings.asco.org/abstracts-presentations/219777
标题:替莫唑胺联合顺铂 vs 特瑞普利单抗(抗PD-1)辅助治疗可切除的黏膜黑色素瘤
主要研究者:郭军(北京大学肿瘤医院)
摘要编号:#9508
在免疫治疗时代,PD-1 抑制剂已经成为可切除黑色素瘤标准疗法,然而尚无研究在黏膜黑色素瘤(MuM)中比较免疫疗法与化疗作为辅助治疗的疗效。这是一项回顾性分析,纳入了 2013 - 2019 年共 247 例患者,其中特瑞普利单抗组 78 例,化疗组 169 例。不过在这项研究中,化疗组表现出了更长的 RFS、DMFS 和 OS,这表明即使在免疫治疗时代,在不同肿瘤亚型中辅助化疗也可能成为更优选。
官网链接:https://meetings.asco.org/abstracts-presentations/226520
百济神州 OX40 单抗首次披露数据,
百利天恒双抗、双抗 ADC、四抗齐登场
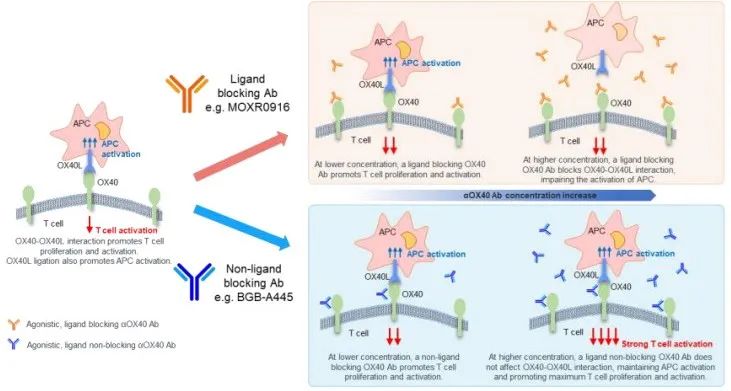
BGB-A445 是百济神州开发的 OX40 激动剂抗体。该药与其他所有临床 OX40 抗体具有差异,不阻断 OX40-OX40L 结合,保持抗原递呈细胞 OX40L 的信号,天然配体刺激达到 OX40 最大程度激活,在包括 PD-1 耐药模型在内的临床前模型中表现出广泛的单药疗效。
而在今年 ASCO 大会中,百济将以海报形式释放该药的首次人体临床试验数据(摘要编号#2574)。
BGB-A445 作用机理
来自:百济神州官网
结果显示,BGB-A445 单药或与替雷利珠单抗联合用于治疗晚期实体瘤患者,在所有剂量下的总体耐受性均良好,无剂量限制性毒性,并表现出初步抗肿瘤活性。为对其进行进一步评价,目前百济正在剂量扩展阶段入组非小细胞肺癌和头颈部鳞状细胞癌队列的患者。
百济从 Zymeworks 公司引进的 HER2 双抗 Zanidatamab(ZW25)也将在这次 ASCO 年会中释放两项数据,包括关键性 IIb 期 HERIZON-BTC-01 研究结果,治疗既往经治的 HER2 扩增型胆管癌,以口头报告形式发布;一项联用多西他赛作为晚期 HER2 阳性乳腺癌一线治疗的 Ib/II 期研究更新结果,以海报形式发布。
据 Insight 数据库显示,ZW25 目前在胃癌和食管癌上已经进展至 III 期临床,胆管癌次之,22 年 12 月也已经释放了 II 期顶线数据。
ZW25 进展最快的适应症

截图来自:Insight 数据库网页版
百利天恒专注于开发多特异性抗体及 ADC 药物,本次也携 5 项结果登场,其中包括了 EGFR/HER3 双抗 SI-B001、PD-1/CTLA-4 双抗 SI-B003、CD19/CD3/PD-L1/4-1BB 四抗 GNC-038 和 EGFR/HER3 双抗 ADC 药物 BL-B01D1。
最值得关注的则是 BL-B01D1,本次公布的首项人体试验入选了口头报告(摘要编号:#3001)。由于第一三共 HER3 ADC 药物 Patritumab Deruxtecan(HER3-DXd,U3-1402)已经取得了一系列亮眼里程碑结果,也为这一靶点带来了无限的想象力。
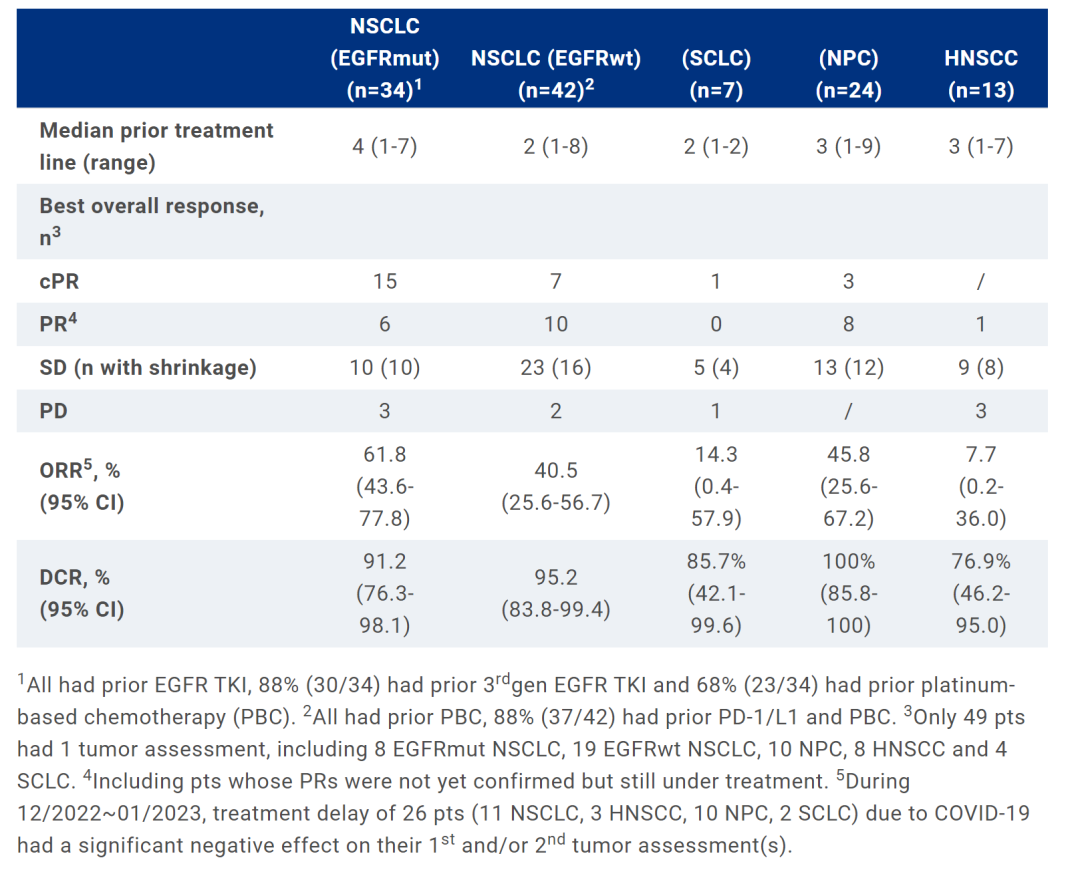
BL-B01D1 临床数据
截图来自:ASCO 官网
科伦、迪哲…小分子化药惊艳亮相
尽管科伦近期持续以 ADC 而闻名,其小分子新药研发实力同样不俗。本次 ASCO 中该公司报告了 2 项临床结果,小分子 RET 抑制剂 KL590586(A400) 的首次 I 期数据以口头报告形式亮相。
本次释放数据的 I 期临床研究,包括剂量递增和剂量扩展两个阶段。截至 2022 年 12 月 30 日,研究纳入 87 例 RET 基因改变的晚期实体瘤患者,按研究设计分配到 6 个剂量组 (10mg-120mg,QD) 接受治疗。
安全性方面,没有观察到剂量限制性毒性 (DLT),最大耐受剂量 (MTD) 未达到。治疗相关不良事件 (TRAEs) 的发生率为 93.1%(81/87),大部分为 1-2 级。
疗效方面,69 例接受有效剂量 (40mg-120mg) 治疗的患者疗效可评估,其中 57 例为非小细胞肺癌(NSCLC),10例为甲状腺髓样癌(MTC),1 例为胰腺癌,1 例为卵巢癌,客观缓解率 (ORR) 为 64%。截至数据截止日,绝大部分患者(58/69) 仍在接受治疗,最长治疗时间超过 11 个月。
在既往接受过系统治疗的患者 (中位线数为 2 [范围,1-9],28% 接受了抗 PD-1/PD-L1 治疗),ORR 为 63% (20/32,1 例 CR),疾病控制率 (DCR) 为 91%,中位 DoR 未达到。11 例基线脑转移患者 (既往未接受放疗),针对脑部病灶的DCR为100%。既往未接受治疗的 NSCLC 患者,ORR 为 76% (19/25,1 例CR),DCR 为 92%,4 例为有可测量脑部病灶患者(既往未接受放疗),3 例脑部病灶响应为 PR 或 CR。
迪哲医药也以口头报告形式公布了自研产品舒沃替尼治疗 EGFR 20 号外显子插入(EGFR exon20ins)突变型晚期非小细胞肺癌(NSCLC)首个关键研究(悟空6, WU-KONG6)的口头报告摘要。
该项研究结果显示,舒沃替尼在既往化疗失败的 97 例 EGFR exon20ins 突变型晚期 NSCLC 患者中经独立影像评估委员会(IRC)确认的客观缓解率(cORR)达 60.8%,在多种 EGFR exon20ins 突变亚型中均观察到抗肿瘤活性,对基线伴有经治且稳定的脑转移患者也显示疗效,进一步显示出潜在同类最优(BIC)疗效。
其整体安全性与传统 EGFR TKI 相似,为 EGFR exon20ins 突变型晚期 NSCLC 带来潜在更优的治疗选择。
题图来源:站酷海洛 plus
免责声明:本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..