尽管癌症治疗已经取得了很大进展,人们依然谈癌色变。据2021年世界卫生组织国际癌症研究机构(IARC)发布的数据,2020年全球新发癌症病例预计为1929万例,全球癌症死亡病例预计为996万例。随着人口老龄化,以及吸烟、饮酒、不健康饮食、缺乏运动和空气污染等多种危险因素,全球癌症发病率、死亡率都在增加。
癌症的治疗给家庭、国家带来巨大的经济负担。据德国海德堡大学/中国医学科学院北京协和医学院陈思邈教授等在JAMA Oncology期刊发表的题为《Estimates and Projections of the Global Economic Cost of 29 Cancers in 204 Countries and Territories From 2020 to 2050》的研究论文,2020年至2050年这30年,全世界将为癌症花费25.2万亿美元。
随着对疾病研究的深入,以及生物技术的发展,目前癌症治疗取得了巨大的进步,新型靶向疗法、免疫疗法、细胞疗法不断涌现。疫苗在癌症预防、治疗中占有重要地位,然而进展相对较缓,不过肿瘤疫苗的研发从未终止。
肿瘤疫苗
肿瘤疫苗是利用肿瘤抗原,通过主动免疫方式诱导机体产生特异性抗肿瘤效应,激发机体自身的免疫保护机制,达到肿瘤治疗或预防复发的作用,属于主动免疫治疗范畴。肿瘤抗原通常被分为肿瘤特异性抗原(TSA)和肿瘤相关抗原(TAA),其中TSA包括病毒抗原和由非同义体细胞突变产生的新表位,TAA则包括组织特异性抗原和发育特异性抗原。
根据用途的不同,肿瘤疫苗可分为预防性肿瘤疫苗(如HPV疫苗)和治疗性肿瘤疫苗(主要以肿瘤抗原为基础,用于放化疗或手术切除后的辅助治疗)。而根据肿瘤抗原组分和性质的不同,肿瘤疫苗可分为以细胞为载体的肿瘤疫苗、病毒疫苗、蛋白/多肽疫苗、核酸疫苗(DNA疫苗)、抗独特型疫苗和异种疫苗等。
据不完全统计,目前全球已经批准了能预防肝癌的乙肝病毒(HBV)疫苗(中国70%左右肝癌和乙肝病毒相关)、预防宫颈癌的人乳头瘤病毒(HPV)疫苗(99%的宫颈癌和人乳头瘤病毒相关),以及治疗前列腺癌的疫苗Sipuleucel-T、治疗肺癌的疫苗CIMAvax-EGF和Vaxira、治疗头颈鳞癌的疫苗CIMAher、治疗皮肤癌的疫苗Heberferon和治疗实体瘤的疫苗(如德国LANEX-DC和日本WT1肽抗原树突细胞疫苗)。
Sipuleucel-T
Sipuleucel-T是一种自体细胞来源的免疫治疗药,由自体树突状细胞(DCs)与融合蛋白PA2024在体外共孵化获得(PA2024是一种由前列腺酸性磷酸酶(PAP)和粒细胞巨噬细胞集落刺激因子(GM-CSF)构建的融合蛋白 (PAP-GM-CSF),PAP-GM-CSF再与自身抗原呈递细胞(PAC)共同培养,融合蛋白可分解成小肽呈现在PAC表面,提高对肿瘤细胞的免疫应答能力)。2020年,Sipuleucel-T被FDA批准用于治疗无症状或症状轻微转移性去势抵抗性前列腺癌。
CIMAvax-EGF
CIMAvax-EGF主要由表皮生长因子(EGF)和一种叫P64K蛋白质组成。CIMAvax-EGF可以激活人体免疫系统产生EGF抗体,抗体与身体内的EGF结合迫使癌细胞接收不到EGF的信号,由于接受不到EGF信号,癌细胞就会感到饥饿,从而阻止癌细胞的增殖和转移。2011年,CIMAvax-EGF被批准进入古巴肺癌治疗的临床使用。
Vaxira
Vaxira是二代疫苗,2012年在古巴上市。Vaxira主要成分包括Racotumomab和氢氧化铝辅剂。Racotumomab是针对AcM P3的IGI同种型的单克隆抗体,它专门识别AcM P3单克隆抗体并抑制其与神经节苷脂NeuGcGM3的结合(神经节苷脂NeuGcGM3是一种特异性的肿瘤抗原,在不同类型的肿瘤细胞如非小细胞肺癌,乳腺癌和黑色素瘤中高表达)。
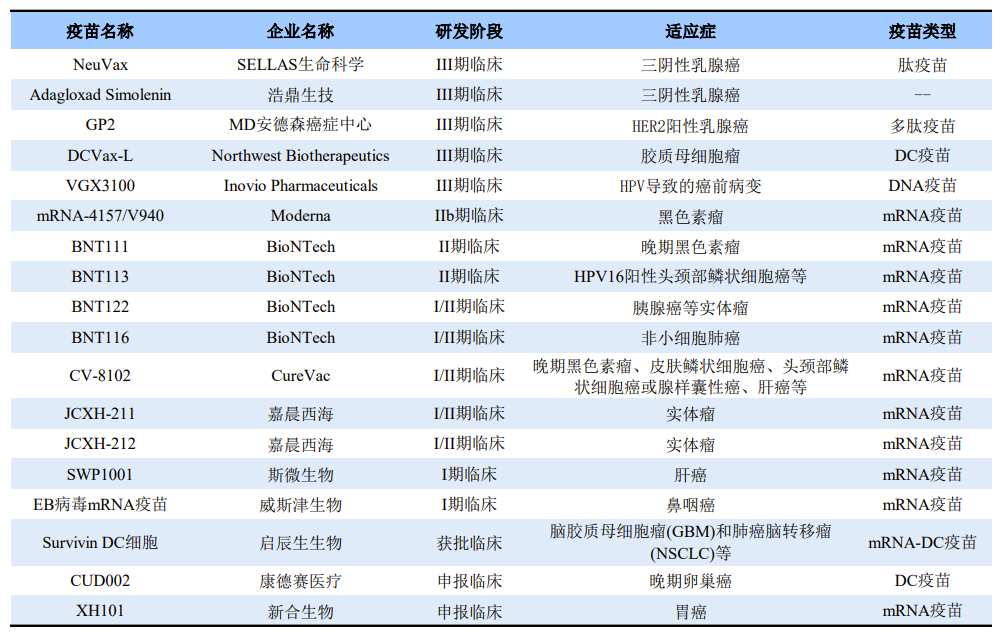
此外,目前全球还有多款在研肿瘤疫苗(详见下表),其中多款已进入III期临床。在研肿瘤疫苗大多被开发用于实体瘤的治疗。疫苗类型上,在研肿瘤疫苗包括肽疫苗、DC疫苗、DNA疫苗和mRNA疫苗等。企业上看,国内外药企均在积极布局。尤其是mRNA肿瘤疫苗领域,除了mRNA三大巨头BioNTech、Moderna、CureVac等国外药企,我国药企,如斯微生物、新合生物、嘉晨西海等也在积极布局布局mRNA肿瘤疫苗领域。
值得一提的是,全球首款mRNA肿瘤新抗原疫苗即将出线,Moderna在其肿瘤新抗原mRNA疫苗mRNA-4157/V940于今年2月被FDA授予突破性疗法认证之后寻求其加速批准。
全球部分在研肿瘤疫苗图片资料来源:公开资料
NeuVax
NeuVax是一种基于肽的癌症免疫疗法,是来源于HER2蛋白的一种免疫原性肽。NeuVax被用作一种疫苗,与免疫佐剂粒细胞-巨噬细胞集落刺激因子(GM-CSF)联合应用时,被证实能够引起强大的抗HER2免疫应答。已公布的2期临床试验结果显示:NeuVax可改善HER-2阳性乳腺癌患者的总生存率,且耐受性良好。NeuVax曾被FDA授予快速通道资格(FTD),用于治疗接受标准护理治疗的HER2表达为低至中等水平(HER2 1+或2+)早期乳腺癌。目前,NeuVax正在进行III期研究,评估NeuVax疫苗(NPS+粒细胞-巨噬细胞集落刺激因子[GM-CSF])联合曲妥珠单抗、GM-CSF单药疗法作为维持疗法,用于TNBC患者在接受标准护理治疗后进行辅助治疗。
Adagloxad simolenin
Adagloxad simolenin是一种以肿瘤相关糖类抗原Globo H为作用靶点的主动免疫抗癌疗法,由Globo H与载体蛋白KLH(钥孔戚血蓝蛋白)共价相连而成(Globo H是一种在乳腺癌、前列腺癌、胃癌、肺癌、结肠癌、胰腺癌与卵巢癌等肿瘤表面大量表达的一种抗原)。Adagloxad simolenin与皂苷佐剂OBI-821联合使用,可以诱导机体产生免疫反应,进而达到抗肿瘤的效果。2021年7月,Adagloxad Simolenin治疗高危早期-Globo H-阳性的三阴性乳腺癌患者的随机、开放、国际多中心3期研究GLORIA启动。
GP2
GP2是一种多肽肿瘤疫苗,是HER2/neu衍生的短肽疫苗。HER2/neu是一种细胞表面受体蛋白,通常表达于HER2阳性乳腺癌及其他各种常见的恶性肿瘤中。2020年圣安东尼奥乳腺癌大会上公布的最新临床试验结果显示:在5年的随访后,46例接受GP2+GM-CSF治疗的HER2+患者的5年DFS发生率为100%,而接受GM-CSF治疗的50例安慰剂患者的5年DFS(无病生存期)发生率为89.4%,GP2将5年生存率提高了近11%。
DCVax-L
DCVax-L是一种完全个性化的免疫疗法,由患者自身肿瘤样本中的树突细胞和抗原(生物标记物)制成。2022年11月,Northwest Biotherapeutics宣布其自体肿瘤裂解液树突状细胞疫苗DCVax-L在新诊断和复发性胶质母细胞瘤脑癌患者中,中位生存期和生存率均延长,达到具有统计学意义的主要和次要终点。
VGX-3100
VGX-3100是东方略与Inovio Pharmaceuticals合作研发的一款DNA免疫治疗产品,用于治疗由人类HPV导致的癌前病变。2021年3月,Inovio Pharmaceuticals宣布VGX-3100与器械CELLECTRATM 5PSP联合治疗HPV-16/18相关宫颈高度鳞状上皮内病变(HSIL)的III期临床试验(REVEAL 1)取得积极结果,在全部可评估受试者中,达到临床疗效的主要终点和所有次要终点。
mRNA-4157/V940
mRNA-4157/V940是一种基于mRNA的新型研究性个性化癌症疫苗,所包含的编码由多达34种新抗原的单一合成mRNA分子组成。该疫苗是根据每位患者肿瘤独特的DNA序列突变特征设计制成,当疫苗被注入患者体内后,会促使患者体内产生特定的T细胞抗肿瘤反应。已公布mRNA-4157/V940联合Keytruda治疗III/IV期黑色素瘤的2b期临床试验KEYNOTE-942/mRNA-4157-P201结果显示:与Keytruda单药治疗相比,mRNA-4157/V940联合Keytruda治疗组使患者的复发或死亡风险降低44%,符合试验的无复发生存期(RFS)的主要终点。2023年2月,FDA基于该试验数据授予mRNA-4157/V940突破性疗法认证,联合Keytruda辅助治疗高危黑色素瘤。
BNT111
BNT111是基于BioNTech完全拥有的FixVac平台的开发的肿瘤疫苗,该平台利用mRNA编码的肿瘤相关抗原的固定组合,旨在触发针对癌症的强大而精确的免疫反应。已发表的BNT111治疗晚期黑色素瘤的I期临床试验结果显示:BNT111可诱导新颖的抗原特异性抗肿瘤免疫应答,并增强针对所编码的黑色素瘤相关抗原(NY-ESO-1、MAGE-A3、酪氨酸酶、TPTE)预先存在的免疫应答,这4种抗原在90%以上的皮肤黑色素瘤中表达,显示出了良好的安全性和初步抗肿瘤效果。2021年11月,BNT111被FDA授予快速通道资格。目前,BNT111已进入II期临床,联和Libtayo(cemiplimab)治疗抗PD-1疗法难治性/复发性不可切除III期或IV期黑色素瘤。
BNT113
BNT-113是一款使用脂质体包裹的mRNA疫苗,编码HPV-16衍生的E6和E7修饰序列,针对HPV16+癌症。已公布的BNT113联合Keytruda一线治疗不可切除复发/转移性头颈部鳞状细胞癌的初步安全数据显示:截至2022年7月5日,在接受治疗的15例患者中,12例已完成安全磨合。安全磨合中的所有患者均有≥1次AE,最常见的是发热(8例)和寒战(6例)。
BNT122
BNT122是利用BioNTech的iNeST技术平台研发的个体化新抗原mRNA疫苗,利用该平台设计的疫苗含有未经修饰的、优化后的mRNA,能够编码多达20种不同的特异性新抗原。2022 ASCO大会上公布的I期临床试验数据显示:BNT122联合PD-L1抑制剂atezolizumab和化疗在接受手术切除的胰腺癌患者中展现出良好的疗效和安全性。
BNT116
BNT116是基于BioNTech的FixVac技术平台开发的癌症疫苗。它表达一组在NSCLC中经常表达的共享肿瘤相关抗原。这些通过mRNA表达的抗原可以激发强力和精准的先天和适应性免疫反应。
CV-8102
CV-8102是一款基于RNA的单链非编码TLR-7/8和RIG-1激动剂,早在2017年就已开展了I期临床研究,用于晚期黑色素瘤、皮肤鳞状细胞癌、头颈部鳞状细胞癌或腺样囊性癌患者的治疗。
JCXH-211
JCXH-211是一款具有差异化优势的自复制型mRNA产品,可在体内长效表达IL-12,潜在适用于多种实体瘤的治疗。结合嘉晨西海自主开发的脂质纳米颗粒递送载体及特有的自复制mRNA技术平台,JCXH-211在临床前研究的多个小鼠和PDX疾病模型中都表现出了优异的肿瘤清除效力,优于采用传统非复制mRNA的类似研究药物。数据显示,JCXH-211在小鼠模型中能有效杀伤肿瘤细胞,消除远端瘤,并预防肿瘤复发。这一优异的肿瘤清除效果来源于RNA复制子引发的强烈的抗病毒免疫反应以及IL-12激活的强效抗肿瘤免疫反应。安全性方面,依托嘉晨西海优化设计的自复制RNA构建以及成熟的CMC工艺平台,JCXH-211在综合GLP毒理学研究中显示出了近乎完美的安全性。而JCXH-212是一款肿瘤新抗原mRNA疫苗。
EB病毒mRNA疫苗
威斯津生物的EB病毒mRNA疫苗由其联合创始人宋相容教授牵头研发,历时长达5年。动物试验研究显示,该mRNA疫苗可显著抑制针EBV阳性肿瘤细胞的生长,安全性较好。2023年2月,威斯津生物在全球首次启动治疗EBV病毒相关恶性肿瘤的mRNA疫苗药物的注册临床试验。
靶向Survivin DC细胞注射液
启辰生生物靶向Survivin DC细胞注射液是将抗原mRNA负载的树突状细胞(DC),分别通过皮内注射和静脉回输的方式给予患者,诱导抗原特异的CD4+和CD8+T淋巴细胞,为原发性脑胶质母细胞瘤患者术后清除肿瘤残余细胞,防止复发,延长生存期,实现长期抗肿瘤效果提供全新的治疗手段。前期非临床研究和研究者发起的探索性临床试验数据已经表明,该mRNA-DC疫苗可诱导出抗Survivin特异性肿瘤免疫反应,安全性良好,有效性显著,试验患者的总生存期显著延长。2023年1月,启辰生生物靶向Survivin DC细胞注射液获批临床,成为全球首个获批开展临床试验的靶向Survivin的mRNA-DC肿瘤治疗性疫苗产品。
CUD002
CUD002是中国首款基于肿瘤新生抗原的mRNA编辑DC肿瘤治疗性疫苗,根据患者独特的突变信息定制设计并制造,能激发患者自身免疫系统识别卵巢癌抗原,产生抗肿瘤免疫反应并杀伤肿瘤细胞。2022年8月,CUD002注射液的IND正式获CDE受理。
XH101
XH101是新合生物研发的靶向胃癌公共新抗原的治疗性mRNA肿瘤疫苗,该靶点为全球首创靶点。该公共新抗原是新合生物通过独家研发的肿瘤新抗原预测算法平台、免疫原性Elispot验证平台及细胞杀伤平台,从大量胃癌患者中筛选、预测、验证出的一段免疫原性强、覆盖度广的肿瘤公共新抗原序列。与传统药物相比,该疫苗具有更强的免疫原性,可诱发人体天然的免疫反应,不仅可以缩短疫苗制备周期,降低患者的治疗成本,还可以在患者体内产生持久有效的免疫记忆,为肿瘤防复发、防转移提供可能。同时,XH101对晚期肿瘤和转移性肿瘤,还可起到有效抑制作用。临床前研究数据显示XH101能够有效激发患者的T细胞免疫应答及肿瘤细胞杀伤效应,具有显著的临床治疗潜力。
近年来全球药企围绕肿瘤疫苗达成多项合作
01
2014年9月,勃林格殷格翰与CureVac公司宣布达成一项排他性全球授权和研发合作协议,获得后者在研肿瘤治疗性疫苗CV9202的全球独家研发和商业化的权利。
02
2016年9月,BioNTech公司已与罗氏旗下Genentech签订全球合作协议,共同开发、生产和商业化基于信使RNA的个性化肿瘤疫苗。据协议,基因泰克将支付BioNtech 3.1亿美元的预付款和近期里程金。
03
2017年10月,CureVac与礼来联手共同开发多达5款癌症疫苗产品,合作总额逾18亿美元。
04
2019年11月,复星医药产业与MimiVax公司达成授权合作,在中国大陆、香港及澳门地区独家临床开发和商业化SurVaxM,授权的适应症为胶质母细胞瘤以及其他肿瘤和非肿瘤疾病。
05
2021年9月,臻和生物与依莫纳达成战略合作,共同开发基于mRNA技术平台的个体化新抗原肿瘤疫苗。
06
2022年3月,BioNTech宣布扩展与再生元的战略研发合作,将联合推动BNT116与PD-1抑制剂Libtayo(cemiplimab)联用的临床试验,用于治疗晚期非小细胞肺癌(NSCLC)患者。
07
2022年5月,CureVac与myNEO达成合作,通过确定特定的癌症抗原开发用于癌症疫苗的新型mRNA免疫疗法。
08
2022年10月,新合生物与信达生物达成合作协议,就个性化新抗原疫苗与信迪利单抗联合治疗肿瘤开展了临床研究。
09
2022年10月,默沙东和Moderna根据现有合作和许可协议的条款,默沙东行使选择权,与Moderna共同开发和商业化mRNA-4157/V940。
10
2023年1月,德国公司BioNTech宣布与英国政府合作,一同测试用于治疗癌症和其他疾病的mRNA疫苗技术。
11
2023年1月,GreenLight生物科学公司和EpiVax Therapeutics签署独家合作协议,共同开发和商业化个性化mRNA癌症的候选疫苗。
12
2023年1月,启辰生生物与华润生物签订战略合作协议,合作开发治疗脑胶质母细胞瘤的mRNA疫苗。
13
2023年3月,康宁杰瑞与斯微生物建立战略合作伙伴关系,重点开展肿瘤领域双特异性抗体药物及mRNA疫苗药物的临床研发合作。
总结
疫苗被誉为20世纪最伟大的科学进步之一,然而目前大多疫苗被应用于传染性疾病的预防。随着肿瘤发病率的增加,疫苗也逐渐被开发用于肿瘤的预防和治疗。从目前研发状况来看,肿瘤疫苗有望成为一种新型的肿瘤免疫疗法。而且,随着高通量基因测序和生物信息学分析技术的快速发展,新抗原不断被筛选和鉴定,个性化癌症疫苗也将成为肿瘤疫苗研发的新方向。从疫苗类型上看,随着mRNA新冠疫苗的成功,mRNA肿瘤疫苗研发进展迅速。据Nature Review的综述预测,2035年全球mRNA预防性疫苗市场规模将达到120-150亿美元,个性化肿瘤疫苗市场规模约为70-100亿美元,蛋白替代疗法等市场规模约40-50亿美元,对应mRNA在治疗和预防领域总市场空间约230-300亿美元。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..