近期,美国基因疗法研究公司Intellia Therapeutic在其第四季度财报中宣布,合作伙伴诺华已结束镰状细胞疗法OTQ923 / HIX763的开发。

据悉,OTQ923/HIX763是诺华与Intellia合作开发的一种基于CRISPR/Cas9基因组编辑的造血干细胞(HSCs)疗法,用于治疗镰状细胞病(SCD)。该疗法将表达胎儿血红蛋白的基因导入患者造血干细胞,目前正处于1/2期临床试验研究。
两家公司最早于2015年12月签订了长达5年的研发合作计划,希望凭借CRISPR/Cas9技术加速CAR-T疗法以及造血干细胞疗法的体外开发。并于2018年12月双方再次扩大协议,除了双方将继续致力于推进CRISPR/Cas9技术的应用外,还将诺华的LNP递送技术扩展到在研项目当中。
无独有偶,另一国际巨头药企葛兰素史克(GSK)也在2022年的第四季度,先后与三家细胞治疗公司解除关于TCR疗法的项目合作。曾经火热的细胞/基因疗法,如今却被大药企“割爱”,细分领域未来路在何方?
01
多款产品遭大药企冷处理
昔日“流量明星”热度不再?
曾经,以CAR-T技术为代表的基因疗法一经问世,便以“天价”与“革命性”疗法的名头赚足了市场的眼球。在引发公众热议的同时,各大药企纷纷入局基因疗法赛道。
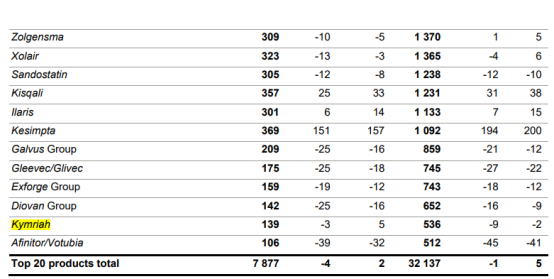
然而,作为全球第一款获批上市的CAR-T疗法Kymriah的拥有者诺华制药,却在逐渐“退热”。根据诺华此前公布的2022年财报数据显示,Kymriah在报告期内全年销售额仅为5.36亿美元,同期比下降9%。这款于2019年上市的产品,似乎开始遭遇瓶颈,这也让Kymriah成为目前所有CAR-T中唯一一款营收下滑的产品。
遭受这股“退热潮”影响的不仅只有诺华。在2022年年底,另一国际巨头GSK就先后解除与三家细胞治疗公司关于TCR疗法的项目合作,引发市场震动:
2022年10月24日,Lyell Immunopharm宣布,GSK退出了细胞治疗2.0联盟,结束了与其合作的实体瘤细胞免疫疗法项目。双方的合作从2019年10月开始,共同开发TCR疗法,原定合作时长为期5年。
紧接着,2022年10月25日,又传出GSK放弃了与Adaptimmune公司合作研发的NY-ESO TCR项目,双方关于该项目的合作于2017年开始。
2022年12月26日,GSK与Immatics关于TCR-T的合作计划也正式终止。
市场观点认为,这一系列的行为在某种方面或是源自于GSK经历了研发管线换帅,其研发策略必然有所调整;另一方面,也传递出GSK对TCR-T疗法的不确定态度。
随后,这一不确定的态度得到企业官方证实。前不久,GSK明确宣布:“终止在细胞与基因疗法方向的研发投入”。短短3个月终止3项细胞疗法合作项目,GSK做出的选择,已经让细分市场不无“寒意”。
此外,不少研发企业也相继结束项目开发。
2023年2月22日,一家名为Graphite Bio的镰状细胞病基因疗法研发企业,在自家旗下nula-cel疗法刚进入临床不久,在评估后就选择推出该领域并决定终止开发nula-cel项目的开发。
同日,另一家研发公司Sangamo公司也选择停止镰状细胞疗法的研发。据悉,Sangamo堪称基因编辑领域,大药企合作的人气王,其合作伙伴不乏吉利德、辉瑞、武田制药、诺华、赛诺菲这些国际大药企。但在2022年1月6日,赛诺菲将镰状细胞病候选药物SAR445136的完全控制权归还给Sangamo。
有市场观点认为,相关的技术疗法在实体瘤领域还未能有实际性突破,目前对应的相关患者群体市场存量不大,增量也十分有限。相较于其他药物,基因药物价格贵,普通患者难以负担,而且疗法具有“一次性”的特点,患者在接受治疗后基本都能够得到治愈,市场规模也在不断的“缩小”,市场前景并不明朗。
02
前沿赛道开始内卷
研发企业何去何从
细胞/基因疗法不仅面临上文所提到的市场问题,还面临靶点集中的困境。
目前,市面上已经获批上市的、或是临床进展较为领先,有望近年上市的基因疗法,主要都集中在CAR-T这一技术衍生的各类靶点产品上。
随之而来的第一大矛盾,是CAR-T产品在实体肿瘤领域的治疗应用效果十分有限。全球已获批上市的CAR-T产品,所对应的适应症都是用于治疗多种不同类型的血液系统恶性肿瘤,但在市场占比超过90%的的实体瘤领域,CAR-T疗法却进展缓慢,困难重重。
有专业分析认为,与血液肿瘤的靶点大多单一且具有特异性不同,实体瘤中肿瘤特异性抗原(TSA)很少,目前发现的肿瘤高表达的抗原多为肿瘤相关抗原(TAA),在正常组织中也有表达。这就带来了很高的脱靶风险,安全性成为关键问题。
事实上,实体瘤具有干扰T细胞转运进行免疫逃逸的机制。一方面,与血液肿瘤细胞呈分散状不同,实体瘤往往形成坚实的团状物,加上丰富的肿瘤相关成纤维细胞(CAF)和血管,形成了一层天然的物理屏障;另一方面,一些实体瘤会抑制某些趋化因子的分泌。趋化因子与其受体的相互作用会促进T细胞向肿瘤微环境的迁移。同时,CAR-T细胞表面也缺乏与实体瘤分泌的趋化因子相匹配的相关受体,造成CAR-T对肿瘤部位的归巢能力差。从应用领域限制了产品市场。
第二大矛盾则是,基因疗法因其特殊性,难以做到像其他药物一般实现大规模批量生产。生产成本高、放量少带来的研发成本平摊,也导致了CAR-T产品的价格居高不下。家庭难以承担、医疗保险难以覆盖以及治疗可支付性问题等都限制了产品市场。
根据Nature期刊的一篇综述,仅仅只是细胞治疗药物,2021年全球管线中就有2073种。这又进一步给相关的研发企业增加了竞争压力,领域专注的企业生存情况不容乐观。
就在2022年9月,世界红细胞载药公司Rubius Therapeutics就宣布裁员75%,砍掉了两条临床研发管线。上市身价曾高达18亿美元,市值已缩水至不足1亿美元,大面积裁员、缩减研发管线、积极转型……这一系列艰难的努力并没能挽救 Rubius Therapeutics。日前,这家公司已申请进行清算和解散。
但仍有市场观点认为,基因疗法的市场前景还未到无路可走的地步。
在国内,已经上市的则有以传奇生物为代表的CAR-T产品Carvykti。据悉,Carvykti是全球第2款BCMA CAR-T疗法,2022年2月28日,传奇生物宣布,其自主研发的细胞治疗产品西达基奥仑赛,在美国FDA成功获批。这是首个国内自主研发在海外获批的细胞疗法。
根据公司公告,产品2022年全年合计1.34亿美元,约为人民币9.24亿人民币。Carvykti在海外的挂网单价已经接近49万美金,可见产品的全年销售量只有寥寥数百份,且平摊每个季度来看,产品销售更显动力不足,表现还有待观望。
事实上,就在近期,科济药业的CAR-T管线CT041,已经展开了针对胃癌实体瘤的临床试验。据悉,CT041则是由科济药业研发的一种潜在全球同类首创的、靶向Claudin18.2的自体CAR-T细胞候选产品,用于治疗CLDN18.2阳性实体瘤,主要治疗胃癌/食管胃结合部腺癌及胰腺癌。
此外,细胞/基因疗法的另一技术路径TCR-T疗法的研究也在实体瘤取得突破,市场关注度不断提升。
2021年3月,Immatics公司宣布开发的TCR细胞疗法,在剂量递增临床试验的早期阶段就显示出抗癌活性。接受治疗的10名患者中,8位患者的肿瘤体积缩小,1位患者获得部分缓解,结果表明TCR-T疗法治疗实体瘤初步临床结果积极。
本土企业加速布局TCR-T领域,进而推动TCR-T疗法行业发展。2020年9月,FDA批准香雪制药控股子公司香雪精准的 TCRT-ESO-A2 的新药临床试验申请,这是国内首个TCR-T项目获FDA临床试验许可。据悉,该临床试验项目是针对实体瘤治疗的国内首个TCR-T项目,用于治疗组织基因型为HLA-A*02:01,肿瘤抗原NY-ESO-1表达为阳性的实体瘤。
国内企业还有天科雅、可瑞生物、复星凯特、药明巨诺、深圳因诺免疫、广州来恩生物医药、深圳宾德生物等多家药企已布局TCR-T细胞疗法。
此外,国外还频频传出通用型TCR-T疗法的消息。如果能够成功实现,对基因疗法产品来说意义重大,或能有效改善治疗的可支付性问题,进一步改善市场前景。
短期而言,细胞/基因疗法的市场前景谈不上乐观;随着新技术、新研究的不断推进,细胞/基因疗法的未来是否依然存在转机,一切有待时间验证。
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..