据FierceBiotech报道,吉利德/Arcus调整了Domvanalimab+赛帕利单抗(TIGIT+PD1)疗法针对NSCLC的III期临床试验方案,放弃与化疗对比,改为直接与Keytruda进行头对头比较。这样调整后,两家公司需要额外增加少量因Keytruda所增加的研发资金,并保持600名患者的入组目标。
吉利德/Arcus正在一系列III期研究中评估TIGIT单抗(Domvanalimab)在NSCLC中的疗效。在一项代号为ARC-10的试验中,这一联合疗法将与标准疗法(SOC)Keytruda直接进行头对头比较,不再包含化疗组。因为目前Keytruda是PD-L1高表达NSCLC的标准疗法。周四上午,Arcus在第三季度业绩报告中宣布了这一调整。

Arcus表示,关于临床试验方案调整是在与FDA讨论之后进行的,该研究还将扩大试验的地理区域。在美国抗癌药物监管格局不断变化的情况下,这一改变强调了使用一种广泛接受的标准疗法作为比较标准在临床和商业化过程中的重要性。
以前,该试验将Domvanalimab联合赛帕利单抗与赛帕利单抗单药进行比较,同时将赛帕利单抗单药与化疗组进行比较。
新试验方案要简单得多,治疗组数将从三个减少为两个,同时保持600名患者的试验人数不变。通过去除化疗组并引入Keytruda,将Domvanalimab联合赛帕利单抗与Keytruda进行头对头比较。根据FDA对1L NSCLC免疫肿瘤治疗主要终点的反馈,总生存期(OS)将被设为主要终点。
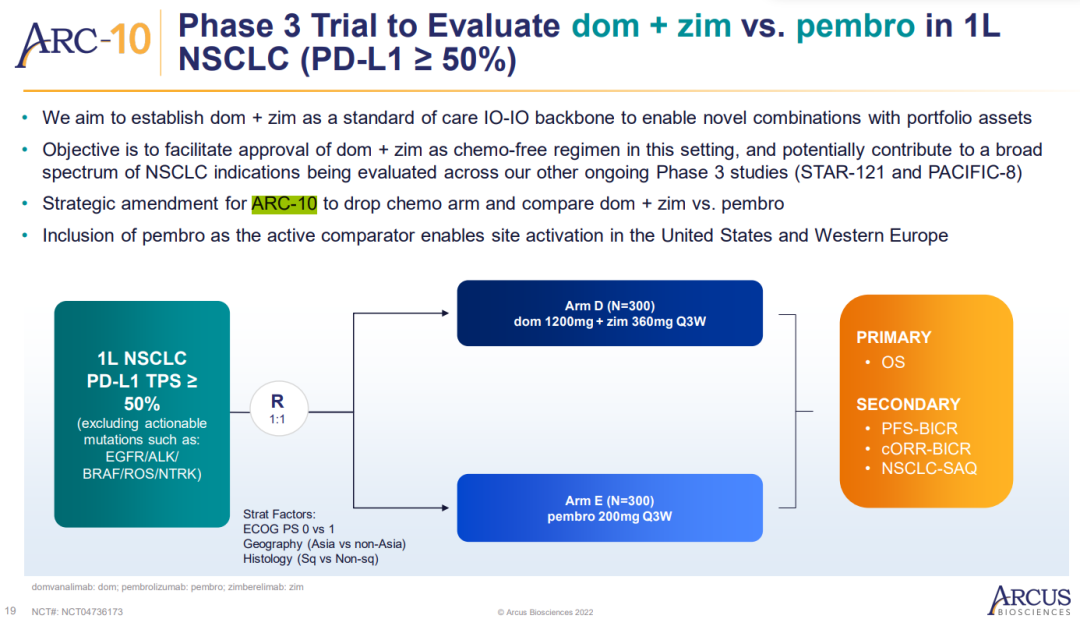
新的临床试验方案(来源:Arcus官网)
Arcus公司CEO Terry Rosen博士表示:“两家公司的目标是挑战Keytruda,在多种治疗场景下创建一种新的抗TIGIT/抗PD-(L)1治疗标准。Arcus还将为该系列增加第4个III期试验。整个后期项目的目的是“在广泛的NSCLC治疗模式中建立domvanalimab的潜在地位”。
在今年早些时候,罗氏的tiragolumab在小细胞肺癌的III期试验中未能证明无进展生存后,TIGIT领域正受到行业分析人士的密切关注。Arcus和吉利德虽然对他们的联合疗法采取了略微不同的方案,但TIGIT假说仍需要临床数据来证明。
SVB证券预计最具影响力的TIGIT产品将在2023年问世,这将取决于吉利德和Arcus的ARC-7试验数据以及罗氏tiragolumab在SKYSCRAPER-01试验中最新数据。SKYSCRAPER-01研究旨在比较tiragolumab联用Tecentriq(PD-L1)对比Tecentriq单药一线治疗PD-L1高表达NSCLC的疗效。
Gilead和Arcus建立了长达10年的合作伙伴关系,合作开发的产品包括Etrumadenant,Domvanalimab,Quemliclustat和Zimberelimab。吉利德为每个项目支付了1.5亿美元,并对Arcus进行了2亿美元的股权投资。该交易于2021年2月进行了修改,吉利德增加了2.2亿美元的投资,并将持股比例提高至19.5%。两家公司目前共同开发产品并分担全球开发成本。
截至2022年9月30日,Arcus的现金、现金等价物和有价证券为11.91亿美元,部分原因是吉利德在2022年1月支付了7.25亿美元。根据Arcus的业绩报告,这些现金应该可以维持公司运营到2026年。
参考资料:https://www.fiercebiotech.com/biotech/gilead-arcus-slim-phase-3-tigit-trial-take-king-keytruda
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..