9月13日,生物技术公司Akero Therapeutics宣布其非酒精性脂肪性肝炎(NASH)新药Efruxifermin在IIb期HARMONY研究中获得了积极数据,Efruxifermin显著改善了NASH患者的肝纤维化情形,且幅度为对照组的2倍。“我们相信试验结果对Akero,乃至对整个非酒精性脂肪性肝炎患者群体,都是一项重要的里程碑。”Akero总裁兼首席执行官Andrew Cheng表示。
非酒精性脂肪性肝炎(NASH)是非酒精性脂肪性肝病的一种严重形式,其特征在于脂肪在肝脏中过度堆积,对肝细胞产生应激和损伤,引起炎症和纤维化,进而发展为肝硬化、肝功能衰竭、癌症甚至死亡。目前,尚无针对此种疾病的获批疗法。
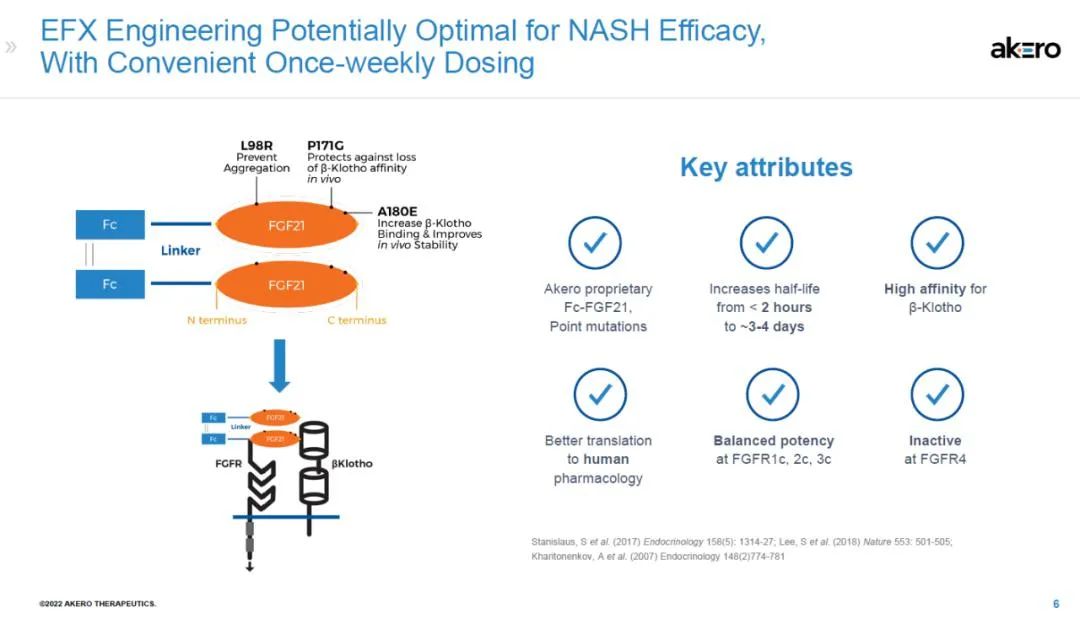
Efruxifermin是一种Fc-FGF21(成纤维细胞生长因子21)融合蛋白,经过工程化改造以模拟天然FGF21的生物活性特征。FGF21是一种全身和个体器官代谢相关的关键调节因子,临床前和临床数据显示,FGF21具有抗纤维化作用,可改善代谢状态并具有治疗NASH的潜力。临床试验表明,Efruxifermin具有逆转纤维化、减少肝脏脂肪、改善血糖控制和脂蛋白分布以及减轻体重的潜力。同时,Efruxifermin通过融合Fc延长半衰期,其半衰期达到3-4天,可以实现每周1次或每2周1次皮下注射给药。
此次的HARMONY研究是一项多中心、随机、双盲、安慰剂对照的IIb期研究,旨在评估Efruxifermin在NASH患者中的有效性和安全性。该研究共招募128例重度NASH患者,随机分为三组,分别接受每周28 mg Efruxifermin、50 mg Efruxifermin或安慰剂的皮下注射。
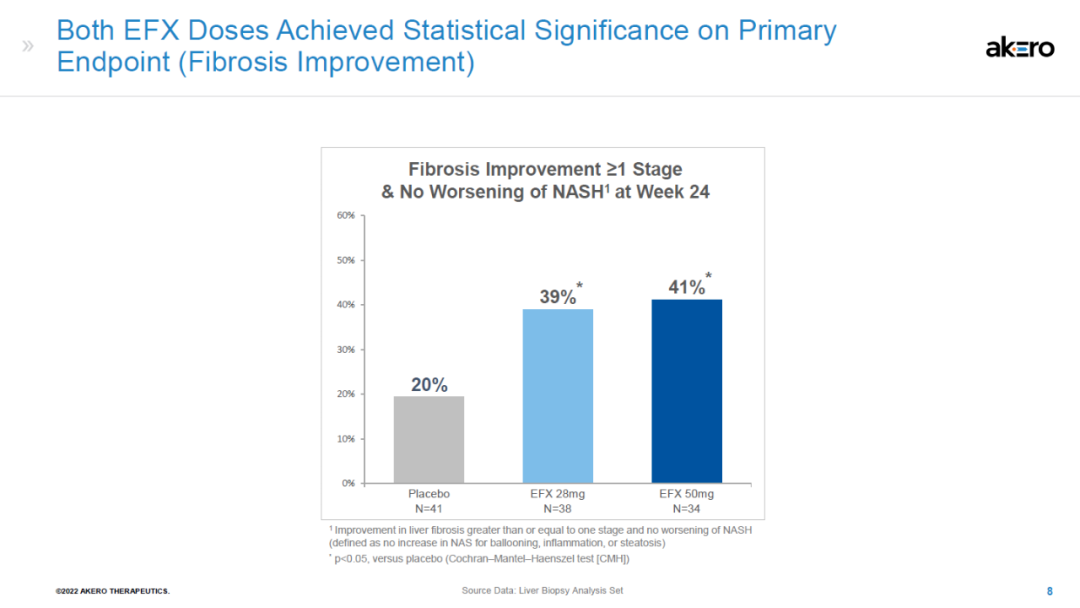
结果显示,在第24周时,Efruxifermin 28mg和50mg 剂量组均达到了研究的主要终点,分别有39%和41%的患者实现了至少一个阶段的肝纤维化改善且NASH没有恶化,而安慰剂组只有20%。同时,该研究还达到了一关键次要终点,Efruxifermin 28mg和50mg治疗组有47%和76%的患者在肝纤维化不恶化的情况下获得了NASH缓解,而安慰剂组为15%。安全性方面,Efruxifermin耐受性良好,最常见的不良反应为1、2级的腹泻、恶心与食欲增加。不过,在试验中有5例患者因副作用而停药,2例为28mg组、3例为50mg组。
Akero总裁兼首席执行官Andrew Cheng表示:“作为美国和欧洲肝移植和肝癌增长最快的原因,NASH代表着一个巨大且不断增长的健康负担。我们相信这些数据非常引人注目,并展现了Efruxifermin的潜力,通过干预疾病进展的各个阶段来满足全球患者的临床需求。”
文 | 医谷
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..