8 月 30 日,安进宣布其 KRAS G12C 抑制剂 Lumakras(sotorasib),在治疗携带 KRAS G12C 突变的经治非小细胞肺癌患者的 III 期 CodeBreaK 200 临床研究中达到主要终点:与标准化疗(静脉注射多西他赛)相比,Lumakras 可显著改善患者的无进展生存期(PFS)。这也是 KRAS G12C 抑制剂首次在随机对照临床试验中达到主要终点。
来自:企业官网
CodeBreaK 200 研究是一项全球随机对照 III 期临床试验,旨在评估与标准化疗相比,Lumakras 在 345 名携带 KRAS G12C 突变非小细胞肺癌 (NSCLC) 患者中的疗效和安全性,这些患者此前至少接受过一种含铂化疗和免疫检查点抑制剂的治疗。研究主要终点是无进展生存期,关键的次要终点包括总生存期、客观缓解率和患者报告的结果。
安进表示,该项实验详细数据将在之后举行的医学会议上分享。
据 Insight 数据库显示, Lumakras 于 2021 年 5 月通过美国 FDA 加速批准途径上市,成为经过近 40 年研究后批准的首个 KRAS 靶向疗法,同时 Lumakras 也是首个被批准用于治疗携带 KRAS G12C 突变的局部晚期或转移性 NSCLC 患者的靶向疗法。此项 III 期临床积极结果将为 Lumakras 从加速批准转化为完全批准提供试验证据。
目前安进也正在探索 Lumakras 与其他药物联用的疗效,正在开展 Lumakras 联合 SHP2 抑制剂、PD-(L)1 的多项临床研究。
今年 7 月,安进披露了 Lumakras 联合赛诺菲/Revolution Medicines 的 SHP2 抑制剂 RMC-4630 部分数据:在 11 例 NSCLC 患者中,3 例(27%)达到部分缓解(PR),其中 2 例在数据截止时仍持续缓解,7 例 (64%) 实现了疾病控制。
8 月,安进披露了 Lumakras 与 K 药、T 药联合治疗安全性及有效性的第一阶段数据。结果显示,对于联合用药,29%(17/58)的患者表现出客观缓解率,表明肿瘤大小减小;在 17 名确诊有反应的患者中,5 名患者的肿瘤持续对治疗有反应,反应持续时间超过 10 个月,而 8 名患者持续有反应。
在安全性方面,与以往 Lumakras 单药治疗的数据相比,Lumakras 联合免疫治疗导致 3-4 级治疗相关不良事件 (trae) 的发生率更高,主要是肝酶升高。不过,在开始联合用药前接受过 Lumakras 治疗的患者,停药和 3-4 级 trae 的发生率较低,且几乎所有 3-4 级 trae 都能得到解决。
CodeBreaK 100/CodeBreaK 101 临床试验结果
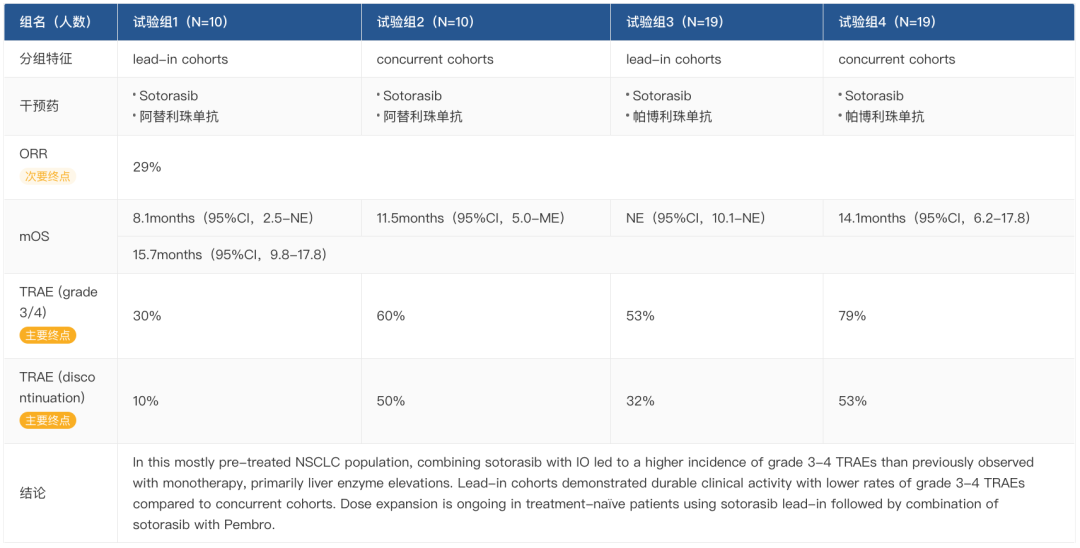
来自:Insight 数据库网页版(http://db.dxy.cn/v5/home/)
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..