今日,BioXcel Therapeutics公司宣布,美国FDA已批准Igalmi(右美托咪定)舌下膜剂上市,用于急性治疗与精神分裂症或I/II型双相情感障碍相关的激越(agitation)。新闻稿指出,这是FDA批准治疗这一患者群体轻度、中度或重度激越的首款口溶舌下膜剂。BioXcel Therapeutics致力于基于人工智能(AI)手段,利用已经获得批准或临床验证过的候选疗法,发掘神经疾病和免疫肿瘤学领域的新疗法。
精神分裂症和双相情感障碍患者中,高达25%会经历激越,每年激越发作可达10~17次,给患者、护理人员和医疗健康系统带来沉重负担。
Igalmi是一种选择性α2肾上腺素受体激动剂右美托咪定的舌下膜剂,通过口腔吸收可以迅速生效。它的发现源于BioXcel的AI技术平台,它可以根据指定适应症,设定搜索条件,从上百万篇科学论文中搜索可能与治疗这一适应症相关的潜在疗法。这一平台发现右美托咪定具有可以治疗激越的所有特征。于是,BioXcel基于这一化合物启动Igalmi的开发。由于右美托咪定已经获批上市,具有已知的安全性特征,这让BioXcel可以大幅度加快它的临床开发速度。从Igalmi的首个临床试验到新药申请(NDA)递交只花了不到3年的时间。
FDA的批准是基于两项关键性随机双盲,含安慰剂对照的3期临床试验结果。在两项试验中,Igalmi的两种不同剂量在接受首次治疗两小时后均达到试验的主要终点,与基线相比,改善评估激越的PEC评分。Igalmi同时达到关键次要终点,显示出快速生效的特征。在接受治疗20~30分钟后与安慰剂相比,出现统计显著差异。
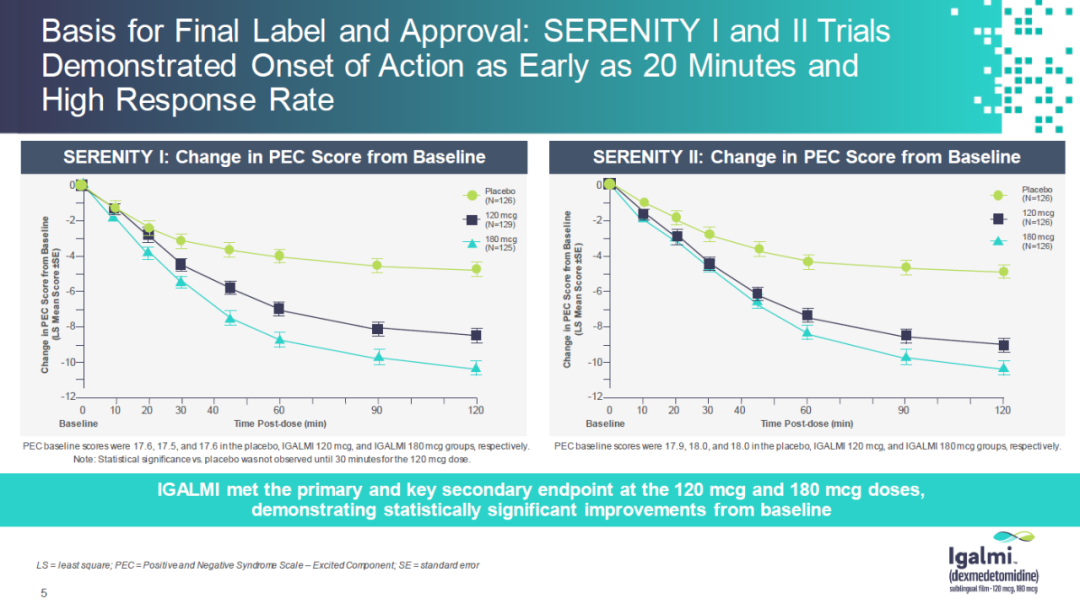
▲Igalmi的3期临床试验结果(图片来源:BioXcel公司官网)
“Igalmi是近10年来首款治疗精神分裂症或I/II型双相情感障碍相关激越的新急性疗法,代表着一种帮助患者控制这一症状的差异化模式。”BioXcel公司首席执行官Vimal Mehta博士表示,“这一里程碑代表着我们向利用AI平台,开发神经疾病变革性疗法的目标迈出的一大步。”
参考资料:
[1] BioXcel Therapeutics Announces FDA Approval of IGALMI™ (dexmedetomidine) Sublingual Film for Acute Treatment of Agitation Associated with Schizophrenia or Bipolar I or II Disorder in Adults. Retrieved April 6, 2022, from https://www.globenewswire.com/news-release/2022/04/06/2417422/0/en/BioXcel-Therapeutics-Announces-FDA-Approval-of-IGALMI-dexmedetomidine-Sublingual-Film-for-Acute-Treatment-of-Agitation-Associated-with-Schizophrenia-or-Bipolar-I-or-II-Disorder-in-.html
[2] A Win for AI: FDA Approves BioXCel Therapy for Bipolar Disorder and Schizophrenia. Retrieved April 6, 2022, from https://www.biospace.com/article/a-win-for-ai-fda-approves-bioxcel-s-treatment-for-bipolar-and-schizophrenia/
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..