▎药明康德内容团队编辑
2022年,生物医药领域的发展仍备受重视,就在开年第一周,已有多家生物医药企业宣布完成融资,助推各自的候选产品研发。1月7日,CAR-T细胞创新药研发公司博生吉宣布完成数亿元B轮融资,同日,小分子抗肿瘤新药研发公司同源康医药也宣布完成3.3亿元C轮融资。此前,据创鉴汇了解到,广州嘉越医药、江苏新元素医药等曾在本周完成超亿元融资,以下是昨日2条融资事件详细介绍。
1.博生吉完成数亿元B轮融资,加速抗肿瘤CAR-T细胞创新药研发
2022年1月7日,博生吉医药科技(苏州)有限公司(简称“博生吉”)宣布完成数亿元B轮融资。本轮融资由中金资本旗下中金启德基金和华泰国信共同领投、磐毅博生、华桐资本跟投。新闻稿显示,本轮融资资金将用于博生吉的PA3-17(CD7-CAR-T细胞)注射液的注册临床试验开展、TAA06(CAR-T细胞)注射液的实体瘤新药临床试验(IND)申请。
博生吉成立于2010年5月31日,总部位于中国苏州,是一家专注于CAR-T细胞创新药研发和临床开发的高新技术企业。该公司以突破性肿瘤细胞免疫治疗技术与产品研发为主要发展目标,旨在针对临床未满足需求的恶性肿瘤领域开发潜在“first-in-class”和“best-in-class”CAR-T细胞药物以造福广大肿瘤患者。新闻稿显示,博生吉拥有强大的自主研发能力,以及完整的从质粒、慢病毒、一直到CAR-T细胞制备的全链条生产体系。该公司凭借其细胞治疗药物研发能力、全自动CAR-T细胞制备工艺技术、以及先进的慢病毒载体工业化生产体系,已成功开发多个细胞产品并进入临床试验阶段,适应症涵盖大部分血液肿瘤和部分实体瘤。
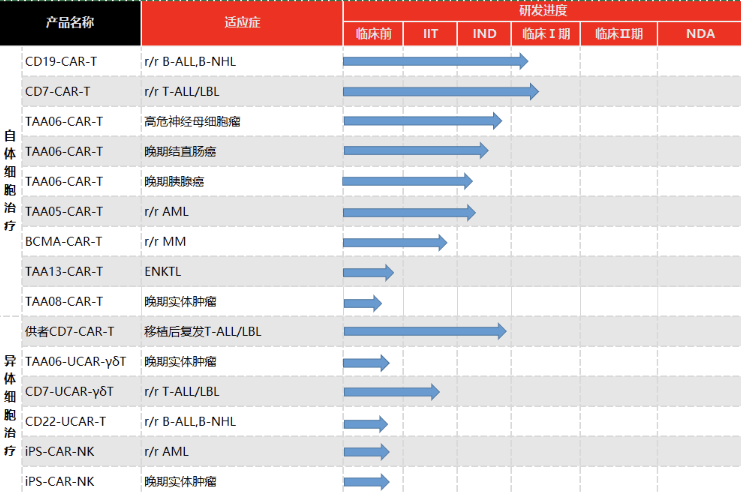
▲博生吉细胞产品研发管线(图片来源:博生吉官网)
据官网资料介绍,博生吉配备有完善的细胞治疗和分子生物学设备,可开展高水平的细胞治疗新技术的研发,涵盖抗原结合域的开发、CAR结构的优化、CAR-T细胞的功能测试、直至体内药效试验的验证,拥有先进的CAR结构及功能验证平台、CAR-T细胞体内药效验证平台、Safeγ UCAR-γδT细胞药物开发平台、诱导多能干细胞(iPSC)诱导的现货型细胞药物开发平台、以及NanoBa双特异性抗体研发平台。博生吉依托自有技术平台开发出一系列全新的具有自主知识产权的CAR-T细胞候选新药,其中针对T淋巴母细胞白血病/淋巴瘤的PA3-17注射液已于2021年8月获得中国注册临床批件,已正式启动患者招募入组。PA3-17注射液还于2021年11月获得了美国FDA授予的孤儿药资格(ODD)。博生吉针对儿童实体瘤的TAA06注射液已进入IND申报的最后阶段,该产品在临床前研究中展现出优异的实体瘤清除能力。
博生吉创始人杨林博士表示,“非常感谢生物医药投资机构对公司的支持。博生吉基于CD7纳米抗体而开发的PA3-17注射液,面向尚无标准治疗策略的、进展快易复发的难治复发性T淋巴母细胞白血病/淋巴瘤,临床价值极大,在前期的临床研究(IIT)中,PA3-17取得了优异的安全性和有效性数据。博生吉还积极布局实肿瘤的CAR-T细胞新药研发,即将提交IND申报的TAA06注射液,首先瞄准儿童肿瘤之王——神经母细胞瘤,这将是儿科肿瘤领域的一个里程碑事件。博生吉特别感谢各位新老投资人的认可和信任,我们一定不负重托,与大家携手共创未来、造福患者,以满足临床真正未满足的需求。”
中金启德创新生物医药投资基金黄序博士表示,“博生吉创始团队曾在优秀癌症研究机构MD安德森癌症研究中心(MD Anderson Cancer Center)工作多年,拥有丰富的一线研发经验。博生吉也是一家拥有完整工艺链的CAR-T细胞药物研发和生产企业,尤其是其独立自主的质粒/慢病毒生产、以及完善的全自动CAR-T细胞工艺开发和制备能力、为CAR-T细胞药物产业化奠定了坚实的基础。博生吉自主研发的PA3-17注射液,是全球首款获批注册临床的自体CD7-CAR-T细胞药物,临床开发进度位列全球第一。我们很荣幸共同领投本轮融资,将坚定支持该公司及团队的产品开发进程,助力其成为全球领先的CAR-T细胞新药研发企业。”
2.同源康医药宣布完成3.3亿元C轮融资,针对肺癌、乳腺癌等开发创新靶点小分子药物
2022年1月7日,浙江同源康医药股份有限公司(以下简称“同源康医药”)宣布完成3.3亿元C轮融资,本轮融资由厚纪资本领投,扬子江基金、浙民投/浙江丝路基金等机构跟投。2021年5月,同源康医药已完成由国海创新资本领投的近4亿元B+轮融资。
同源康医药成立于2017年11月,是一家立足中国、面向国际的创新型生物医药高科技公司,于浙江长兴生命科学园建立了6000平方米新药研发中心,并在上海建立了行政总部、临床医学部和商务拓展部。同源康医药专注于开发潜在“best-in-class”和“first-in-class”的小分子抗肿瘤新药,建立了高效率小分子新药研发平台,其使命是集聚全球药物开发专家,与患者共同探寻健康之源。自2018年8月成型以来,同源康医药已完成两个1类新药的新药临床试验(IND)申报并开展临床试验,两个新靶点的药物从立项推进到临床前候选化合物(PCC)阶段,并将其中一个候选化合物中国权益超1.5亿元“license-out”至丽珠医药公司。
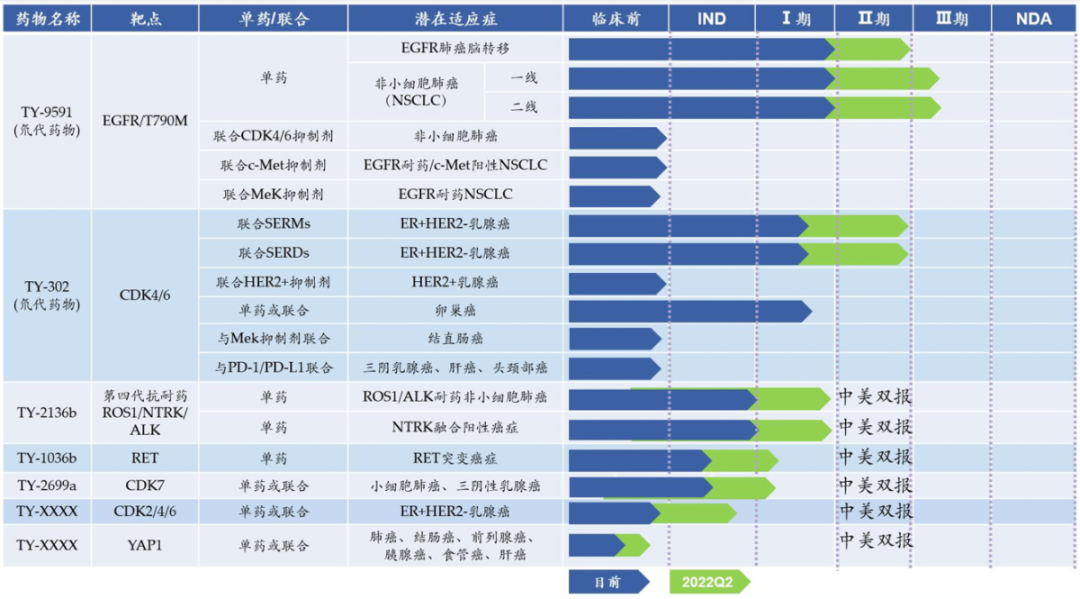
▲同源康医药的在研管线(图片来源:同源康医药官网)
据官网资料显示,同源康医药已建立多条在研管线,适应症涵盖肺癌、乳腺癌、肝癌等。TY-2136b是该公司自主研发的一款在研新一代ROS1/NTRK/ALK多靶点小广谱酪氨酸激酶抑制剂(TKI),已于2021年11月获得美国FDA批准进行临床试验,预计将于今年第二季度启动1期临床试验。临床前研究表明,TY-2136b对ROS1/NTRK/ALK多个靶点均显示出优异的疗效,同时还能有效抑制耐药基因突变,有效解决诸多未满足临床需求。此外,据同源康医药首席科学官李钧博士介绍,TY-2136b还具有一定的穿透血脑屏障能力,对脑转移患者具有潜在优势。
除TY-2136b之外,该公司首个获批临床的在研1.1类化药新药TY9591即将启动临床3期试验,TY-302即将进入2期临床试验,另有一系列创新靶点小分子药物准备申报中美IND。
同源康医药董事长吴豫生博士表示,“非常感谢新老股东对公司的认可,公司专注于抗肿瘤小分子创新药物研发,汇集了一批经验丰富的专家人才,搭建了先进的药物研发实验室,开发了一系列有竞争力的产品管线,受到众多知名投资机构的认可,公司也将继续提高产品推进效率,回报各位投资人和患者的信任。”
厚纪资本合伙人何超先生表示:“同源康医药针对肺癌、乳腺癌等重大未满足临床需求,在非小细胞肺癌(NSCLC)、HR+/HER2-乳腺癌亚洲女性绝经前用药方面做了很深入的研究和前瞻性探索,依托成熟的小分子开发和成药性评价平台,开发一系列涵盖NSCLC各种靶点抑制剂、CDK系列小分子药物。我们很高兴可以和这么优秀的公司合作,也期待他们未来在肺癌及全球大量未满足临床需求的肺癌耐药突变、CDK等细胞周期激酶领域做出世界级的创新药,相信同源康医药未来的发展会越来越好。”
结语
据不完全统计,2022年第一周,除前述介绍的博生吉医药、同源康医药外,江苏新元素医药、苏州克睿基因、赛岚医药科技(深圳)、四环医药旗下控股子公司轩竹生物、广州嘉越医药、爱科诺生物医药(苏州)等近十家中国biotech公司均分别完成超亿元融资,推进各自在研新药临床开发,以满足临床真正未满足的需求,造福患者。
参考资料:
[1] 博生吉完成数亿元人民币B轮融资 | 会员动态. Retrieved 2022-01-07, from https://mp.weixin.qq.com/s/ZgzP6XWg57dJ3dZ6DS6W1A
[2] 【首发】同源康医药完成3.3亿元C轮融资,厚纪资本领投,凯乘资本担任独家财务顾问. Retrieved 2022-01-07, from https://mp.weixin.qq.com/s/BW0QkItbFIJ7kgLbarwHyg
四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..关于收取2026年度会费的通知
各会员单位: 在过去的一年里,..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..