2020年诺贝尔化学奖授予埃马纽埃尔·卡彭蒂耶(Emmanuelle Charpentier)和詹妮弗·杜德纳(Jennifer A. Doudna),以表彰她们在“基因组编辑方法”研究领域作出的贡献。而这里的基因组编辑方法,指的正是当下热门的CRISPR/Cas9基因编辑技术。
CRISPR/Cas作为基因编辑系统被应用最早开始于2012年。Jennifer Doudna和Emmanuelle Charpentier通过体外实验证明:成熟的crRNA通过碱基互补配对与tracrRNA形成特殊的双链RNA结构,指导cas9蛋白在目标DNA上引起双链断裂。在与crRNA指导序列互补的位点,cas9蛋白的HNH核酸酶结构域切割crRNA的互补链,而cas9蛋白RuvC样结构域切割非互补链。当双tracrRNA:crRNA被嵌合到一条RNA时,同样可以指导cas9切割双链DNA。她们的研究证明,在双链RNA指导下切割双链DNA断裂的内切酶家族并揭示了CRISPR/Cas系统在RNA指导下进行基因编辑的巨大潜力。
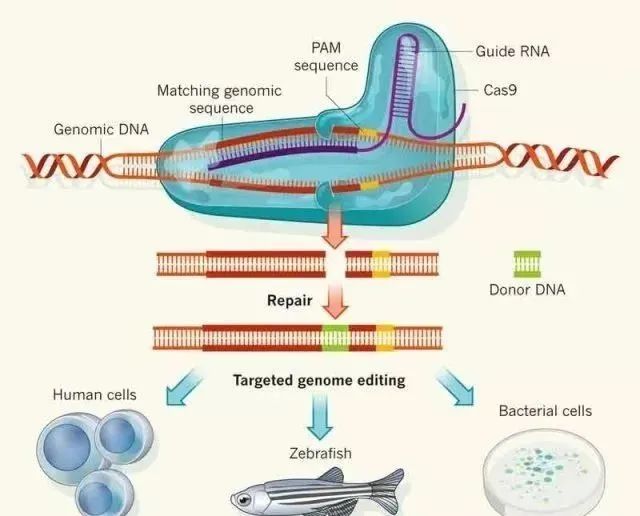
基因编辑技术的基本原理,图源origene.com
2013年,发现CRISPR/Cas9系统可高效地编辑基因组。张锋等使用CRISPR系统成功地在人类细胞和小鼠细胞中实现了基因编辑。
从此开始,CRISPR/Cas9技术给生命科学领域带来了巨大冲击,CRISPR/Cas9相关研究成果频频登上Cell、Nature、Science等顶级期刊,更是拿到了2020的诺贝尔化学奖。
而最近有研究表明,通过CRISPR–Cas9进行基因组编辑或会在原代细胞中诱导p53所介导的DNA损伤反应,从而阻碍细胞的生长,这或许就会导致对已经存在的p53突变的细胞的选择。
近日,一篇发表在国际杂志Nature Communications上题为“A systematic genome-wide mapping of oncogenic mutation selection during CRISPR-Cas9 genome editing”的研究报告中,来自美国国立卫生研究院等机构的科学家们通过研究发现,基于CRISPR -Cas9的基因编辑(尤其是基因敲除)或许会让细胞产生于癌症相关的基因突变形式。这些研究发现强调了对接受基于CRISPR -Cas9的基因编辑疗法来修饰癌症相关基因突变患者及时监测的必要性。

图片来源:https://www.nature.com/articles/s41467-021-26788-6
研究者Ani Deshpande博士说道:本文研究结果表明,在多种不同的细胞类型中,CRISPR基因编辑或许会给携带与癌症相关基因突变的细胞带来一定的选择性优势,比如p53和KRAS基因等。当利用CRISPR-Cas9来对基因组进行编辑时,携带癌症相关突变的细胞很有可能会选择性地存活下来,而且这要比科学家们此前所了解的更为普遍一些。
CRISPR-Cas9的工作原理是在DNA序列的特定位点上产生双链DNA断裂,从而就能使得科学家们靶向作用并编辑特定的基因,然而,p53基因能通过抑制细胞生长来对双链的断裂产生反应,这意味着经历CRISPR细胞的生长和分裂效率会降低,而且携带p53基因突变的细胞会持续生长并分裂,从而使其更具优势。如果发生基因组错误,p53基因就会停止细胞分裂,并试图纠正细胞出现的问题;如果错误不能被修复的话,p53就会在细胞发生癌变之前开启程序性的细胞死亡,这就使得p53成为了一种关键的抗癌基因,失去其功能就会让人们对肿瘤更加易感。P53基因如此重要以至于其被称之为基因组的守护者。
研究者Eytan Ruppin指出,这篇文章中,我们分析了p53对近1000个人类细胞系中出现的双链断裂所产生的反应,在几乎所有的细胞类型中,我们都发现,当进行CRISPR-Cas9所介导的基因敲除后,携带正常p53基因的细胞就会表现出生长减缓,而携带突变p53基因的细胞则受到的影响较小,从而就能使其生长迅速且优于正常细胞。
此外研究者还发现,CRISPR或能介导携带其它癌症相关突变的细胞表现出一定的优势,比如携带KRAS癌基因的细胞等。这并不是研究者第一次揭示出CRISPR基因编辑技术或会引入潜在的危险改变,然而本文研究却是研究人员首次在多种人类细胞中揭示出CRISPR技术所带来的潜在影响。
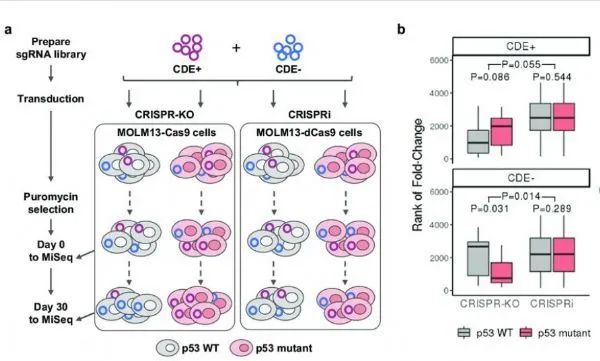
通过汇集CRISPR筛查来证实等基因MOLM13细胞系中p53 CDE基因。
图片来源:Sinha, S., et al. Nat Commun 12, 6512 (2021). doi:10.1038/s41467-021-26788-6
相关研究结果表明,在使用基于CRISPR的基因疗法时或许需要谨慎,尤其是在治疗携带p53或KRAS基因突变的患者时,目前研究人员正在开发的CRISPR疗法能纠正很多人类组织中的突变,但正如很多科学家指出的那样,我们或许需要谨慎,因为在使用CRISPR-Cas9基因编辑的过程中或许就会选择出携带关键驱动癌症基因突变的细胞,而这或许具有一定的潜在危险。但幸运的是,研究者最近开发的新型CRISPR编辑技术或许就会降低这种风险。
研究者Deshpande表示,早期的CRISPR技术会产生双链断裂,但更为现代的迭代技术或许进行更简单的编辑来靶向作用RNA;如果我们利用一种非切割版本的CRISRP,或许就会避免产生很多问题,这对于患者而言或许是非常好的消息。
综上,尽管存在潜在的风险,但研究者认为,CRISPR技术依然一种令人兴奋的革命性技术,而诸如上述障碍并非不能克服。未来研究人员将会继续深入研究,出足够安全用于患者机体的基因编辑技术。
原始出处:
Sinha, S., Barbosa, K., Cheng, K. et al. A systematic genome-wide mapping of oncogenic mutation selection during CRISPR-Cas9 genome editing. Nat Commun 12, 6512 (2021). doi:10.1038/s41467-021-26788-6
关于召开第七届九次理事会暨会长办公会
各相关单位: 经研究,四川省医..四川省医药保化品质量管理协会举办2026
当前,制药行业正处于合规升级与绿..关于举办四川省药品生产企业拟新任质量
各相关企业: 新修订的《中华人..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部
2026年4月8日上午,省医药保化品质..四川省医药保化品质量管理协会党支部召
按照省市场监督管理局社会组织联合..